1 . 元素在周期表中的位置与元素原子的结构、性质间的关系
(1)在元素周期表中,同族元素价层电子数_______ ,是同族元素性质_______ 的结构基础。
(2)长周期比短周期多出的元素,其原子的最外层电子数_______ 2(Pd除外),所以它们全部是_______ 。
(1)在元素周期表中,同族元素价层电子数
(2)长周期比短周期多出的元素,其原子的最外层电子数
您最近一年使用:0次
名校
2 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。如图元素周期表的回答下列问题。

(1)元素 Ga 在元素周期表中的位置为________ 。
(2) Sn 的最高正价为________ ;As 的气态氢化物为_____ ;CCl4的电子式________
(3)根据元素周期律推断:
①阴影部分元素氢化物热稳定性最高的是______ (填化学式)。
②H3AsO4、H2SeO4的酸性强弱:H3AsO4___ H2SeO4(填“>”、“<”或“=”)。
③简单氢化物的熔沸点:H2O__ H2S(填“>”“<”或“=”)。
(4)硒(Se)化铟(In)是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是____ 。
a.原子半径:In>Se
b.In 的金属性比 Se 强
c.In 的金属性比 Al 弱
d.硒化铟的化学式为 InSe2

(1)元素 Ga 在元素周期表中的位置为
(2) Sn 的最高正价为
(3)根据元素周期律推断:
①阴影部分元素氢化物热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱:H3AsO4
③简单氢化物的熔沸点:H2O
(4)硒(Se)化铟(In)是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是
a.原子半径:In>Se
b.In 的金属性比 Se 强
c.In 的金属性比 Al 弱
d.硒化铟的化学式为 InSe2
您最近一年使用:0次
3 . 根据如图,已知有机物A,B,C,D,E,F 有以下转化关系。A是分子量为 28 的气体烯烃,其产量是衡量一个国家石油化工生产水平的标志;D是食醋的主要成分,E 是不溶于水且具有香味的无色液体,相对分子质量是C的 2倍,F 是一种高分子化合物。结合如图关系回答问题:

(1)写出B、D 中官能团的名称:B___________ 、D___________ ;
(2)写出下列反应的化学方程式:
①___________ ;该反应类型是___________ 。
②___________ ;该反应类型是___________ 。
④___________ 。
F是常见的高分子材料,合成F的化学方程式是___________ 。
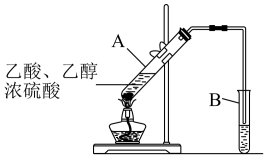
(3)根据上图,实验室用该装置制备E,试管A中浓硫酸的作用是___________ ;B中的试剂是___________ ;B中导管的位置在液面上方,目的是:___________ 。

(4)根据上图,某化学课外小组设计了这样的装置(图中铁架台、铁夹、加热装置均已略去)制取E,与原装置相比,该装置的主要优点有:___________ 。(至少回答两点)

(1)写出B、D 中官能团的名称:B
(2)写出下列反应的化学方程式:
①
②
④
F是常见的高分子材料,合成F的化学方程式是

(3)根据上图,实验室用该装置制备E,试管A中浓硫酸的作用是

(4)根据上图,某化学课外小组设计了这样的装置(图中铁架台、铁夹、加热装置均已略去)制取E,与原装置相比,该装置的主要优点有:
您最近一年使用:0次
名校
解题方法
4 . 依据图中氮元素及其化合物的转化关系,回答问题:
(1)图1中,X的化学式为________ ,从化合价上看,X具有___________ 性(填“氧化”或“还原”)。
(2)根据图2回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为________ 。
②下列试剂不能用于干燥NH3的是________ (填字母)。
A.浓硫酸 B.碱石灰 C.NaOH固体
③氨气是重要的化工原料,可以合成多种物质,写出氨气催化氧化的化学方程式________ 。
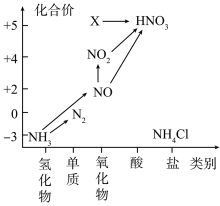
(1)图1中,X的化学式为
(2)根据图2回答下列关于NH3的问题:

①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为
②下列试剂不能用于干燥NH3的是
A.浓硫酸 B.碱石灰 C.NaOH固体
③氨气是重要的化工原料,可以合成多种物质,写出氨气催化氧化的化学方程式
您最近一年使用:0次
5 . A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如下图所示(反应条件及其他产物已略去):
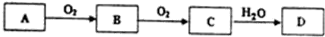
(1)若A、D的水溶液均呈酸性,且D为强酸.
①A、D分别为A:_____ ,D:_____ .(填写化学式,下同)
②写出B→C转化的化学方程式:_____ .
③简述检验B物质的方法_____ .
④写出D的浓溶液和Cu在加热条件的化学方程式_____ .21*cnjy*com
(2)若A的水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使蓝色的湿润石蕊试纸变红.
①工业上合成A的化学方程式:_______________ .在实验室中则用加热固体混合物的方法制取气体A,其化学方程式为_____ .
②写出C→D的化学方程式,并用双线桥标出电子转移的方向和数目.____________
③写出A→B的化学方程式_____
④1.92g铜投入一定的D浓溶液中,铜完全溶解,共收集到672mL气体(标准状况).将盛有此气体的容器倒扣在水中,通入标准状况下一定体积的O2,恰好使气体完全溶于水中,则通入O2的体积为_____ mL.
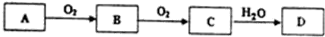
(1)若A、D的水溶液均呈酸性,且D为强酸.
①A、D分别为A:
②写出B→C转化的化学方程式:
③简述检验B物质的方法
④写出D的浓溶液和Cu在加热条件的化学方程式
(2)若A的水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使蓝色的湿润石蕊试纸变红.
①工业上合成A的化学方程式:
②写出C→D的化学方程式,并用双线桥标出电子转移的方向和数目.
③写出A→B的化学方程式
④1.92g铜投入一定的D浓溶液中,铜完全溶解,共收集到672mL气体(标准状况).将盛有此气体的容器倒扣在水中,通入标准状况下一定体积的O2,恰好使气体完全溶于水中,则通入O2的体积为
您最近一年使用:0次



