解题方法
1 . X、Y、Z、W是原子序数依次增大的短周期主族元素且均为非金属元素,X原子最外层电子数为内层电子数的2倍,Z是地壳中含量(质量分数)最高的元素,W与X位于同一主族。下列说法正确的是
| A.XZ、YZ均为酸性氧化物 | B.非金属性: |
C.简单氢化物的沸点: | D.氧化物对应水化物的酸性: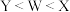 |
您最近一年使用:0次
名校
2 . 某血液化验单中,高密度酯蛋白胆固醇的含量为 ,该体检指标所采用的物理量是
,该体检指标所采用的物理量是
 ,该体检指标所采用的物理量是
,该体检指标所采用的物理量是| A.物质的量浓度 | B.摩尔质量 | C.质量分数 | D.溶解度 |
您最近一年使用:0次
2020-03-10更新
|
72次组卷
|
2卷引用:广西崇左市2019-2020学年高一上学期期末考试化学试题
名校
3 . 已知硫铁矿的主要成分是FeS2(铁元素呈+2价,硫元素呈-1价)。以下是分析硫铁矿中FeS2含量的三种方法,各方法的操作流程图如下:
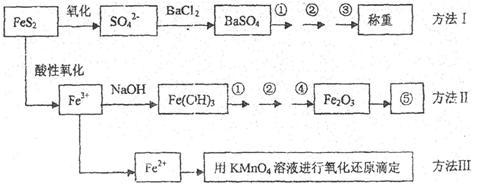
请回答下列问题:
(1)流程图中操作①、②、③分别指的是:①____________ 、②___________ 、③________ 。
操作④、⑤用到的主要仪器是:④_________ 、⑤__________ (每空填1~2个仪器)。
(2)判断溶液中SO42-离子已沉淀完全的方法是_______________________________ 。
(3)某同学用方法Ⅲ测定试样中Fe元素的含量,需要准确配制KMnO4标准溶液,下列因素导致所配制的溶液浓度偏大的有_______
A.砝码生锈 B.定容时俯视
C.称量时物质和砝码位置反了(需要游码) D.容量瓶用待装液润
(4)某同学采用方法Ⅱ分析矿石中的Fe含量,发现测定结果总是偏高,则产生误差的可能原因是______________________________________ 。
(5)称取矿石试样1.60g,按方法Ⅰ分析,称得BaSO4的质量为4.66g,假设矿石中的硫元素全部来自于FeS2,则该矿石中FeS2的质量分数是_________________________ 。

请回答下列问题:
(1)流程图中操作①、②、③分别指的是:①
操作④、⑤用到的主要仪器是:④
(2)判断溶液中SO42-离子已沉淀完全的方法是
(3)某同学用方法Ⅲ测定试样中Fe元素的含量,需要准确配制KMnO4标准溶液,下列因素导致所配制的溶液浓度偏大的有
A.砝码生锈 B.定容时俯视
C.称量时物质和砝码位置反了(需要游码) D.容量瓶用待装液润
(4)某同学采用方法Ⅱ分析矿石中的Fe含量,发现测定结果总是偏高,则产生误差的可能原因是
(5)称取矿石试样1.60g,按方法Ⅰ分析,称得BaSO4的质量为4.66g,假设矿石中的硫元素全部来自于FeS2,则该矿石中FeS2的质量分数是
您最近一年使用:0次
4 . 某同学用中和滴定的方法测定混有少量Na2CO3的NaOH固体中NaOH的含量,准确称取2.0 g样品配制成200 mL溶液,然后分三次各取20.00 mL溶液于三个洁净的锥形瓶中,分别加入过量BaCl2溶液和1~2滴指示剂,用浓度为0.2000 mol·L-1的盐酸标准液进行滴定。
(1)滴定时应选用____ 作指示剂;到达滴定终点的实验现象是____ 。
(2)下列操作会导致烧碱样品中NaOH含量测定值偏高的是____ 。
E.滴定终点前加水清洗锥形瓶
F.指示剂变色后立即读数
(3)实验相关数据记录如下:
依据表中数据,计算样品中NaOH的质量分数____ 。
(1)滴定时应选用
(2)下列操作会导致烧碱样品中NaOH含量测定值偏高的是
| A.锥形瓶未用待测液润洗 |
| B.酸式滴定管未用标准液润洗 |
| C.在滴定前有气泡,滴定后气泡消失 |
| D.滴定前平视读数,滴定结束俯视读数 |
F.指示剂变色后立即读数
(3)实验相关数据记录如下:
| 实验编号 | V(烧碱溶液)/mL | V(HCl)/mL | |
| 初读数 | 末读数 | ||
| 1 | 20.00 | 0.60 | 20.62 |
| 2 | 20.00 | 0.80 | 20.78 |
| 3 | 20.00 | 0.20 | 20.90 |
依据表中数据,计算样品中NaOH的质量分数
您最近一年使用:0次
5 . 电石中的碳化钙和水能完全反应: CaC2+2H2O→C2H2↑+Ca(OH)2
现在使该反应产生的气体排水,测量排出水的体积,可计算出标准状况乙炔的体积,从而可测定电石中碳化钙的含量。
(1)用下列仪器和导管组装该实验装置:

如果所制气体流向从左向右时,上述仪器和导管从上到下和从左到右直接连接的顺序(填各仪器、导管的序号)是:( ) 接( ) 接( ) 接( ) 接( ) 接( ) ;
(2)一般实验产生的气体含有______ (填化学式,至少2种)等杂质导致测定结果偏大,通常用______ (填化学式)溶液除去;
(3) 实验室制取乙炔时,为了______ 通常用饱和食盐水代替蒸馏水;
(4)若实验时称取的电石1.60g,测量排出水的体积后,折算成标准状况乙炔的体积为448mL,此电石中碳化钙的质量分数是_______ 。
现在使该反应产生的气体排水,测量排出水的体积,可计算出标准状况乙炔的体积,从而可测定电石中碳化钙的含量。
(1)用下列仪器和导管组装该实验装置:

如果所制气体流向从左向右时,上述仪器和导管从上到下和从左到右直接连接的顺序(填各仪器、导管的序号)是:
(2)一般实验产生的气体含有
(3) 实验室制取乙炔时,为了
(4)若实验时称取的电石1.60g,测量排出水的体积后,折算成标准状况乙炔的体积为448mL,此电石中碳化钙的质量分数是
您最近一年使用:0次
6 . 短周期元素X、Y、Z、W、N的原子序数依次增大,其中X的一种同位素原子没有中子,Y的一种核素可做考古学家测文物的年代,Z为地壳中含量最多的非金属元素,相同质量的W的单质在空气中缓慢氧化的产物与其在空气中燃烧产物不同,但转移的电子数相同,N原子为所在周期中原子半径最小的原子(稀有气体除外)。
(1)写出X元素没有中子的原子符号___________ ;Y与X形成的X元素的质量分数最高的分子的结构式___________ ;X、Z、N形成的原子个数比1:1:1的分子的电子式___________ 。
(2)用电子式表示W2Z形成过程___________ ;
(3)Z、W、N的简单离子半径从大到小的顺序___________ (用离子符号表示);
(4)甲由上述元素X、Y元素形成的18电子分子,常温下是气态,可燃烧。
①甲分子中若两个H原子被Br取代,则可生成___________ 种溴代物;
②若把甲与氧气设计成燃烧电池(KOH溶液为电解质溶液),则负极反应的方程式为___________ ;放电一段时间后溶液的碱性___________ (增强、减弱、不变)。
(1)写出X元素没有中子的原子符号
(2)用电子式表示W2Z形成过程
(3)Z、W、N的简单离子半径从大到小的顺序
(4)甲由上述元素X、Y元素形成的18电子分子,常温下是气态,可燃烧。
①甲分子中若两个H原子被Br取代,则可生成
②若把甲与氧气设计成燃烧电池(KOH溶液为电解质溶液),则负极反应的方程式为
您最近一年使用:0次
13-14高三上·福建莆田·期中
名校
7 . 下列关于碱金属及其化合物的叙述错误的是( )
| A.金属钠投入Ca(HCO3)2溶液,反应后有白色沉淀析出 |
| B.干粉灭火器能用于扑灭金属钠、钾的着火 |
| C.生理盐水的质量分数为0.9%,与人体的血液中含量相同,它的溶质是NaCl |
| D.取用金属钠、钾时,所需实验用品有小刀、镊子、滤纸、玻璃片 |
您最近一年使用:0次
2016-12-09更新
|
1100次组卷
|
3卷引用:2012届福建省莆田二中高三上学期期中考试化学试卷
(已下线)2012届福建省莆田二中高三上学期期中考试化学试卷山西省太原市第五中学校2020届高三上学期9月阶段性检测化学试题江西省宜春市丰城市第九中学日新班2023-2024学年高二下学期开学考试化学试题
8 . 由A、B两种烃组成的混合物,当混合物总质量一定时,无论A、B以何种比例混合,完全燃烧消耗氧气的质量为一恒量。对A、B两种烃有下面几种说法:①互为同系物;②互为同分异构体;③具有相同的最简式;④两种烃中碳的质量分数相同。正确的结论是
| A.①②③④ | B.①③④ | C.③④ | D.①②③ |
您最近一年使用:0次
9 . 有A、B、C、D四种有机物,A、B属于烃类物质,C、D都是烃的衍生物。A是含氢质量分数最大的有机物,分子结构为正四面体;B的产量可以用来衡量一个国家石油化学工业的发展水平,也是一种植物生长调节剂;C的相对分子质量为46,能与Na反应,但不能与NaOH溶液反应;D的空间填充模型为 ,用pH试纸测试该物质的水溶液,试纸变红。请回答下列问题:
,用pH试纸测试该物质的水溶液,试纸变红。请回答下列问题:
(1)B的结构式是___________ ,D中官能团的名称是___________ 。
(2)已知B可以发生如图转化过程:
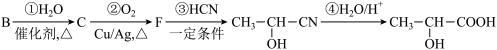
①写出反应②的化学方程式:___________ 。
②反应③的反应类型是___________ 。
 ,用pH试纸测试该物质的水溶液,试纸变红。请回答下列问题:
,用pH试纸测试该物质的水溶液,试纸变红。请回答下列问题:(1)B的结构式是
(2)已知B可以发生如图转化过程:
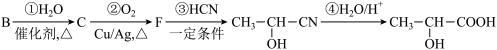
①写出反应②的化学方程式:
②反应③的反应类型是
您最近一年使用:0次
解题方法
10 . 互为同分异构体的物质不可能
| A.具有相同的相对分子质量 |
| B.具有相同的熔、沸点和密度 |
| C.具有相同的分子式 |
| D.各组成元素的质量分数分别相同 |
您最近一年使用:0次



