2015-2016学年四川省资阳市高二下学期期末化学试卷
四川
高二
期末
2017-07-27
459次
整体难度:
适中
考查范围:
化学反应原理、认识化学科学、化学实验基础、有机化学基础、常见无机物及其应用
一、单选题 添加题型下试题
| A.纽扣银锌电池体型小,含有害物质少,用后可以随意丢弃 |
| B.采用外加电流的阴极保护法可防止钢铁锈蚀 |
| C.裂化汽油与直馏汽油的成分不完全相同 |
| D.色谱法可用于分离、提纯有机物 |
【知识点】 金属的电化学腐蚀与防护
A.乙烯(C2H4)的电子式: |
| B.丙烯(C3H6)的结构简式:CH2CHCH3 |
C.立方烷(C8H8)的键线式: |
D.溴乙烷(C2H5Br)的比例模型: |
【知识点】 化学用语
| A.用托盘天平称取8.75 g食盐 |
| B.用25 mL量筒量取12.36 mL盐酸 |
| C.用广泛pH试纸测得某溶液pH值为3.5 |
| D.用碱式滴定管移取NaOH溶液23.10 mL |
【知识点】 仪器使用与实验安全
| A.电镀铜时用待镀的金属制品作阳极、铜作阴极 |
| B.AlCl3熔点低,电解熔融AlCl3冶炼铝更节能 |
| C.电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属 |
| D.氯碱工业实际是指电解饱和食盐水的工业生产 |
【知识点】 电解池
A.NH4Cl溶液呈酸性:NH4++2H2O NH3·H2O+H3O+ NH3·H2O+H3O+ |
| B.氨气溶于水,溶液呈碱性:NH3·H2O=NH4++OH- |
C.NaHSO4溶液可以导电:NaHSO4 Na++H++SO42- Na++H++SO42- |
D.常温下,饱和H2CO3溶液pH=4:H2CO3 2H++CO32- 2H++CO32- |
【知识点】 弱电解质的电离方程式解读 水解的离子方程式书写解读
| A.溶液的c(H+)=10-7 mol/L |
| B.溶液的溶质为盐 |
| C.溶液中既含有H+又含有OH- |
D.混合溶液中,pH=- |
【知识点】 水的电离及溶液的酸碱性
| A.7、2 | B.7、1 | C.4、2 | D.4、1 |
| A.d、a、b、c | B.d、b、a、c |
| C.a、b、c、d | D.a、b、d、c |
| A.乙炔中碳原子形成的是sp杂化轨道,因此易于发生加成反应和氧化反应 |
| B.金属锂的摩尔质量小,因此锂电池具有比能量大的优点 |
| C.苯环中含有大π键,因此易于发生加成反应,难于发生取代反应 |
| D.相同温度、相同浓度的CH3COOH与NH3·H2O的电离能力相同,因此CH3COONH4溶液呈中性 |
【知识点】 烃
① 0.1 mol/L HNO2溶液的pH=2;
② HNO2溶液不与Na2SO4溶液反应;
③ HNO2溶液的导电性比盐酸弱;
④ 25℃时NaNO2溶液的pH大于7;
⑤ 将pH=2的HNO2溶液稀释至原体积的100倍,溶液的pH=3.7
| A.①③④ | B.①④⑤ | C.②③④ | D.③④⑤ |
【知识点】 一元强酸与一元弱酸的比较解读

| A.分子式为C25H20,属于苯的同系物 |
| B.该物质不能发生硝化反应 |
| C.能使溴水和酸性KMnO4溶液褪色 |
| D.1 mol该物质最多能与12 mol氢气发生反应 |
【知识点】 有机物的结构特点
二、未知 添加题型下试题
三、单选题 添加题型下试题
| A.108∶1∶108 | B.1∶1∶108 |
| C.1∶108∶1 | D.1∶108∶108 |
【知识点】 盐类的水解
| A.0.1mol/L醋酸溶液加水稀释,电离平衡正移,电离平衡常数增大 |
| B.0.1mol/L醋酸溶液中加入锌粒,电离平衡正移,c(H+)增大 |
| C.0.1mol/L醋酸钠溶液中加入醋酸钠固体,水解平衡正移,c(OH-)增大 |
| D.在AgCl饱和溶液中加入AgCl固体,沉淀溶解平衡正移,c(Ag+)增大 |
【知识点】 弱电解质的电离平衡 难溶电解质的溶解平衡
| A.CH4C2H4C3H4 | B.CH4C2H6C2H2 |
| C.C2H2C2H4C3H6 | D.C2H4C3H6C4H8、 |
【知识点】 烃
| A.欲除去乙烷中混有的乙烯可选用酸性KMnO4溶液洗气 |
| B.使用萃取的方法可提纯粗苯甲酸 |
| C.欲区分苯和甲苯,分别取少量样品价足量KMnO4溶液,振荡,KMnO4溶液褪色为甲苯,反之为苯 |
| D.欲确定溴乙烷中含有溴原子,加入适量NaOH溶液后加热,待溶液冷却后滴加AgNO3溶液,若生成淡黄色沉淀即可确定 |

| A.充电时,a为阴极 |
| B.充电时,溶液中Li+从b向a迁移 |
| C.电池放电时负极反应为Li-e-=Li+ |
| D.利用该电池电解水,消耗锂14 g可生成气体33.6 L |
| A.c(Na+)>c(CO32-)>c(HCO3-)>c(H2CO3) |
| B.c(Na+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)] |
| C.c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) |
| D.c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
【知识点】 弱电解质的电离
| 物质 | H2CO3 | HClO | HAlO2 |
| 电离常数 (25℃) | Ka1=4.4×10-7 | Ka=3×10-8 | Ka=6.3×10-13 |
| Ka2=4.7×10-11 |
| A.NaClO溶液中通入过量CO2:ClO-+CO2+H2O=HClO+HCO3- |
| B.NaClO溶液中通入少量CO2:2ClO-+CO2+H2O=2HClO+CO32- |
| C.NaAlO2溶液中加入过量CO2:AlO2-+CO2+2H2O=HCO3-+Al(OH)3↓ |
| D.NaAlO2溶液中通入少量CO2:2AlO2-+CO2+3H2O=CO32-+2Al(OH)3↓ |
【知识点】 水的电离及溶液的酸碱性
四、填空题 添加题型下试题
(1)用离子方程式表示盐碱地(含较多Na2CO3)呈碱性的原因:
(2)常温时,AlCl3溶液呈
【知识点】 离子反应的发生及书写

(1)电源A极是
(2)欲用丙装置给铜镀银。G应该是
(3)如用甲醇燃料电池(如图)充当电源,写出负极的电极反应方程式:
【知识点】 电解池
(1)有pH均为2的a盐酸、b醋酸两瓶溶液,与足量锌反应放出等体积H2所需时间的长短顺序是a
(2)已知:25℃时水的离子积为1×10-14。试回答:
①取pH=5的H2SO4溶液1 mL加水稀释至1000 mL后溶液中c(H+)∶c(SO42-)=
②将体积为Va、pH=13的NaOH溶液与体积为Vb、pH=1的H2SO4溶液混合:
若所得混合液为中性,则Va∶Vb=
若所得混合液pH=2,则Va∶Vb=
【知识点】 水的电离及溶液的酸碱性

已知:298 K时各离子开始沉淀及完全沉淀时的pH如下表所示。
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.34 | 9.7 |
| Fe3+ | 1.48 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
请回答下列问题:
(1)在H2SO4作用下矿石中含有的ZnS溶解而CuS不溶,这是由于相同温度下:Ksp(CuS)
(2)除铁过程中试剂甲最好选用
A.KMnO4 B.H2O2 C.HNO3 D.Cl2
(3)除铁过程中加入氨水的目的是调节pH在
(4)试写出沉淀Zn2+时发生反应的离子方程式:
【知识点】 水的电离及溶液的酸碱性
甲认为:HCO3-的水解程度随温度升高而增大,溶液碱性增强。
乙认为:温度升高造成NaHCO3受热生成Na2CO3,溶液碱性增强。
丙同学认为甲、乙的判断都不充分,提出以下方案补充实验:
(1)在50℃的NaHCO3饱和溶液中加入足量的试剂
| A.CaCl2溶液 | B.Ba(OH)2溶液 | C.NaOH溶液 | D.澄清石灰水 |
(2)将加热后的NaHCO3饱和溶液冷却到20℃,若溶液的pH
(3)查阅资料,发现NaHCO3的分解温度为150℃,丙断言
【知识点】 水的电离及溶液的酸碱性
五、解答题 添加题型下试题
(1)滴定时应选用
(2)下列操作会导致烧碱样品中NaOH含量测定值偏高的是
| A.锥形瓶未用待测液润洗 |
| B.酸式滴定管未用标准液润洗 |
| C.在滴定前有气泡,滴定后气泡消失 |
| D.滴定前平视读数,滴定结束俯视读数 |
F.指示剂变色后立即读数
(3)实验相关数据记录如下:
| 实验编号 | V(烧碱溶液)/mL | V(HCl)/mL | |
| 初读数 | 末读数 | ||
| 1 | 20.00 | 0.60 | 20.62 |
| 2 | 20.00 | 0.80 | 20.78 |
| 3 | 20.00 | 0.20 | 20.90 |
依据表中数据,计算样品中NaOH的质量分数
【知识点】 仪器使用与实验安全
六、填空题 添加题型下试题

(1)反应③、⑥的反应类型分别是
(2)有机物C按照系统命名,其名称是:
(3)写出反应⑧的化学方程式为
(4)环己烷的一种同分异构体W,已知W分子中所有碳原子均在同一平面上,写出其结构简式
【知识点】 有机物的命名
七、计算题 添加题型下试题
(1)通过计算确定A的分子式;
(2)A分子的核磁共振氢谱如图,红外光谱显示分子中氧原子只以羟基形式存在,试写出其结构简式。

【知识点】 有机物的结构特点
试卷分析
试卷题型(共 30题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.64 | 金属的电化学腐蚀与防护 | |
| 2 | 0.64 | 电解池 | |
| 3 | 0.64 | 化学用语 | |
| 4 | 0.64 | 仪器使用与实验安全 | |
| 5 | 0.94 | 电解池 | |
| 6 | 0.64 | 烃 | |
| 7 | 0.65 | 弱电解质的电离方程式 水解的离子方程式书写 | |
| 8 | 0.64 | 水的电离及溶液的酸碱性 | |
| 9 | 0.64 | 电解池 | |
| 10 | 0.85 | 单烯烃的加成反应 炔烃的加成 | |
| 11 | 0.65 | 常见金属的活动性顺序及其应用 利用原电池原理比较金属活动性强弱 电解原理的应用 | |
| 12 | 0.64 | 烃 | |
| 13 | 0.94 | 一元强酸与一元弱酸的比较 | |
| 14 | 0.94 | 有机物的结构特点 | |
| 16 | 0.64 | 盐类的水解 | |
| 17 | 0.65 | 弱电解质的电离平衡 难溶电解质的溶解平衡 | |
| 18 | 0.4 | 烃 | |
| 19 | 0.4 | 化学实验基础 卤代烃 | |
| 20 | 0.65 | 其他二次电池 | |
| 21 | 0.85 | 弱电解质的电离 | |
| 22 | 0.94 | 水的电离及溶液的酸碱性 | |
| 二、未知 | |||
| 15 | 0.4 | 离子共存 | 未知 |
| 三、填空题 | |||
| 23 | 0.94 | 离子反应的发生及书写 | |
| 24 | 0.85 | 电解池 | |
| 25 | 0.85 | 水的电离及溶液的酸碱性 | |
| 26 | 0.64 | 水的电离及溶液的酸碱性 | |
| 27 | 0.85 | 水的电离及溶液的酸碱性 | |
| 29 | 0.94 | 有机物的命名 | |
| 四、解答题 | |||
| 28 | 0.94 | 仪器使用与实验安全 | 实验探究题 |
| 五、计算题 | |||
| 30 | 0.85 | 有机物的结构特点 | |









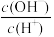 =106的溶液:Al3+、NH4+、Cl-、S2-
=106的溶液:Al3+、NH4+、Cl-、S2-

