名校
1 . 6.5g的锌与100mL稀盐酸完全反应。计算:
(1)参加反应的锌的物质的量______ ;
(2)生成氢气的体积(标准状况)______ 。
(1)参加反应的锌的物质的量
(2)生成氢气的体积(标准状况)
您最近一年使用:0次
名校
解题方法
2 . 实验室欲用铁粉与稀硫酸反应制取标准状况下的氢气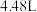 ,计算生成硫酸亚铁的物质的量是多少,至少需要铁粉的质量是多少
,计算生成硫酸亚铁的物质的量是多少,至少需要铁粉的质量是多少___________ 。(按步骤写出计算过程)
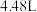 ,计算生成硫酸亚铁的物质的量是多少,至少需要铁粉的质量是多少
,计算生成硫酸亚铁的物质的量是多少,至少需要铁粉的质量是多少
您最近一年使用:0次
3 . 氯的几种同位素的质量数和相对丰度如下,氯元素的近似相对原子质量为___________ (列式并计算保留三位小数)。
| 核素符号 | 相对原子质量 | 丰度(%) |
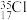 | 34.969 | 75.77 |
 | 36.966 | 24.23 |
您最近一年使用:0次
名校
解题方法
4 . 阅读下面文字材料。化学家在研究中发现,参加反应的微粒质量很小,但实际参加反应的微粒数目往往很大。为了将一定数目的微观粒子与可称量的宏观物质之间联系起来,在化学上特引入“物质的量”这个物理量。“物质的量(符号为n)”是国际单位制中的基本物理量之一,单位为“摩(符号为mol)”。1mol某种微粒集合体中含有 个微粒;单位物质的量的物质具有的质量称为该物质的摩尔质量(符号为M),单位为g/mol”,当物质的质量以g为单位时,摩尔质量的数值等于该物质的相对原子质量或相对分子质量;1mol任何气体在0℃、101kPa(称为标准状况)下所占的体积约为22.4L。以上物理量之间的关系为:
个微粒;单位物质的量的物质具有的质量称为该物质的摩尔质量(符号为M),单位为g/mol”,当物质的质量以g为单位时,摩尔质量的数值等于该物质的相对原子质量或相对分子质量;1mol任何气体在0℃、101kPa(称为标准状况)下所占的体积约为22.4L。以上物理量之间的关系为: 。请回答以下问题:
。请回答以下问题:
(1)9g水的物质的量为___________ mol,含有___________ 个水分子。
(2)2.2g二氧化碳含有___________ 个 分子,在标准状况下的体积为
分子,在标准状况下的体积为___________ L。
(3)14.2g 晶体中含有
晶体中含有___________ 个Na离子、___________ 个 离子。
离子。
 个微粒;单位物质的量的物质具有的质量称为该物质的摩尔质量(符号为M),单位为g/mol”,当物质的质量以g为单位时,摩尔质量的数值等于该物质的相对原子质量或相对分子质量;1mol任何气体在0℃、101kPa(称为标准状况)下所占的体积约为22.4L。以上物理量之间的关系为:
个微粒;单位物质的量的物质具有的质量称为该物质的摩尔质量(符号为M),单位为g/mol”,当物质的质量以g为单位时,摩尔质量的数值等于该物质的相对原子质量或相对分子质量;1mol任何气体在0℃、101kPa(称为标准状况)下所占的体积约为22.4L。以上物理量之间的关系为: 。请回答以下问题:
。请回答以下问题:(1)9g水的物质的量为
(2)2.2g二氧化碳含有
 分子,在标准状况下的体积为
分子,在标准状况下的体积为(3)14.2g
 晶体中含有
晶体中含有 离子。
离子。
您最近一年使用:0次
解题方法
5 . 从1L NaOH溶液取出100mL,若将取出的这100mL NaOH溶液加水稀释至500mL,所得溶液中溶质的物质的量浓度是
NaOH溶液取出100mL,若将取出的这100mL NaOH溶液加水稀释至500mL,所得溶液中溶质的物质的量浓度是______  ?含NaOH的质量
?含NaOH的质量______ 克?
 NaOH溶液取出100mL,若将取出的这100mL NaOH溶液加水稀释至500mL,所得溶液中溶质的物质的量浓度是
NaOH溶液取出100mL,若将取出的这100mL NaOH溶液加水稀释至500mL,所得溶液中溶质的物质的量浓度是 ?含NaOH的质量
?含NaOH的质量
您最近一年使用:0次
解题方法
6 . 计算题本题要求写计算过程。
(1)计算出 的物质的量为
的物质的量为___________ 。
(2)配置 溶液,需要NaOH是多少?
溶液,需要NaOH是多少?___________
(1)计算出
 的物质的量为
的物质的量为(2)配置
 溶液,需要NaOH是多少?
溶液,需要NaOH是多少?
您最近一年使用:0次
名校
解题方法
7 . 硅元素存在三种天然稳定核素,相关数据如表:硅元素的近似相对原子质量为_______ 。
| 核素符号 | 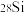 |  | 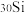 |
丰度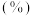 | 92.2 | 4.7 | 3.1 |
您最近一年使用:0次
解题方法
8 . 0.16gNaOH恰好与20mL的盐酸完全反应,求盐酸中 的物质的量浓度
的物质的量浓度________ 。
 的物质的量浓度
的物质的量浓度
您最近一年使用:0次
解题方法
9 . 为测定某种铝镁合金中铝的质量分数,探究小组进行了实验:称取质量为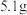 的合金,加入的稀盐酸,恰好完全反应,并产生了
的合金,加入的稀盐酸,恰好完全反应,并产生了 的氢气。计算铝镁合金中铝的质量分数是多少
的氢气。计算铝镁合金中铝的质量分数是多少_____ 。
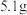 的合金,加入的稀盐酸,恰好完全反应,并产生了
的合金,加入的稀盐酸,恰好完全反应,并产生了 的氢气。计算铝镁合金中铝的质量分数是多少
的氢气。计算铝镁合金中铝的质量分数是多少
您最近一年使用:0次
名校
10 . 稀硫酸与铝恰好完全反应,所得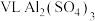 溶液中含有
溶液中含有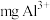 ,则该浴液中
,则该浴液中 物质的量浓度为
物质的量浓度为_______  。
。
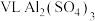 溶液中含有
溶液中含有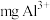 ,则该浴液中
,则该浴液中 物质的量浓度为
物质的量浓度为 。
。
您最近一年使用:0次



