名校
解题方法
1 . 25℃时,在等体积的①pH=0的H2SO4溶液、②0.05mol/L的Ba(OH)2溶液、③pH=10的Na2S溶液、④pH=5的NH4NO3溶液中,发生电离的水的物质的量之比是___________ 。
您最近一年使用:0次
名校
解题方法
2 . 硼元素有两种同位素: (相对原子质量10.0129,丰度19.78%)和
(相对原子质量10.0129,丰度19.78%)和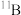 (相对原子质量11.00931,丰度80.22%)。请列式计算硼元素的相对原子质量(计算结果保留至小数点后两位)
(相对原子质量11.00931,丰度80.22%)。请列式计算硼元素的相对原子质量(计算结果保留至小数点后两位)___________ 。
 (相对原子质量10.0129,丰度19.78%)和
(相对原子质量10.0129,丰度19.78%)和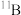 (相对原子质量11.00931,丰度80.22%)。请列式计算硼元素的相对原子质量(计算结果保留至小数点后两位)
(相对原子质量11.00931,丰度80.22%)。请列式计算硼元素的相对原子质量(计算结果保留至小数点后两位)
您最近一年使用:0次
解题方法
3 . 铜与浓硫酸在加热条件下反应生成CuSO4、SO2和H2O,现将6.4g铜与足量的浓硫酸充分反应,铜完全溶解,反应后将溶液稀释至100mL。请计算:
(1)铜的物质的量为_______ mol。
(2)反应生成的SO2的体积(标准状况下)为_______ L。
(3)稀释后溶液中硫酸铜的物质的量浓度_______ 。
(1)铜的物质的量为
(2)反应生成的SO2的体积(标准状况下)为
(3)稀释后溶液中硫酸铜的物质的量浓度
您最近一年使用:0次
解题方法
4 . 某些化学键的键能(kJ·mol-1)如下表:
(1)1 mol H2在2 mol Cl2中燃烧,生成2 mol HCl放出的热量为_______ kJ。
(2)在一定条件下,1 mol H2分别与足量的Cl2、Br2、I2完全反应,放出热量由多到少的顺序是_______ 。
| 键 | H—H | Br—Br | I—I | Cl—Cl | H—Cl | H—I | H—Br |
| 键能 | 436 | 193 | 151 | 247 | 431 | 299 | 366 |
(2)在一定条件下,1 mol H2分别与足量的Cl2、Br2、I2完全反应,放出热量由多到少的顺序是
您最近一年使用:0次
解题方法
5 . 室温下,测得某溶液中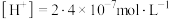 ,则
,则 的物质的量浓度为
的物质的量浓度为_______ ,该溶液的 为
为_______ ,该溶液的 为
为_______ 。
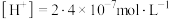 ,则
,则 的物质的量浓度为
的物质的量浓度为 为
为 为
为
您最近一年使用:0次
名校
解题方法
6 . 完成下列反应的热化学方程式。
(1)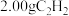 气体完全燃烧生成液态水和
气体完全燃烧生成液态水和 气体,放出
气体,放出 的热量,写出该反应的热化学方程式
的热量,写出该反应的热化学方程式_______
(2)室温下,充分燃烧一定量的丁烷放出的热量为Q,生成的 恰好与
恰好与 浓度为
浓度为 的
的 溶液完全反应生成正盐,写出表示丁烷燃烧热的热化学方程式
溶液完全反应生成正盐,写出表示丁烷燃烧热的热化学方程式_______
(3)已知: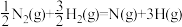


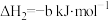

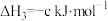
写出 和
和 反应生成液氨的热化学方程式
反应生成液氨的热化学方程式_______ 。
(4)已知:①

②
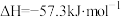
试写出 电离的热化学方程式
电离的热化学方程式_______ 。
(5)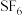 是一种优良的绝缘气体,分子结构中,只存在S-F键,已知
是一种优良的绝缘气体,分子结构中,只存在S-F键,已知 转化为气态硫原子吸收能量
转化为气态硫原子吸收能量 ,F-F键能为
,F-F键能为 ,S-F键能为
,S-F键能为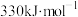 ,试写出
,试写出 和
和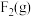 反应生成
反应生成 的热化学方程式
的热化学方程式_______ 。
(1)
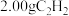 气体完全燃烧生成液态水和
气体完全燃烧生成液态水和 气体,放出
气体,放出 的热量,写出该反应的热化学方程式
的热量,写出该反应的热化学方程式(2)室温下,充分燃烧一定量的丁烷放出的热量为Q,生成的
 恰好与
恰好与 浓度为
浓度为 的
的 溶液完全反应生成正盐,写出表示丁烷燃烧热的热化学方程式
溶液完全反应生成正盐,写出表示丁烷燃烧热的热化学方程式(3)已知:
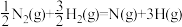


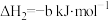

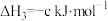
写出
 和
和 反应生成液氨的热化学方程式
反应生成液氨的热化学方程式(4)已知:①


②

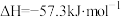
试写出
 电离的热化学方程式
电离的热化学方程式(5)
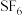 是一种优良的绝缘气体,分子结构中,只存在S-F键,已知
是一种优良的绝缘气体,分子结构中,只存在S-F键,已知 转化为气态硫原子吸收能量
转化为气态硫原子吸收能量 ,F-F键能为
,F-F键能为 ,S-F键能为
,S-F键能为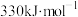 ,试写出
,试写出 和
和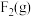 反应生成
反应生成 的热化学方程式
的热化学方程式
您最近一年使用:0次
解题方法
7 . 取含26.1gMnO2的软锰矿石跟200mL10mol/L的浓盐酸反应完全,已知:MnO2+4HCl(浓)→MnCl2+Cl2↑+2H2O。计算:
(1)生成的氯气在标准状况的体积为多少升___ ?
(2)在反应中被消耗的HCl的质量为多少克___ ?
(3)在反应后的溶液中加入足量的硝酸银溶液,试计算产生沉淀的质量___ ?(不考虑氯化氢的挥发)。
(1)生成的氯气在标准状况的体积为多少升
(2)在反应中被消耗的HCl的质量为多少克
(3)在反应后的溶液中加入足量的硝酸银溶液,试计算产生沉淀的质量
您最近一年使用:0次
8 . 液态肼(N2H4)和液态双氧水可作为火箭推进剂的原料,它们混合时发生反应,生成N2和水蒸气,并放出大量的热。已知1 g液态肼完全反应生成气态水放出的热量为20 kJ。
(1)H2O(l)=H2O(g) ΔH=+44 kJ·mol-1,写出液态肼与液态双氧水反应生成N2和液态水的热化学方程式:___________ 。
(2)以N2和H2为原料通过一定途径可制得N2H4,已知断裂1 mol N—N键、N≡N键、N—H键、H—H键所需的能量分别为193 kJ·mol-1、946 kJ·mol-1、390.8 kJ·mol-1、436 kJ·mol-1,试写出由N2、H2合成气态肼(N2H4)的热化学方程式为___________ 。
(3)温度在150 ℃以上时,H2O2便迅速分解为H2O和O2,发射火箭时用过氧化氢作强氧化剂就是利用这个原理。
已知:
①H2(g)+O2(g)=H2O2(l) ΔH1=-134.3 kJ·mol-1;
②H2O(l)=H2(g)+ O2(g) ΔH2=+286 kJ·mol-1。
O2(g) ΔH2=+286 kJ·mol-1。
则反应③H2O2(l)=H2O(l)+ O2(g)的ΔH=
O2(g)的ΔH=___________ 。
(1)H2O(l)=H2O(g) ΔH=+44 kJ·mol-1,写出液态肼与液态双氧水反应生成N2和液态水的热化学方程式:
(2)以N2和H2为原料通过一定途径可制得N2H4,已知断裂1 mol N—N键、N≡N键、N—H键、H—H键所需的能量分别为193 kJ·mol-1、946 kJ·mol-1、390.8 kJ·mol-1、436 kJ·mol-1,试写出由N2、H2合成气态肼(N2H4)的热化学方程式为
(3)温度在150 ℃以上时,H2O2便迅速分解为H2O和O2,发射火箭时用过氧化氢作强氧化剂就是利用这个原理。
已知:
①H2(g)+O2(g)=H2O2(l) ΔH1=-134.3 kJ·mol-1;
②H2O(l)=H2(g)+
 O2(g) ΔH2=+286 kJ·mol-1。
O2(g) ΔH2=+286 kJ·mol-1。则反应③H2O2(l)=H2O(l)+
 O2(g)的ΔH=
O2(g)的ΔH=
您最近一年使用:0次
解题方法
9 . 在容积为1.00L的密闭容器中,通入一定量的N2O4,发生反应:N2O4(g) 2NO2(g)。100℃时,各物质浓度随时间变化如图所示。
2NO2(g)。100℃时,各物质浓度随时间变化如图所示。
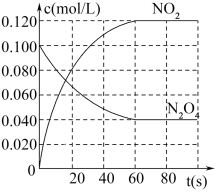
请回答:
(1)60s内,v(N2O4)=___ mol/(L•s)。
(2)若升高温度,混合气体的颜色变深,则正反应是___ (填“放热”或吸热”)反应。
(3)100℃时,该反应的化学平衡常数数值为___ 。
(4)平衡时,N2O4的转化率是___ 。
 2NO2(g)。100℃时,各物质浓度随时间变化如图所示。
2NO2(g)。100℃时,各物质浓度随时间变化如图所示。
请回答:
(1)60s内,v(N2O4)=
(2)若升高温度,混合气体的颜色变深,则正反应是
(3)100℃时,该反应的化学平衡常数数值为
(4)平衡时,N2O4的转化率是
您最近一年使用:0次
2022-09-18更新
|
483次组卷
|
3卷引用:甘肃省镇原县第二中学2021-2022学年高二上学期期中考试化学试题
10 . 标准状况时,33.6LNH3约含有____ 个氨分子,质量是____ g,全部溶于水后配成1L溶液,所得溶液的物质的量浓度为____ mol/L。
您最近一年使用:0次
2022-09-18更新
|
203次组卷
|
2卷引用:甘肃省镇原县第二中学2021-2022学年高二上学期期中考试化学试题



