名校
解题方法
1 . 锌在工业中有重要作用,也是人体必需的微量元素。请回答:
(1)基态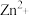 的价层电子排布式
的价层电子排布式_______ , 中阴离子空间结构为
中阴离子空间结构为_______ 。
(2)下列说法正确的是_______。
(3)已知: 和
和 的熔点数据如下表:
的熔点数据如下表:
 熔点明显高于
熔点明显高于 ,原因是
,原因是_______ 。
(4)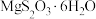 的晶胞形状为长方体,边长分别为anm、bnm、cnm,结构如图所示。
的晶胞形状为长方体,边长分别为anm、bnm、cnm,结构如图所示。 个数为
个数为_______ 。已知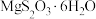 的摩尔质量是
的摩尔质量是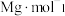 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,该晶体的密度为
,该晶体的密度为_______  。(
。(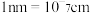 )
)
(1)基态
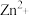 的价层电子排布式
的价层电子排布式 中阴离子空间结构为
中阴离子空间结构为(2)下列说法正确的是_______。
A.电负性: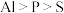 | B.离子半径: |
| C.Fe位于元素周期表的第四周期第Ⅷ族 | D.Cr在元素周期表中处于d区 |
(3)已知:
 和
和 的熔点数据如下表:
的熔点数据如下表:| 物质 | 熔点/℃ |
 | 800.7 |
 |  |
 熔点明显高于
熔点明显高于 ,原因是
,原因是(4)
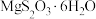 的晶胞形状为长方体,边长分别为anm、bnm、cnm,结构如图所示。
的晶胞形状为长方体,边长分别为anm、bnm、cnm,结构如图所示。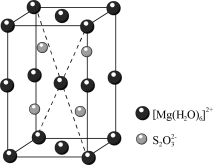
 个数为
个数为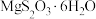 的摩尔质量是
的摩尔质量是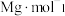 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,该晶体的密度为
,该晶体的密度为 。(
。(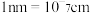 )
)
您最近一年使用:0次
名校
解题方法
2 . 很多重要的工业原料来源于石油化工,结合下图回答有关问题:______ 。
(2)丙烯酸中碳原子杂化方式为______ ,含氧官能团的名称为______ 。
(3)写出下列反应的反应类型:②______ 、③______
(4)B、C的沸点大小关系:B______ C(填>、=或<),原因是____________ 。
(5)写出下列反应的化学方程式:
丙烯酸+B→丙烯酸乙酯:__________________ 。
反应④:__________________ 。
(6)H与C互为同系物,且H比C多2个 ,H共有
,H共有______ 种结构(不考虑立体异构)。
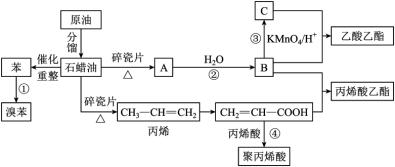
(2)丙烯酸中碳原子杂化方式为
(3)写出下列反应的反应类型:②
(4)B、C的沸点大小关系:B
(5)写出下列反应的化学方程式:
丙烯酸+B→丙烯酸乙酯:
反应④:
(6)H与C互为同系物,且H比C多2个
 ,H共有
,H共有
您最近一年使用:0次
3 . 某烃A是一种植物生长调节剂,A可发生如图所示的一系列化学反应,根据图像回答下列问题:_____ ;B_____ ;C_____ ;D_____ 。
(2)写出③⑤反应类型:③_____ ;⑤_____ 。
(3)②、④两步反应的化学方程式:②_____ 。④_____ 。

(2)写出③⑤反应类型:③
(3)②、④两步反应的化学方程式:②
您最近一年使用:0次
解题方法
4 . 回答下列问题。
(1)一定条件下,在 密闭容器中充入
密闭容器中充入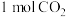 和
和 ,发生反应:
,发生反应: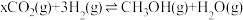 。测得
。测得 和
和 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。
___________ ; 内
内 的平均反应速率
的平均反应速率
___________ 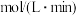 ,平衡时
,平衡时 的转化率为
的转化率为___________ 。
(2)下列措施能提高正反应速率的是___________(填正确答案的字母)。
(3)工业上常以水煤气( 和
和 )为原料合成甲醇。已知:
)为原料合成甲醇。已知: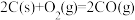
 ;
;
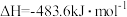 ,则
,则 与
与 制备水煤气的热化学方程式为
制备水煤气的热化学方程式为___________ 。
(1)一定条件下,在
 密闭容器中充入
密闭容器中充入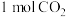 和
和 ,发生反应:
,发生反应: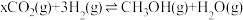 。测得
。测得 和
和 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。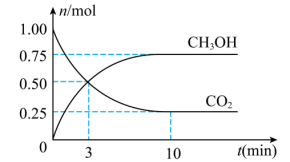

 内
内 的平均反应速率
的平均反应速率
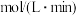 ,平衡时
,平衡时 的转化率为
的转化率为(2)下列措施能提高正反应速率的是___________(填正确答案的字母)。
| A.降低温度 | B.增加 的量 的量 | C.使用催化剂 | D.及时分离出甲醇 |
 和
和 )为原料合成甲醇。已知:
)为原料合成甲醇。已知: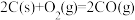
 ;
;
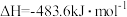 ,则
,则 与
与 制备水煤气的热化学方程式为
制备水煤气的热化学方程式为
您最近一年使用:0次
解题方法
5 . 以铁、硫酸、柠檬酸、双氧水、氨水等为原料可制备柠檬酸铁铵[(NH4)3Fe(C6H5O7)2]。
(1)Fe基态核外电子排布式为___________ ;[Fe(H2O)6]2+中与Fe2+配位原子是___________ (填元素符号)。
(2)NH3分子中氮原子的杂化轨道类型为___________ ,分子空间构型为___________ ;NH3分子H—N—H键角比PH3分子中的H—P—H键角大,请解释其原因___________
(3)与NH 互为等电子体的一种分子为
互为等电子体的一种分子为___________ (填化学式)。
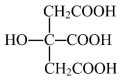
(4)柠檬酸的结构简式如图。1 mol 柠檬酸分子中碳原子与氧形成的σ键的数目为___________ mol,π键的数目为___________ mol。
(1)Fe基态核外电子排布式为
(2)NH3分子中氮原子的杂化轨道类型为
(3)与NH
 互为等电子体的一种分子为
互为等电子体的一种分子为(4)柠檬酸的结构简式如图。1 mol 柠檬酸分子中碳原子与氧形成的σ键的数目为

您最近一年使用:0次
6 . “金相玉振”学习小组设计如图实验装置(部分夹持装置已略去)制取氯酸钾并进行氯气性质探究实验。
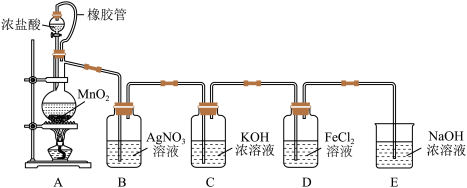
请回答:
(1)装置A中制取 的离子反应方程式是
的离子反应方程式是______ 。
(2)装置B中溶液变浑浊,______ (填“能”或“不能”)说明 与
与 溶液发生反应生成
溶液发生反应生成 ,理由是
,理由是______ 。
(3)装置C中制取氯酸钾的化学方程式为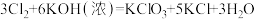 ,该反应中氧化剂与还原剂的物质的量之比是
,该反应中氧化剂与还原剂的物质的量之比是______ 。
(4)装置D中导管接错,若导致溶液进入装置E,则E中出现的现象是______ 。
(5)装置D改为“长管进短管出”后,装置E中仍然存在的一处明显错误是______ 。

请回答:
(1)装置A中制取
 的离子反应方程式是
的离子反应方程式是(2)装置B中溶液变浑浊,
 与
与 溶液发生反应生成
溶液发生反应生成 ,理由是
,理由是(3)装置C中制取氯酸钾的化学方程式为
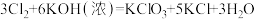 ,该反应中氧化剂与还原剂的物质的量之比是
,该反应中氧化剂与还原剂的物质的量之比是(4)装置D中导管接错,若导致溶液进入装置E,则E中出现的现象是
(5)装置D改为“长管进短管出”后,装置E中仍然存在的一处明显错误是
您最近一年使用:0次
7 . 完成下列填空:
(1) 水解的离子方程式为
水解的离子方程式为_______ ,在配制硫化钠溶液时可以加入少量的_______ (填化学式)以抑制其水解。
(2)硫酸铁水溶液呈_______ 性,原因是_______ 用离子方程式表示)。把 溶液蒸干灼烧,最后得到的主要固体产物是
溶液蒸干灼烧,最后得到的主要固体产物是_______ 。
(3)氢能是一种理想的绿色能源,有科学家预言,氢能有可能成为人类未来的主要能源。高纯氢的制备是目前的研究热点,包括氢的制备、储存和应用三个环节。
①适量 在
在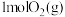 中完全燃烧,生成
中完全燃烧,生成 ,放出
,放出 的热量,请写出表示燃烧热的热化学方程式
的热量,请写出表示燃烧热的热化学方程式_______ 。
②与汽油相比,氢气作为燃料的有点是_______ 。
③下列反应均可获取 。
。
反应I:
反应II: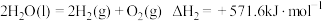
反应III: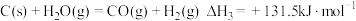
反应IV:
计算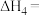
_______ 。
(1)
 水解的离子方程式为
水解的离子方程式为(2)硫酸铁水溶液呈
 溶液蒸干灼烧,最后得到的主要固体产物是
溶液蒸干灼烧,最后得到的主要固体产物是(3)氢能是一种理想的绿色能源,有科学家预言,氢能有可能成为人类未来的主要能源。高纯氢的制备是目前的研究热点,包括氢的制备、储存和应用三个环节。
①适量
 在
在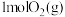 中完全燃烧,生成
中完全燃烧,生成 ,放出
,放出 的热量,请写出表示燃烧热的热化学方程式
的热量,请写出表示燃烧热的热化学方程式②与汽油相比,氢气作为燃料的有点是
③下列反应均可获取
 。
。反应I:

反应II:
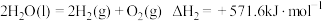
反应III:
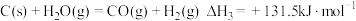
反应IV:

计算
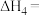
您最近一年使用:0次
解题方法
8 . 金属及塑料制品表面镀铬不仅美观还可提高金属制品抗腐蚀性能,电镀废水中六价铬具有高毒性,必须经处理后才能排放。
(1)常见镀铬液由重铬酸(H2Cr2O7)和催化剂硫酸组成。
①镀铬液在水溶液中存在如下平衡:Cr2O +H2O
+H2O 2 CrO
2 CrO +2H+该反应平衡常数表达式为K=
+2H+该反应平衡常数表达式为K=______ 。
②镀铬时由CrO 放电产生铬镀层。阴极的电极反应式为
放电产生铬镀层。阴极的电极反应式为_______ 。
(2)电解法处理含六价铬(Cr2O 和CrO
和CrO )的强酸性废水,其原理如下图所示。
)的强酸性废水,其原理如下图所示。

①电解一段时间后随着溶液pH的升高,便有Fe(OH)3和Cr(OH)3沉淀生成。图中A为电源_______ 极(选填:“正”或“负”);
②阴极产生的气体为_______ (写化学式)。
(1)常见镀铬液由重铬酸(H2Cr2O7)和催化剂硫酸组成。
①镀铬液在水溶液中存在如下平衡:Cr2O
 +H2O
+H2O 2 CrO
2 CrO +2H+该反应平衡常数表达式为K=
+2H+该反应平衡常数表达式为K=②镀铬时由CrO
 放电产生铬镀层。阴极的电极反应式为
放电产生铬镀层。阴极的电极反应式为(2)电解法处理含六价铬(Cr2O
 和CrO
和CrO )的强酸性废水,其原理如下图所示。
)的强酸性废水,其原理如下图所示。
①电解一段时间后随着溶液pH的升高,便有Fe(OH)3和Cr(OH)3沉淀生成。图中A为电源
②阴极产生的气体为
您最近一年使用:0次
9 . 绿矾 可作补血剂,其结构如图所示:
可作补血剂,其结构如图所示:
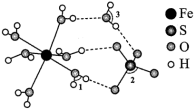
由成键一方单独提供孤电子对给予另外一方,这类“电子对给予—接受”化学键称为配位键。
(1)按照核外电子排布,可把元素周期表划分成五个区,铁元素位于元素周期表的_______ 区。
(2)基态S原子核外电子空间运动状态有___________ 种,电子占据最高能级的电子云轮廓图形状为___________ 。
(3) 中
中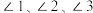 由大到小的顺序是
由大到小的顺序是___________ 。
(4)二价铁易被氧化为三价铁,结合价层电子排布式解释原因:___________ 。
 可作补血剂,其结构如图所示:
可作补血剂,其结构如图所示:
由成键一方单独提供孤电子对给予另外一方,这类“电子对给予—接受”化学键称为配位键。
(1)按照核外电子排布,可把元素周期表划分成五个区,铁元素位于元素周期表的
(2)基态S原子核外电子空间运动状态有
(3)
 中
中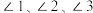 由大到小的顺序是
由大到小的顺序是(4)二价铁易被氧化为三价铁,结合价层电子排布式解释原因:
您最近一年使用:0次
名校
解题方法
10 . 化合物E(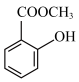 )常用作饮料、牙膏、化妆品的香料,也用作制取止痛药、杀虫剂等,可用以下路线合成:
)常用作饮料、牙膏、化妆品的香料,也用作制取止痛药、杀虫剂等,可用以下路线合成:
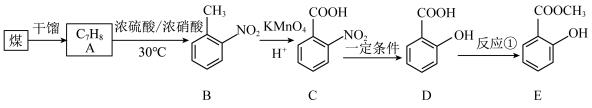
(1)煤的干馏是___________ (填“物理变化”或“化学变化”)。
(2)有机物A的名称是___________ ,有机物B的分子式为___________ 。
(3)①有机物C中所含的官能团名称是___________ 、___________ 、
②反应①的反应类型为___________ 。
③有机物M是E的同分异构体,其苯环上的取代基与E相同,则M的结构简式可能为___________ 、___________ 。(写出两种即可)
 )常用作饮料、牙膏、化妆品的香料,也用作制取止痛药、杀虫剂等,可用以下路线合成:
)常用作饮料、牙膏、化妆品的香料,也用作制取止痛药、杀虫剂等,可用以下路线合成:
(1)煤的干馏是
(2)有机物A的名称是
(3)①有机物C中所含的官能团名称是
②反应①的反应类型为
③有机物M是E的同分异构体,其苯环上的取代基与E相同,则M的结构简式可能为
您最近一年使用:0次



