解题方法
1 . Fe/Fe3O4复合物是一种高密度磁记录材料,磁记录材料有记录和存储信息的功能。制备该材料的一种流程如下:
Ⅰ、相关反应原理:
①Fe2++2OH-=Fe(OH)2
②3Fe(OH)2=Fe+2Fe(OH)3
③Fe(OH)2+2Fe(OH)3=Fe3O4+4H2O
Ⅱ、25℃时Fe(OH)2的Ksp=8.0×10-16
1.用FeCl2溶液和KOH溶液制备Fe/Fe3O4反应的离子方程式为_____ 。该“反应”中通入氩气的原因_____ 。
2.取少量反应后溶液于试管中,选择试剂_____,可证明FeCl2溶液已反应完全。
3.已知参加反应的FeCl2溶液浓度为lmol·L−1。由题给信息分析,25℃时,当pH<2时,Fe/Fe3O4产率极低的原因_____ 。
下图1为回流时间与Fe/Fe3O4产率的关系图,图2为回流1h所得产品的X射线衍射图。_____ 。
通过Fe3O4和FeO的热化学循环可以利用太阳能,其转化关系如图所示。
6.从绿色化学角度评价该循环过程(说一点)。_____

Ⅰ、相关反应原理:
①Fe2++2OH-=Fe(OH)2
②3Fe(OH)2=Fe+2Fe(OH)3
③Fe(OH)2+2Fe(OH)3=Fe3O4+4H2O
Ⅱ、25℃时Fe(OH)2的Ksp=8.0×10-16
1.用FeCl2溶液和KOH溶液制备Fe/Fe3O4反应的离子方程式为
2.取少量反应后溶液于试管中,选择试剂_____,可证明FeCl2溶液已反应完全。
| A.SO2 | B.铁粉 |
| C.KSCN溶液 | D.KSCN溶液新制氯水 |
下图1为回流时间与Fe/Fe3O4产率的关系图,图2为回流1h所得产品的X射线衍射图。

通过Fe3O4和FeO的热化学循环可以利用太阳能,其转化关系如图所示。
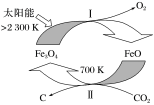
| A.反应物 | B.中间产物 | C.催化剂 | D.产物 |
您最近一年使用:0次
解题方法
2 . 氮及其化合物在生产、生活中广泛应用。
Ⅰ.氮元素化合价-物质类别关系图如图所示。

(1)图中A可以是__________ (写化学式)。写出一个能够生成B的化学方程式__________ 。
(2)实验室中,检验溶液中是否含有 的操作方法是
的操作方法是__________ 。
(3)水体中硝酸盐含量过高对环境不利,通过电催化法可以将水体中的硝酸盐进行合理转化。写出在中性介质中硝酸盐转化为氮气的阴极电极反应式__________ 。
Ⅱ.下图为实验室模拟尿素法制备水合肼( )的流程图:
)的流程图:
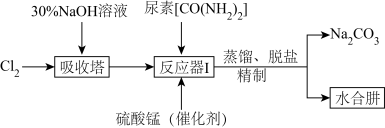
已知:① 易溶于水,具有强还原性,易被氧化成
易溶于水,具有强还原性,易被氧化成 。
。
②一定条件下,碱性NaClO溶液与尿素溶液反应生成 。
。
回答下列问题:
(4)“吸收塔”内发生反应的离子方程式为__________ 。
(5)写出“反应器Ⅰ”中生成水合肼反应的化学方程式为__________ 。
(6)“反应器Ⅰ”要控制NaClO溶液的用量,其主要目的是__________ 。
Ⅰ.氮元素化合价-物质类别关系图如图所示。

(1)图中A可以是
(2)实验室中,检验溶液中是否含有
 的操作方法是
的操作方法是(3)水体中硝酸盐含量过高对环境不利,通过电催化法可以将水体中的硝酸盐进行合理转化。写出在中性介质中硝酸盐转化为氮气的阴极电极反应式
Ⅱ.下图为实验室模拟尿素法制备水合肼(
 )的流程图:
)的流程图:
已知:①
 易溶于水,具有强还原性,易被氧化成
易溶于水,具有强还原性,易被氧化成 。
。②一定条件下,碱性NaClO溶液与尿素溶液反应生成
 。
。回答下列问题:
(4)“吸收塔”内发生反应的离子方程式为
(5)写出“反应器Ⅰ”中生成水合肼反应的化学方程式为
(6)“反应器Ⅰ”要控制NaClO溶液的用量,其主要目的是
您最近一年使用:0次
解题方法
3 .  俗称蓝矾、胆矾或铜矾,是颜料、电池、杀虫剂、木材防腐等方面的化工原料。其具有催吐,祛腐,解毒作用。
俗称蓝矾、胆矾或铜矾,是颜料、电池、杀虫剂、木材防腐等方面的化工原料。其具有催吐,祛腐,解毒作用。
I.实验室需配制 的
的 溶液.根据溶液配制情况,回答下面问题:
溶液.根据溶液配制情况,回答下面问题:
(1)用胆矾配制上述 溶液,需用托盘天平称量的质量为
溶液,需用托盘天平称量的质量为_______________ 。
(2)下列关于 容量瓶的操作,正确的是
容量瓶的操作,正确的是_______________ 。_____________ (填序号)。
a.配制前容量瓶底部有少量水 b.胆矾长期放置失去部分结晶水
c.定容时仰视刻度线 d.装瓶时有少量溶液溅出
(4)现利用上述 溶液配制
溶液配制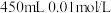 的
的 溶液,需用量筒量取
溶液,需用量筒量取________ 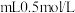 的
的 溶液。完成该实验,除用量筒,烧杯,玻璃棒之外,还需使用的玻璃仪器有
溶液。完成该实验,除用量筒,烧杯,玻璃棒之外,还需使用的玻璃仪器有___________ 。
Ⅱ.实验室有一瓶标签污损的硫酸铜溶液,为测定其浓度,研究小组设计了如下方案。
实验原理: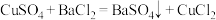
实验步骤: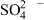 沉淀完全的方法为
沉淀完全的方法为_________ 。
(6)固体质量为wg,则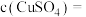
______  。
。
(7)若步骤①从烧杯中转移沉淀时未洗涤烧杯,则测得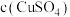
_______ (填“偏高”“偏低”或“无影响”)。
 俗称蓝矾、胆矾或铜矾,是颜料、电池、杀虫剂、木材防腐等方面的化工原料。其具有催吐,祛腐,解毒作用。
俗称蓝矾、胆矾或铜矾,是颜料、电池、杀虫剂、木材防腐等方面的化工原料。其具有催吐,祛腐,解毒作用。I.实验室需配制
 的
的 溶液.根据溶液配制情况,回答下面问题:
溶液.根据溶液配制情况,回答下面问题:(1)用胆矾配制上述
 溶液,需用托盘天平称量的质量为
溶液,需用托盘天平称量的质量为(2)下列关于
 容量瓶的操作,正确的是
容量瓶的操作,正确的是
a.配制前容量瓶底部有少量水 b.胆矾长期放置失去部分结晶水
c.定容时仰视刻度线 d.装瓶时有少量溶液溅出
(4)现利用上述
 溶液配制
溶液配制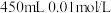 的
的 溶液,需用量筒量取
溶液,需用量筒量取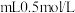 的
的 溶液。完成该实验,除用量筒,烧杯,玻璃棒之外,还需使用的玻璃仪器有
溶液。完成该实验,除用量筒,烧杯,玻璃棒之外,还需使用的玻璃仪器有Ⅱ.实验室有一瓶标签污损的硫酸铜溶液,为测定其浓度,研究小组设计了如下方案。
实验原理:
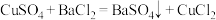
实验步骤:
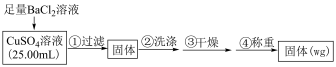
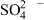 沉淀完全的方法为
沉淀完全的方法为(6)固体质量为wg,则
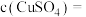
 。
。(7)若步骤①从烧杯中转移沉淀时未洗涤烧杯,则测得
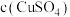
您最近一年使用:0次
名校
解题方法
4 . 化合物E(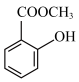 )常用作饮料、牙膏、化妆品的香料,也用作制取止痛药、杀虫剂等,可用以下路线合成:
)常用作饮料、牙膏、化妆品的香料,也用作制取止痛药、杀虫剂等,可用以下路线合成:
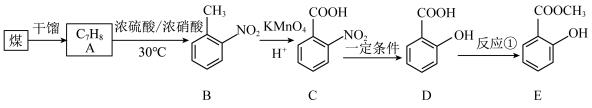
(1)煤的干馏是___________ (填“物理变化”或“化学变化”)。
(2)有机物A的名称是___________ ,有机物B的分子式为___________ 。
(3)①有机物C中所含的官能团名称是___________ 、___________ 、
②反应①的反应类型为___________ 。
③有机物M是E的同分异构体,其苯环上的取代基与E相同,则M的结构简式可能为___________ 、___________ 。(写出两种即可)
 )常用作饮料、牙膏、化妆品的香料,也用作制取止痛药、杀虫剂等,可用以下路线合成:
)常用作饮料、牙膏、化妆品的香料,也用作制取止痛药、杀虫剂等,可用以下路线合成:
(1)煤的干馏是
(2)有机物A的名称是
(3)①有机物C中所含的官能团名称是
②反应①的反应类型为
③有机物M是E的同分异构体,其苯环上的取代基与E相同,则M的结构简式可能为
您最近一年使用:0次
名校
解题方法
5 .  具有易液化、含氢密度高、应用广泛等优点,
具有易液化、含氢密度高、应用广泛等优点, 的合成及应用是科学研究的重要课题。
的合成及应用是科学研究的重要课题。
(1)以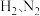 合成
合成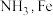 是常用的催化剂。
是常用的催化剂。
①基态 原子的电子排布式为
原子的电子排布式为___________ ,基态N原子轨道表示式___________ 。
②实际生产中采用铁的氧化物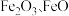 ,使用前用
,使用前用 和
和 的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:
的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:
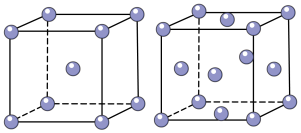
ⅰ.两种晶胞所含铁原子个数比为___________ 。
ⅱ.图1晶胞的棱长为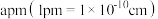 ,则其密度ρ=
,则其密度ρ=__________ g/cm3。
③我国科学家开发出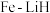 双中心催化剂,在合成
双中心催化剂,在合成 中显示出高催化活性。第一电离能
中显示出高催化活性。第一电离能 :
:
 ,从原子结构角度解释原因
,从原子结构角度解释原因___________ 。
(2)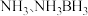 (氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
① 的中心原子的杂化轨道类型为
的中心原子的杂化轨道类型为___________ 。
② 存在配位键,提供空轨道的是
存在配位键,提供空轨道的是___________ 。其他含氮配合物,如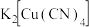 的配离子是
的配离子是___________ 、配合物 的配体是
的配体是___________ 。
(3)常温下 是橙黄色液体,其分子结构如图所示。
是橙黄色液体,其分子结构如图所示。
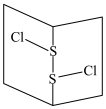
少量泄漏会产生窒息性气味,遇水易水解,并产生酸性悬浊液。
 分子中含有
分子中含有___________ 键(填“极性”、“非极性”,下同),是___________ 分子, 与
与 分子结构相似,熔沸点S2Br2
分子结构相似,熔沸点S2Br2______ S2Cl2(填“>”或“<”)。
 具有易液化、含氢密度高、应用广泛等优点,
具有易液化、含氢密度高、应用广泛等优点, 的合成及应用是科学研究的重要课题。
的合成及应用是科学研究的重要课题。(1)以
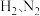 合成
合成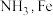 是常用的催化剂。
是常用的催化剂。①基态
 原子的电子排布式为
原子的电子排布式为②实际生产中采用铁的氧化物
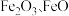 ,使用前用
,使用前用 和
和 的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:
的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:
ⅰ.两种晶胞所含铁原子个数比为
ⅱ.图1晶胞的棱长为
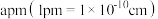 ,则其密度ρ=
,则其密度ρ=③我国科学家开发出
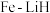 双中心催化剂,在合成
双中心催化剂,在合成 中显示出高催化活性。第一电离能
中显示出高催化活性。第一电离能 :
: ,从原子结构角度解释原因
,从原子结构角度解释原因(2)
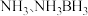 (氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。①
 的中心原子的杂化轨道类型为
的中心原子的杂化轨道类型为②
 存在配位键,提供空轨道的是
存在配位键,提供空轨道的是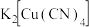 的配离子是
的配离子是 的配体是
的配体是(3)常温下
 是橙黄色液体,其分子结构如图所示。
是橙黄色液体,其分子结构如图所示。
少量泄漏会产生窒息性气味,遇水易水解,并产生酸性悬浊液。
 分子中含有
分子中含有 与
与 分子结构相似,熔沸点S2Br2
分子结构相似,熔沸点S2Br2
您最近一年使用:0次
6 . 实验装置,装置特点:固+液 气。
气。
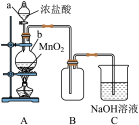
(1)仪器a的名称________ ,仪器b的名称________ 。
(2)Cl2的收集方法是________ 。
(3)烧杯中NaOH溶液的作用是________ 。
 气。
气。
(1)仪器a的名称
(2)Cl2的收集方法是
(3)烧杯中NaOH溶液的作用是
您最近一年使用:0次
7 . 由硅原子核形成的三种微粒,电子排布式分别为:①[Ne]3s23p2、②[Ne]3s23p1、③[Ne]3s23p14s1,有关这些微粒的叙述,正确的是_______ 。
| A.微粒半径:③>①>② |
| B.电子排布属于基态原子(或离子)的是:①② |
| C.电离一个电子所需最低能量:①>②>③ |
| D.得电子能力:①>② |
您最近一年使用:0次
8 . 小明在家清洗餐具时发现下水道堵塞,小明爸爸请来的家政师傅拿出几包白色粉状管道疏通剂(如图) ,取部分投入管道并倒入适量水,只见管道中的水上下翻滚,并产生大量泡沫,用工具在管道内搅动几下,管道即通。好奇的小明与化学兴趣小组同学利用剩余的管道疏通剂开展探究活动。
【查阅资料】该管道疏通剂中过碳酸钠的化学式为2Na2CO3·3H2O2,白色晶体,加入水中,剧烈反应并产生气体;香精只起除臭作用。
【理论推测】 兴趣小组的同学们根据所学知识和资料信息推测该气体为氧气。
【实验验证】 同学们选择下列实验装置开展验证实验。

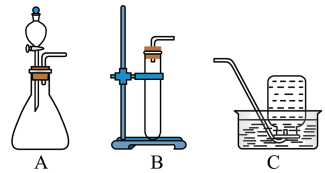
(1)疏通剂与水反应剧烈,你认为应选择_______ 作为发生装置( 选填“A”或“B”)。
(2)利用装置C收集一瓶气体,将带火星的木条伸入其中,现象为_______ ,证明小组同学的推测正确。
【深入探究】 为检验疏通剂与水反应后剩余溶液中溶质成分,兴趣小组开展了下表所示的探究实验。( 提示:氯化钙溶液呈中性)
(3)请完善下面的表格。
讨论与分析实验步骤②中不能使用氢氧化钙溶液的原因可能是_______ 。
【交流反思】
(4)下面是管道疏通剂的作用原理,你认为正确的是_______ 。
A.氢氧化钠溶于水放出热,促进管内油脂与其反应。
B.氢氧化钠能使有机残渣快速腐蚀,加快管道疏通。
C.管道疏通剂与水反应产生大量氧气,疏散堵塞物。
(5)经探究,过碳酸钠与水反应生成了碳酸钠和过氧化氢;过氧化氢在碱性条件下快速分解,其化学方程式为_______ 。
【查阅资料】该管道疏通剂中过碳酸钠的化学式为2Na2CO3·3H2O2,白色晶体,加入水中,剧烈反应并产生气体;香精只起除臭作用。
【理论推测】 兴趣小组的同学们根据所学知识和资料信息推测该气体为氧气。
【实验验证】 同学们选择下列实验装置开展验证实验。


(1)疏通剂与水反应剧烈,你认为应选择
(2)利用装置C收集一瓶气体,将带火星的木条伸入其中,现象为
【深入探究】 为检验疏通剂与水反应后剩余溶液中溶质成分,兴趣小组开展了下表所示的探究实验。( 提示:氯化钙溶液呈中性)
(3)请完善下面的表格。
| 实验步骤 | 实验现象 | 实验结论 |
| ①取适量该疏通剂于烧杯中,加少量水,触摸烧杯外壁。 | 烧杯外壁发烫 | 疏通剂加入水中会 |
| ②取少许实验①的溶液于试管中,滴加过量的氯化钙溶液,静置,观察现象。 | 溶液中溶质含有Na2CO3 | |
| ③ | 溶液变红 | 溶液中溶质含有NaOH |
【交流反思】
(4)下面是管道疏通剂的作用原理,你认为正确的是
A.氢氧化钠溶于水放出热,促进管内油脂与其反应。
B.氢氧化钠能使有机残渣快速腐蚀,加快管道疏通。
C.管道疏通剂与水反应产生大量氧气,疏散堵塞物。
(5)经探究,过碳酸钠与水反应生成了碳酸钠和过氧化氢;过氧化氢在碱性条件下快速分解,其化学方程式为
您最近一年使用:0次
2023-09-05更新
|
78次组卷
|
2卷引用:四川省彭州市2023-2024学年高三上学期期中考试理综化学试题
解题方法
9 . 下图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容。现用该浓硫酸配制
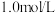 的稀硫酸。可供选用的仪器有:①玻璃棒;②烧杯;③药匙;④量筒;⑤托盘天平。请回答下列问题:
的稀硫酸。可供选用的仪器有:①玻璃棒;②烧杯;③药匙;④量筒;⑤托盘天平。请回答下列问题:
(1)配制上述稀硫酸时,还缺少的仪器有___________ (写仪器名称);
(2)配制
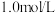 的稀硫酸需要用量筒量取上述浓硫酸的体积为
的稀硫酸需要用量筒量取上述浓硫酸的体积为___________ mL,量取硫酸时应选用以下___________ 规格的量筒(填选项)。
A. B.
B. C.
C. D.
D.
(3)根据计算结果,进行如下实验操作:
①用量筒量取计算所需体积的浓硫酸;
②向量筒中加入少量蒸馏水,并用玻璃棒搅拌;
③待溶液冷却到室温,转移入容量瓶中;
④然后将蒸馏水沿玻璃棒注入容量瓶直至刻度线;
⑤把容量瓶盖盖紧,上下颠倒摇匀
你认为上述实验中错误的操作是___________ (填序号)
(4)若遇到下列情况,对配制硫酸的物质的量浓度有何影响(填“偏高”“偏低”或“不变”)
①用于稀释硫酸的烧杯未洗涤___________ ;
②容量瓶中有少量的蒸馏水___________ 。

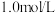 的稀硫酸。可供选用的仪器有:①玻璃棒;②烧杯;③药匙;④量筒;⑤托盘天平。请回答下列问题:
的稀硫酸。可供选用的仪器有:①玻璃棒;②烧杯;③药匙;④量筒;⑤托盘天平。请回答下列问题:| 硫酸 化学纯(CP)(  ) )品名:硫酸 化学式:  相对分子质量:98 密度:  质量分数:98%(  ) ) |
(2)配制

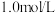 的稀硫酸需要用量筒量取上述浓硫酸的体积为
的稀硫酸需要用量筒量取上述浓硫酸的体积为A.
 B.
B. C.
C. D.
D.
(3)根据计算结果,进行如下实验操作:
①用量筒量取计算所需体积的浓硫酸;
②向量筒中加入少量蒸馏水,并用玻璃棒搅拌;
③待溶液冷却到室温,转移入容量瓶中;
④然后将蒸馏水沿玻璃棒注入容量瓶直至刻度线;
⑤把容量瓶盖盖紧,上下颠倒摇匀
你认为上述实验中错误的操作是
(4)若遇到下列情况,对配制硫酸的物质的量浓度有何影响(填“偏高”“偏低”或“不变”)
①用于稀释硫酸的烧杯未洗涤
②容量瓶中有少量的蒸馏水
您最近一年使用:0次
2023-08-11更新
|
205次组卷
|
2卷引用:海南省省直辖县级行政单位定安县高三联考2023-2024学年高三上学期11月月考化学试题
名校
解题方法
10 . 薰衣草精油常用作芳香剂、驱虫剂的原料。“DIY”兴趣小组在实验室从新鲜薰衣草中提取少量精油。
【查阅资料】薰衣草精油成分复杂,沸点范围100℃~220℃,相同温度时在水中溶解度小于在苯、四氯化碳(有毒、沸点76.8℃)等溶剂中的溶解度。
【设计方案】小组讨论后提出如下提取方案。(在横线上填写相应操作对应装置图的字
母 )

【方案实施】按预先设计的方案进行实验。
(1)步骤①:在研钵中将薰衣草捣碎,转移至小烧杯中并加入适量蒸馏水,搅拌使充分溶解后___________ 。
(2)步骤②:在薰衣草水中加入适量CCl4进行___________ ;溶有精油的CCl4层在___________ 层(填“上”或“下”)。
(3)步骤③:将分离出的CCl4层进行___________ 。收集温度在___________ ℃的馏分(该馏分可循环使用)。
(4)仪器e的名称是___________ 。冷却水的方向是___________ 进___________ 出(填“g”或“f)。
(5)利用上述实验装置进行相应实验,操作正确或能达到实验目的的是___________
A.蒸发操作,加热至(大量)固体出现时,应停止加热,利用余热蒸干
B.碘在酒精中的溶解度较大,可用酒精把碘水中的碘萃取出来
C.蒸馏海水,可在锥形瓶中收集到高浓度的氯化钠溶液
D.过滤操作时,要沿着玻璃棒慢慢向漏斗中倾倒过滤液
【查阅资料】薰衣草精油成分复杂,沸点范围100℃~220℃,相同温度时在水中溶解度小于在苯、四氯化碳(有毒、沸点76.8℃)等溶剂中的溶解度。
【设计方案】小组讨论后提出如下提取方案。(在横线上填写

【方案实施】按预先设计的方案进行实验。
(1)步骤①:在研钵中将薰衣草捣碎,转移至小烧杯中并加入适量蒸馏水,搅拌使充分溶解后
(2)步骤②:在薰衣草水中加入适量CCl4进行
(3)步骤③:将分离出的CCl4层进行
(4)仪器e的名称是
(5)利用上述实验装置进行相应实验,操作正确或能达到实验目的的是
A.蒸发操作,加热至(大量)固体出现时,应停止加热,利用余热蒸干
B.碘在酒精中的溶解度较大,可用酒精把碘水中的碘萃取出来
C.蒸馏海水,可在锥形瓶中收集到高浓度的氯化钠溶液
D.过滤操作时,要沿着玻璃棒慢慢向漏斗中倾倒过滤液
您最近一年使用:0次
2023-08-10更新
|
187次组卷
|
2卷引用:新疆石河子第一中学2023-2024学年高三上学期第二次月考化学试题



