1 . 实验测知久储的某NaOH固体中含有水的质量分数为3.5%,含 的质量分数为6.5%。若取质量为
的质量分数为6.5%。若取质量为 的此样品加入到含HCl质量为
的此样品加入到含HCl质量为 的稀盐酸(过量)中,完全反应后加入含NaOH质量为
的稀盐酸(过量)中,完全反应后加入含NaOH质量为 的NaOH溶液,恰好中和残余的盐酸,则所得溶液蒸干时得到晶体质量可能为
的NaOH溶液,恰好中和残余的盐酸,则所得溶液蒸干时得到晶体质量可能为
A.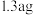 | B.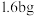 | C. | D. |
您最近一年使用:0次
解题方法
2 . 化学是以实验为主的自然科学,实验操作有严格的规范。下列实验操作的描述错误的是
| A.向沸水中滴加饱和FeCl3溶液,用玻璃棒不断搅拌并继续煮沸至溶液呈透明的红褐色即可制得氢氧化铁胶体 |
| B.配制一定体积某浓度的稀硫酸,将浓硫酸稀释后立即转移入容量瓶并定容,所配溶液浓度偏大 |
| C.容量瓶检漏方法:向容量瓶中加水,塞好瓶塞,将容量瓶倒转过来,若不漏水,将容量瓶正立后,将瓶塞旋转180°,再倒转,看是否漏水 |
| D.用质量分数为98%,密度为1.84g·mL-1浓硫酸,配240mL 2mol·L-1稀硫酸,需用量筒量取浓硫酸26.1mL |
您最近一年使用:0次
名校
解题方法
3 . 向三份同浓度的25mL盐酸中分别加入质量不等的NaHCO3、KHCO3的混合物,测得产生气体的体积如下表所示(不考虑气体溶解)
下列分析推理正确的是
| 编号 | 1 | 2 | 3 |
| m(混合物)/g | 4.6 | 7.2 | 7.9 |
| V(CO2)(标准状况)/L | 1.12 | 1.68 | 1.68 |
| A.根据实验1中的数据可以计算出盐酸的浓度 |
| B.混合物中NaHCO3的质量分数约为45.7% |
| C.根据第2、3组数据可以分析出第2组中的混合物完全反应 |
D.盐酸的物质的量浓度为3mol L-1 L-1 |
您最近一年使用:0次
名校
4 . 已知: ,若
,若 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 ,若
,若 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.10g质量分数为28%的NaOH溶液中含氢原子数目为 |
B.0.1 mol/L NaCN溶液中含阴离子总数大于 |
C.当生成1 mol NaSCN消耗11.2 L  |
D.相同温度下,相同体积的两个容器中,加入等质量的 和 和 ,则两个容器内的压强之比为3:2 ,则两个容器内的压强之比为3:2 |
您最近一年使用:0次
5 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
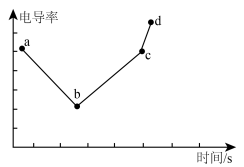
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
A. 质量分数为46%的乙醇 质量分数为46%的乙醇 溶液中,含有的氢原子数为 溶液中,含有的氢原子数为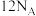 |
B.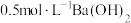 溶液中含有 溶液中含有 的数目为 的数目为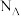 |
C.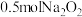 固体中含有离子总数目为 固体中含有离子总数目为 |
D.标准状况下,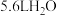 有的原子数目为 有的原子数目为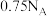 |
您最近一年使用:0次
名校
6 . 标准状况下VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为w,物质的量浓度为cmol/L,则下列关系中错误的是
A.ρ=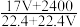 | B.w=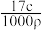 |
C.w=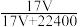 | D.w=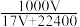 |
您最近一年使用:0次
2023-11-12更新
|
255次组卷
|
2卷引用:上海市上海中学2023-2024学年高一上学期10月月考化学试题
名校
7 . 下列说法正确的是
A.将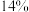 的 的 溶液蒸发掉 溶液蒸发掉 水后,变为 水后,变为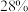 的 的 溶液 溶液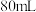 ,该 ,该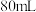 溶液的物质的量浓度为 溶液的物质的量浓度为 |
B.把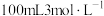 的 的 溶液与 溶液与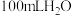 混合后,硫酸的物质的量浓度变为 混合后,硫酸的物质的量浓度变为 |
C.某 溶液的密度为 溶液的密度为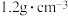 , , 的质量分数为 的质量分数为 , , 该溶液中 该溶液中 的物质的量为 的物质的量为 |
D.已知 氨水的密度为 氨水的密度为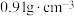 , , 氨水的密度为 氨水的密度为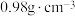 ,若将上述两溶液等体积混合,所得氨水的质量分数大于 ,若将上述两溶液等体积混合,所得氨水的质量分数大于 |
您最近一年使用:0次
2023-10-11更新
|
301次组卷
|
3卷引用:山东省普通高中大联考2023-2024学年高一10月月考化学试题
8 . 标准状况下,将 某气体(摩尔质量为
某气体(摩尔质量为 )溶于
)溶于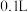 水(密度
水(密度 )中,所得溶液的密度为
)中,所得溶液的密度为 ,质量分数为
,质量分数为 ,则此溶液的物质的量浓度
,则此溶液的物质的量浓度 为
为
 某气体(摩尔质量为
某气体(摩尔质量为 )溶于
)溶于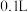 水(密度
水(密度 )中,所得溶液的密度为
)中,所得溶液的密度为 ,质量分数为
,质量分数为 ,则此溶液的物质的量浓度
,则此溶液的物质的量浓度 为
为A.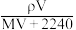 | B.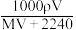 | C.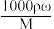 | D.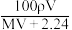 |
您最近一年使用:0次
名校
解题方法
9 . 将agNH3溶于水得到VmL溶液,假设该溶液的密度为ρg/cm3,质量分数为w,溶液中NH 为bmol。已知氨水的密度比水小且浓度越大密度越小。下列叙述正确的是
为bmol。已知氨水的密度比水小且浓度越大密度越小。下列叙述正确的是
 为bmol。已知氨水的密度比水小且浓度越大密度越小。下列叙述正确的是
为bmol。已知氨水的密度比水小且浓度越大密度越小。下列叙述正确的是A.据电荷守恒知:溶液中c(OH-)=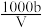 +c(H+) +c(H+) |
B.溶质的质量分数为w= ×100% ×100% |
C.溶质的物质的量浓度c=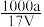 mol/L mol/L |
| D.上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5w |
您最近一年使用:0次
解题方法
10 . 配制 溶液时,将
溶液时,将 溶于水,所得溶液的体积为
溶于水,所得溶液的体积为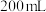 ,溶液的密度为
,溶液的密度为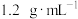 ,再将溶液稀释成
,再将溶液稀释成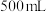 。下列说法正确的是
。下列说法正确的是
 溶液时,将
溶液时,将 溶于水,所得溶液的体积为
溶于水,所得溶液的体积为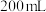 ,溶液的密度为
,溶液的密度为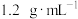 ,再将溶液稀释成
,再将溶液稀释成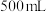 。下列说法正确的是
。下列说法正确的是A.稀释前溶液中 的物质的量浓度为 的物质的量浓度为 |
B.稀释前溶液中 的质量分数为 的质量分数为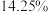 |
C.稀释后溶液中 的物质的量浓度为 的物质的量浓度为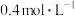 |
D.稀释后溶液中 的物质的量浓度为 的物质的量浓度为 |
您最近一年使用:0次



