1 . 下列说法正确的是
| A.Na跟水反应所得产物既有电解质又有非电解质 |
| B.加入还原剂才可完成NaCl→Na的转化 |
C.过氧化钠的电子式为 |
| D.Na2CO3溶液显碱性,Na2CO3属于盐类 |
您最近一年使用:0次
名校
2 . 如图是部分短周期主族元素原子半径与原子序数的关系,下列说法正确的是


| A.最高价氧化物对应的水化物的碱性:Z<M |
| B.M的氧化物属于碱性氧化物,N的氧化物属于酸性氧化物 |
| C.X、Y两种元素简单气态氢化物的稳定性:X>Y |
| D.简单离子的半径:Z<Y<R |
您最近一年使用:0次
2024-03-21更新
|
121次组卷
|
4卷引用:河南省周口市鹿邑县2023-2024学年高一上学期1月期末化学试题
名校
解题方法
3 . 分类是科学研究的重要方法。下列物质分类正确的是
| A.碱性氧化物:Fe2O3、Na2O2、Al2O3 |
| B.盐:硫酸氢铵、氯化铝、过氧化钠 |
| C.电解质:二氧化碳、氨气、氯气 |
| D.碱:烧碱、一水合氨、消石灰 |
您最近一年使用:0次
2024-03-17更新
|
99次组卷
|
2卷引用:安徽省六安第二中学2023-2024学年高一上学期期末考试化学试题
解题方法
4 . Ⅰ.铁是一种常见的金属,它的单质及化合物在生活生产中处处可见。
(1)苹果中含有丰富的铁元素,新榨的苹果汁是浅绿色的,在空气中久置后会变成黄色,原因是___________ ,若再向其中加入少量的维生素C,又将恢复浅绿色,上述过程中,氧气是___________ 剂(选填“氧化”或“还原”,下同),维生素C是___________ 剂。
Ⅱ.铁及其重要化合物的“价类二维图”如下图所示。

(2)该“价类二维图”中缺失的类别A应为___________ 。
(3)要实现Fe转化为Fe3O4,除了将Fe与氧气点燃外,另外的方法是(写出化学方程式)___________ 。
(4)下列关于金属冶炼的说法中正确的是____;
(5)有关合金的说法错误的是____。
(6)生活中的钢铁制品如废旧铁锅,使用时间长久后若要丢弃,应归为____。
(7)在烧制砖瓦时,用黏土做成的坯经过烘烧后,铁的化合物转化成而制得红色砖瓦____。
(8)要实现Fe转化为Fe2+,可选用足量的____。
(9)下列各组离子在溶液中能大量共存的是____。
(10)有失去标签的NaCl、FeCl2、FeCl3、MgCl2四种溶液,只需要一种试剂就可以把它们鉴别开来,这种试剂是____。
Ⅲ.某化学兴趣小组同学设计以下实验探究氢氧化亚铁的制备:
两组同学分别设计如下实验探究能较长时间观察到白色Fe(OH)2沉淀的制取方法。
A组实验:用NaOH溶液和FeSO4溶液直接反应。(如图)

(11)FeSO4可由铁粉还原Fe2(SO4)3制得,反应的离子方程式是:___________ 。
(12)该方法能观察到白色Fe(OH)2沉淀,但沉淀颜色快速发生变化,其颜色变化为___________ 。
B组实验:选用稀硫酸、铁粉、NaOH溶液进行实验,装置如图。

(13)实验时,先___________ (填“打开”或“关闭”)止水夹K,然后打开分液漏斗的玻璃塞和活塞,使稀硫酸与铁粉反应,一段时间后,___________ (填“打开”或“关闭”)止水夹K,制得白色Fe(OH)2沉淀,且沉淀能持续一段时间不变色。
(1)苹果中含有丰富的铁元素,新榨的苹果汁是浅绿色的,在空气中久置后会变成黄色,原因是
Ⅱ.铁及其重要化合物的“价类二维图”如下图所示。

(2)该“价类二维图”中缺失的类别A应为
(3)要实现Fe转化为Fe3O4,除了将Fe与氧气点燃外,另外的方法是(写出化学方程式)
(4)下列关于金属冶炼的说法中正确的是____;
| A.通过电解饱和食盐水制备金属钠 |
| B.热还原法常用的还原剂有CO、H2、C等 |
| C.金属Mg、Al均能通过电解熔融氯化物的方法获得 |
| D.人类历史上金属被发现的顺序与金属的活泼性无关 |
(5)有关合金的说法错误的是____。
| A.熔点通常低于组成金属 | B.任意两种金属均可以形成合金 |
| C.钢比生铁的含碳量低 | D.可能含有非金属 |
(6)生活中的钢铁制品如废旧铁锅,使用时间长久后若要丢弃,应归为____。
| A.干垃圾 | B.湿垃圾 | C.有毒有害垃圾 | D.可回收垃圾 |
(7)在烧制砖瓦时,用黏土做成的坯经过烘烧后,铁的化合物转化成而制得红色砖瓦____。
| A.Fe2O3 | B.Fe3O4 | C.FeO | D.Fe(OH)3 |
(8)要实现Fe转化为Fe2+,可选用足量的____。
| A.浓硫酸 | B.氯气 | C.稀硝酸 | D.稀硫酸 |
(9)下列各组离子在溶液中能大量共存的是____。
A.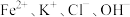 | B.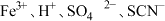 |
C. | D. |
(10)有失去标签的NaCl、FeCl2、FeCl3、MgCl2四种溶液,只需要一种试剂就可以把它们鉴别开来,这种试剂是____。
| A.氨水 | B.盐酸 | C.Na2SO4溶液 | D.KSCN溶液 |
Ⅲ.某化学兴趣小组同学设计以下实验探究氢氧化亚铁的制备:
两组同学分别设计如下实验探究能较长时间观察到白色Fe(OH)2沉淀的制取方法。
A组实验:用NaOH溶液和FeSO4溶液直接反应。(如图)

(11)FeSO4可由铁粉还原Fe2(SO4)3制得,反应的离子方程式是:
(12)该方法能观察到白色Fe(OH)2沉淀,但沉淀颜色快速发生变化,其颜色变化为
B组实验:选用稀硫酸、铁粉、NaOH溶液进行实验,装置如图。

(13)实验时,先
您最近一年使用:0次
名校
解题方法
5 . 下列物质分类正确的是
| 碱 | 电解质 | 碱性氧化物 | 共价化合物 | 离子化合物 | |
| A | KOH | Na2SO4 | Na2O | HCl | Na2O2 |
| B | 氢氧化铝 |  | Na2O2 | N2 | H2SO4 |
| C | 纯碱 | 漂白粉 | Fe2O3 | KCl | HCl |
| D | Cu(OH)2 | 盐酸 | 氧化铝 | H2O2 | KF |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-12更新
|
127次组卷
|
2卷引用:宁夏回族自治区石嘴山市第三中学2023-2024学年高一上学期1月期末化学试题
解题方法
6 . 铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:
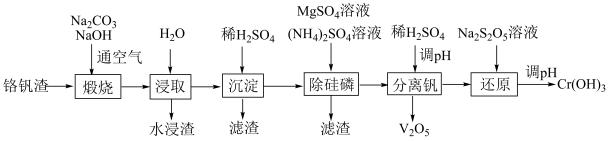
已知:最高价铬酸根在酸性介质中以Cr2O 存在,在碱性介质中以CrO
存在,在碱性介质中以CrO 存在。回答下列问题:
存在。回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为___________ (填化学式)。
(2)水浸渣中主要有SiO2和___________ 。
(3)“分离钒”步骤中,将溶液pH调到1.8左右得到V2O5沉淀,V2O5在pH<1时,溶解为VO 或VO3+;在碱性条件下,溶解为VO
或VO3+;在碱性条件下,溶解为VO 或VO
或VO ,上述性质说明V2O5具有
,上述性质说明V2O5具有___________ (填标号)。
A.酸性 B.碱性 C.两性
(4)“还原”步骤中加入焦亚硫酸钠(Na2S2O5)溶液,反应的离子方程式为___________ 。

已知:最高价铬酸根在酸性介质中以Cr2O
 存在,在碱性介质中以CrO
存在,在碱性介质中以CrO 存在。回答下列问题:
存在。回答下列问题:(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为
(2)水浸渣中主要有SiO2和
(3)“分离钒”步骤中,将溶液pH调到1.8左右得到V2O5沉淀,V2O5在pH<1时,溶解为VO
 或VO3+;在碱性条件下,溶解为VO
或VO3+;在碱性条件下,溶解为VO 或VO
或VO ,上述性质说明V2O5具有
,上述性质说明V2O5具有A.酸性 B.碱性 C.两性
(4)“还原”步骤中加入焦亚硫酸钠(Na2S2O5)溶液,反应的离子方程式为
您最近一年使用:0次
7 . 下列各组物质,按化合物、单质、混合物的顺序排列的是
| A.明矾、石墨、熟石灰 | B.食盐水、白磷、冰水混合物 |
| C.干冰、铁、液氧 | D.烧碱、氮气、盐酸 |
您最近一年使用:0次
8 . 下列关于化学的应用和记载对其说明不合理的是
| A.《天工开物》中记载了火法炼锌的工艺,冶炼过程中锌元素被还原 |
B.《本草经集注》中记载了区分硝石( )和朴硝( )和朴硝( )的方法:“以火烧之,紫青烟起,乃真硝石也”,二者可以利用“焰色试验”区分 )的方法:“以火烧之,紫青烟起,乃真硝石也”,二者可以利用“焰色试验”区分 |
C.《神农本草经》中提到“白青[ ]得铁化为铜”,其中白青属于碱 ]得铁化为铜”,其中白青属于碱 |
| D.先秦文献《考工记》记录了六类青铜器物的合金成分配比,合金的熔点一般比纯金属的低 |
您最近一年使用:0次
2024-02-27更新
|
181次组卷
|
3卷引用:吉林省长春市东北师大附中2023-2024学年高一上学期期末考试化学试题
名校
解题方法
9 . 下列关于物质的分类中,正确的是
| 酸性氧化物 | 酸 | 盐 | 混合物 | 电解质 | |
| A |  |  | 烧碱 |  |  |
| B | 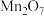 |  |  | 漂白粉 |  |
| C |  |  | 纯碱 |  胶体 胶体 |  |
| D |  |  |  | 铝热剂 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-27更新
|
208次组卷
|
3卷引用:吉林省长春市东北师大附中2023-2024学年高一上学期期末考试化学试题
名校
解题方法
10 . 下列物质的分类不正确 的是
| A.刚玉——氧化物 | B.重晶石——正盐 | C.氨水——碱 | D.玻璃——混合物 |
您最近一年使用:0次
2024-02-24更新
|
109次组卷
|
2卷引用:海南华侨中学2023-2024学年高一上学期期末考试化学试题



