解题方法
1 . 为探究铁和铁的化合物的一些化学性质,某学生实验小组设计了以下实验。
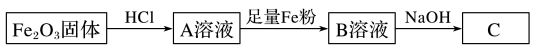
(1)往A、B溶液中分别滴入几滴KSCN溶液,溶液的颜色:A_________ ,B_________ 。
(2)写出上述过程中有关反应的化学方程式: →A
→A_________ ,A→B_________ 。
(3)向B溶液中逐滴加入NaOH得到C,此过程中可观察到的现象是_________ 。
(4)将A的饱和溶液滴入沸水中并不断加热,可制得_________ 胶体;当光束通过该胶体时,可看到一条光亮的“通路”,这种现象称为_________ 。
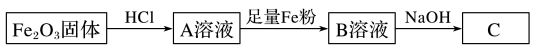
(1)往A、B溶液中分别滴入几滴KSCN溶液,溶液的颜色:A
(2)写出上述过程中有关反应的化学方程式:
 →A
→A(3)向B溶液中逐滴加入NaOH得到C,此过程中可观察到的现象是
(4)将A的饱和溶液滴入沸水中并不断加热,可制得
您最近一年使用:0次
2022-12-02更新
|
136次组卷
|
2卷引用:辽宁省沈阳市辽中区第二高级中学2022-2023学年高一上学期期中考试化学试题
名校
解题方法
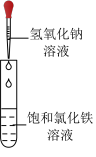
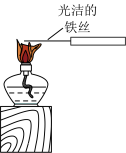
2 . 下列实验装置能达到实验目的的是
| ①验证Na和水反应是否为放热反应 | ②制备氢氧化铁胶体 | ③观察K2CO3的焰色试验 | ④比较Na2CO3、NaHCO3的稳定性 |
 |  |  | 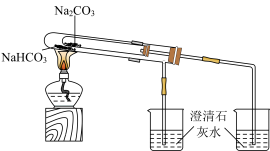 |
| A.只有① | B.只有①② | C.只有①②③ | D.全部 |
您最近一年使用:0次
解题方法
3 . 为探究铁和铁的化合物的一些化学性质,某学生实验小组设计了以下实验。
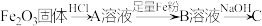
(1)往A、B溶液中分别滴入几滴KSCN溶液,溶液的颜色:A____ ,B____ 。
(2)写出上述过程中有关反应的化学方程式:Fe2O3→A____ ,A→B____ 。
(3)向B溶液中逐滴加入NaOH得到C,此过程中可观察到的现象是____ 。
(4)将A的饱和溶液滴入沸水中并不断加热,可制得____ 胶体;当光束通过该胶体时,可看到一条光亮的“通路”,这种现象称为____ 。
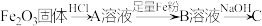
(1)往A、B溶液中分别滴入几滴KSCN溶液,溶液的颜色:A
(2)写出上述过程中有关反应的化学方程式:Fe2O3→A
(3)向B溶液中逐滴加入NaOH得到C,此过程中可观察到的现象是
(4)将A的饱和溶液滴入沸水中并不断加热,可制得
您最近一年使用:0次
名校
解题方法
4 . 下列关于胶体的说法,正确的是
| A.胶体与溶液和浊液的本质区别是能够发生丁达尔效应 |
B.利用过滤的方法能将 胶体从 胶体从 溶液中分离出来 溶液中分离出来 |
| C.牛奶、云、雾、有色玻璃都属于胶体 |
| D.向浓氨水中缓慢滴加足量的氯化铁饱和溶液可制得氢氧化铁胶体 |
您最近一年使用:0次
2022-11-16更新
|
363次组卷
|
3卷引用:辽宁省沈阳、大连、丹东、本溪等协作校2022-2023学年高一上学期期中考试化学试题
5 . 实验室以铁碳化合物(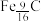 )为主要原料,制备
)为主要原料,制备 溶液,步骤如下:
溶液,步骤如下:
步骤Ⅰ:称取5.6g铁碳化合物,在足量空气中高温灼烧,生成有磁性的固体X。
步骤Ⅱ:将X与过量3mol/L的盐酸反应,向反应后溶液中加入过量 溶液。
溶液。
步骤Ⅲ:将“步骤Ⅱ”所得的溶液加热煮沸一段时间,冷却。
回答下列问题:
(1)步骤Ⅰ中用到的硅酸盐仪器有酒精灯、玻璃棒、_______ 、_______ ,若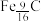 充分反应,则X的质量=
充分反应,则X的质量=_______ g。
(2)实验室有各种规格的常用容量瓶,用 的盐酸和蒸馏水配制
的盐酸和蒸馏水配制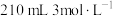 盐酸。
盐酸。
①配制时需要用量筒量取_______  的盐酸。
的盐酸。
②下列操作导致所配溶液浓度偏高的是_______ (填标号)。
a.定容时俯视刻度线
b.转移溶液时有液体溅出
c.配制溶液时容量瓶中有少许蒸馏水
d.量取12mol/L的盐酸时仰视读数
(3)步骤Ⅱ中X与过量盐酸反应后,溶液中含有的盐的化学式为 、
、_______ ,若将 溶液中的
溶液中的 氧化成
氧化成 ,转移电子的物质的量为
,转移电子的物质的量为_______ mol。
(4)用步骤Ⅲ所制得的 溶液制备
溶液制备 胶体的具体操作为
胶体的具体操作为_______ ,检验制备胶体成功的方法是_______ 。
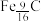 )为主要原料,制备
)为主要原料,制备 溶液,步骤如下:
溶液,步骤如下:步骤Ⅰ:称取5.6g铁碳化合物,在足量空气中高温灼烧,生成有磁性的固体X。
步骤Ⅱ:将X与过量3mol/L的盐酸反应,向反应后溶液中加入过量
 溶液。
溶液。步骤Ⅲ:将“步骤Ⅱ”所得的溶液加热煮沸一段时间,冷却。
回答下列问题:
(1)步骤Ⅰ中用到的硅酸盐仪器有酒精灯、玻璃棒、
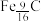 充分反应,则X的质量=
充分反应,则X的质量=(2)实验室有各种规格的常用容量瓶,用
 的盐酸和蒸馏水配制
的盐酸和蒸馏水配制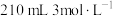 盐酸。
盐酸。①配制时需要用量筒量取
 的盐酸。
的盐酸。②下列操作导致所配溶液浓度偏高的是
a.定容时俯视刻度线
b.转移溶液时有液体溅出
c.配制溶液时容量瓶中有少许蒸馏水
d.量取12mol/L的盐酸时仰视读数
(3)步骤Ⅱ中X与过量盐酸反应后,溶液中含有的盐的化学式为
 、
、 溶液中的
溶液中的 氧化成
氧化成 ,转移电子的物质的量为
,转移电子的物质的量为(4)用步骤Ⅲ所制得的
 溶液制备
溶液制备 胶体的具体操作为
胶体的具体操作为
您最近一年使用:0次
2022-11-13更新
|
108次组卷
|
2卷引用:辽宁省朝阳市建平县2022-2023学年高三上学期11月期中考试化学试题
名校
解题方法
6 . 宏观辨识与微观探析是化学学科核心素养之一,下列离子方程式能准确解释相应事实的是
A.工业上制漂白粉: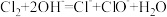 |
B. 通入水中: 通入水中: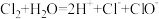 |
C.钠与水反应: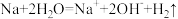 |
D.用饱和氯化铁溶液制取氢氧化铁胶体: |
您最近一年使用:0次
解题方法
7 . 某实验小组制备 胶体的步骤如下,其中操作正确的是
胶体的步骤如下,其中操作正确的是
 胶体的步骤如下,其中操作正确的是
胶体的步骤如下,其中操作正确的是A.向煮沸的 溶液中滴加几滴NaOH溶液,继续加热至液体呈红褐色,停止加热 溶液中滴加几滴NaOH溶液,继续加热至液体呈红褐色,停止加热 |
B.向煮沸的蒸馏水中滴加几滴饱和 溶液,继续加热至液体呈红褐色,停止加热 溶液,继续加热至液体呈红褐色,停止加热 |
C.向煮沸的 溶液中滴加几滴NaOH溶液,用玻璃棒不断搅拌,至液体呈红褐色,停止加热 溶液中滴加几滴NaOH溶液,用玻璃棒不断搅拌,至液体呈红褐色,停止加热 |
D.向煮沸的蒸馏水中滴加几滴饱和 溶液,用玻璃棒不断搅拌,至液体呈红褐色 溶液,用玻璃棒不断搅拌,至液体呈红褐色 |
您最近一年使用:0次
解题方法
8 . 下列关于胶体的叙述正确的是
| A.有色玻璃是胶体,能产生丁达尔效应 |
| B.溶液呈电中性,胶体带有电荷 |
| C.将胶体过滤,在滤纸上能得到分散质 |
| D.在饱和氯化铁溶液中逐滴加入NaOH溶液,产生红褐色的Fe(OH)3胶体 |
您最近一年使用:0次
2022-11-06更新
|
197次组卷
|
2卷引用:辽宁省沈阳市市级重点高中联合体2022-2023学年高一上学期期中测试化学试题
名校
解题方法
9 . 高铁酸钠(Na2FeO4)是水处理过程中的一种新型的绿色多功能净水剂。其净水过程中所发生的化学反应主要为4Na2FeO4+10H2O=4Fe(OH)3(胶体)+3O2↑+8NaOH。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。请回答下列问题:
(1)高铁酸钠(Na2FeO4)属于____ (“酸”、“碱”、“盐”或“氧化物”),其中铁 化合价为
化合价为____ 价;与O2互为同素异形体的物质的化学式为____ 。
(2)将上述反应的化学方程式改写成离子方程式:____ ,该反应中物质的氧化性大小关系是:____ 。
(3)实验室制备Fe(OH)3胶体的操作:向烧杯中加入40mL蒸馏水,将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴____ 溶液,继续煮沸至溶液呈____ ,停止加热,写出实验室制备Fe(OH)3胶体的化学方程式为____ 。
(4)当生成48gO2时,生成的NaOH的质量为____ g。
(1)高铁酸钠(Na2FeO4)属于
 化合价为
化合价为(2)将上述反应的化学方程式改写成离子方程式:
(3)实验室制备Fe(OH)3胶体的操作:向烧杯中加入40mL蒸馏水,将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴
(4)当生成48gO2时,生成的NaOH的质量为
您最近一年使用:0次
2022-10-29更新
|
109次组卷
|
2卷引用:辽宁省大连市第一〇三中学2022-2023学年高一上学期第一次月考化学试题
10 . 新冠变异毒株可通过咳嗽、打喷嚏、说话等形成的飞沫传播,飞沫直径在1〜100nm之间,口罩可以预防和降低感染的风险性。下列有关说法正确的是
| A.直径为1〜100nm的飞沫分散到空气中形成的分散系为胶体 |
| B.胶体与其他分散系的本质区别是胶体可以产生丁达尔效应 |
C.向 饱和溶液中逐滴加入NaOH溶液,可制得 饱和溶液中逐滴加入NaOH溶液,可制得 胶体 胶体 |
| D.NaCl溶液、葡萄糖溶液和纯水都属于分散系 |
您最近一年使用:0次



