名校
1 . 针对下表中的9种元素,用化学用语回答下列问题:
(1)写出⑧的原子结构示意图:_________________________ 。
(2)形成物质种类最多的元素是__________________ 。
(3)用电子式表示⑤和⑨形成化合物的过程__________________ 。
(4)⑤⑥⑦最高正价氧化物对应水化物碱性由强至弱的顺序是_____________ 。
(5)④的单质与甲醇(CH3OH)形成的碱性燃料电池的负极方程式:________________ 。
(6)写出⑦的单质与三氧化二铁反应的化学方程式____________________ 。
(7)③和④的气态氢化物的稳定性顺序为:______________ 。④和⑧的气态氢化物的沸点顺序为:_____________ ,出现这种变化的原因是:_____________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
(2)形成物质种类最多的元素是
(3)用电子式表示⑤和⑨形成化合物的过程
(4)⑤⑥⑦最高正价氧化物对应水化物碱性由强至弱的顺序是
(5)④的单质与甲醇(CH3OH)形成的碱性燃料电池的负极方程式:
(6)写出⑦的单质与三氧化二铁反应的化学方程式
(7)③和④的气态氢化物的稳定性顺序为:
您最近一年使用:0次
名校
2 . KMnO4是一种常见的强氧化剂,主要用于防腐、化工、制药等。现以某种软锰矿(主要成分MnO2,还有Fe2O3、Al2O3、SiO2等)作脱硫剂,通过如下简化流程既脱除燃煤尾气中的SO2,又制得KMnO4(反应条件已经省略)。
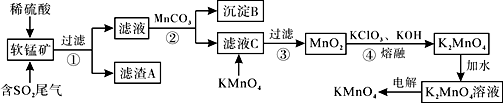
已知:Ksp[Fe(OH)3]=4×10-38,Ksp[Al(OH)3]=1×10-33。回答下列问题:
(1)K2MnO4中Mn的化合价为___________ 。
(2)滤渣A的成分是_________ ,析出沉淀B时,首先析出的物质是_________ 。
(3)步骤2中加入MnCO3的作用为_______________ 。
(4)滤液C中加入KMnO4时发生反应的离子方程式是_________________ 。
(5)步骤4中反应的化学方程式是_______________ 。
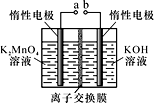
(6)电解制备KMnO4的装置如图所示。b与电源的______ 极相连,电解液中最好选择_______ 离子交换膜(填“阳”或“阴”)。电解时,阳极的电极反应式为_________ 。

已知:Ksp[Fe(OH)3]=4×10-38,Ksp[Al(OH)3]=1×10-33。回答下列问题:
(1)K2MnO4中Mn的化合价为
(2)滤渣A的成分是
(3)步骤2中加入MnCO3的作用为
(4)滤液C中加入KMnO4时发生反应的离子方程式是
(5)步骤4中反应的化学方程式是
(6)电解制备KMnO4的装置如图所示。b与电源的

您最近一年使用:0次
2019-01-25更新
|
1214次组卷
|
2卷引用:四川省绵阳市2019届高三上学期第二次(1月)诊断性考试理科综合化学试题



