20-21高一上·全国·课时练习
解题方法
1 . 有A、B、C、D、E五种微粒:
I.A微粒不带电,其质量数为1;
II.B微粒呈电中性,得2个电子后,其电子层结构与Ne相同;
III.C微粒带有一个单位的正电荷,核电荷数为11;
IV.D微粒核内有14个中子,核外M层上有3个电子;
V.E微粒核外有18个电子,当失去一个电子时呈电中性。
(1)写出A微粒的符号_______ ,B微粒的结构示意图_______ ,C微粒的电子式_______ ,D微粒的质量数_______ ,E微粒的结构示意图_______ ;
(2)B、C、E所属三种元素可组成多种物质,请写出它们的化学式_______ 、_______ 。
I.A微粒不带电,其质量数为1;
II.B微粒呈电中性,得2个电子后,其电子层结构与Ne相同;
III.C微粒带有一个单位的正电荷,核电荷数为11;
IV.D微粒核内有14个中子,核外M层上有3个电子;
V.E微粒核外有18个电子,当失去一个电子时呈电中性。
(1)写出A微粒的符号
(2)B、C、E所属三种元素可组成多种物质,请写出它们的化学式
您最近一年使用:0次
解题方法
2 . I.按要求回答下列问题:
(1)某粒子有1个原子核,核中有17个质子、20个中子,核外有18个电子,该粒子的化学符号是___________ 。
(2)写出下列物质的电子式:
_______ ,
________ ,
_______ 。
(3)用电子式表示下列化合物的形成过程: :
:_____________ ; :
:_______________ 。
Ⅱ.如图为元素周期表的一部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
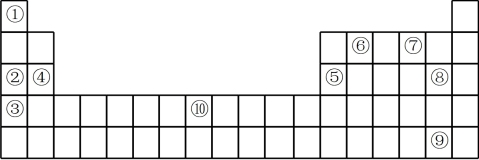
(1)②③④三种元素最高价氧化物对应水化物的碱性由强到弱的顺序是______ (填化学式)。
(2)10种元素中,原子半径最小的是________ (填序号)。
(3)元素⑦的简单氢化物与元素⑧的单质反应的离子方程式为_____________ 。
(4)元素②和⑤的最高价氧化物对应水化物相互反应的化学方程式为____________ 。
(5)元素⑩的原子序数为______ ,其单质与元素⑦的简单氢化物在高温下反应的化学方程式为________________ 。
(6)元素⑨的单质易溶于元素⑥与⑧形成的化合物中,所得溶液颜色为______ 色。
(1)某粒子有1个原子核,核中有17个质子、20个中子,核外有18个电子,该粒子的化学符号是
(2)写出下列物质的电子式:



(3)用电子式表示下列化合物的形成过程:
 :
: :
:Ⅱ.如图为元素周期表的一部分,列出了10种元素在元素周期表中的位置,试回答下列问题:

(1)②③④三种元素最高价氧化物对应水化物的碱性由强到弱的顺序是
(2)10种元素中,原子半径最小的是
(3)元素⑦的简单氢化物与元素⑧的单质反应的离子方程式为
(4)元素②和⑤的最高价氧化物对应水化物相互反应的化学方程式为
(5)元素⑩的原子序数为
(6)元素⑨的单质易溶于元素⑥与⑧形成的化合物中,所得溶液颜色为
您最近一年使用:0次
解题方法
3 . (1)将下列符合要求的组别字母填入相应位置
A.O2和O3B.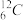 和
和 C.CH3CH2CH2CH3和
C.CH3CH2CH2CH3和
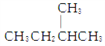
D. E.CH3CH2CH2CH3和
E.CH3CH2CH2CH3和
①___________ 组两种微粒互为同位素;
②__________ 组两种物质互为同素异形体;
③___________ 组两种物质属于同系物;
④___________ 组两物质互为同分异构体;
⑤___________ 组两物质是同一物质。
(2)一定温度下,将3molA气体和1molB气体通入一容积固定为2L的密闭容器中,发生如下反应:3A(g)+B(g) xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为
xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为__________________ ,X为________ ,若反应经2min达到平衡,平衡时C的浓度________ 0.8mol/L(填“大于,小于或等于”)。
A.O2和O3B.
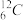 和
和 C.CH3CH2CH2CH3和
C.CH3CH2CH2CH3和
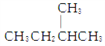
D.
 E.CH3CH2CH2CH3和
E.CH3CH2CH2CH3和
①
②
③
④
⑤
(2)一定温度下,将3molA气体和1molB气体通入一容积固定为2L的密闭容器中,发生如下反应:3A(g)+B(g)
 xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为
xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为
您最近一年使用:0次



