2010·上海徐汇·一模
1 . 用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路是成熟的传统工艺,现对某印刷电路生产厂家蚀刻绝缘板后所得的混合溶液(标记为A)进行如下分析:
①取50.0mL A溶液加入足量的硝酸银溶液,析出沉淀86.1g
②取50.0mL A溶液试探性地加入1.12g铁粉,结果全部溶解未见固体析出
③向实验②所得溶液中加入50 mL稀硝酸,产生1.12L NO(标准状况),反应后所得溶液的pH为1。
结合上述信息计算:
(1)所得沉淀的物质的量_____________mol;
(2)该厂所使用的FeCl3溶液的物质的量浓度_____________mol/L;
(3)A溶液中Cu2+的物质的量浓度。
①取50.0mL A溶液加入足量的硝酸银溶液,析出沉淀86.1g
②取50.0mL A溶液试探性地加入1.12g铁粉,结果全部溶解未见固体析出
③向实验②所得溶液中加入50 mL稀硝酸,产生1.12L NO(标准状况),反应后所得溶液的pH为1。
结合上述信息计算:
(1)所得沉淀的物质的量_____________mol;
(2)该厂所使用的FeCl3溶液的物质的量浓度_____________mol/L;
(3)A溶液中Cu2+的物质的量浓度。
您最近一年使用:0次
2012·辽宁·一模
2 . 若NA代表阿伏加德罗常数,则下列叙述正确的是
| A.1mol/L的氨水与等质量的水混合后(忽略体积变化),所得溶液浓度大于0.5mol/L |
| B.1mol Na2O2与足量的水完全反应,转移的电子数为2NA |
| C.在标准状况下,22.4L氢气与22.4L氦气所含有的原子数均为2NA |
| D.28g乙烯和环丙烷(C3H6)的混合气体含有的原子总数为3NA |
您最近一年使用:0次
11-12高三上·江苏泰州·期中
解题方法
3 . 常温下,海水在浓缩过程中析出盐的种类和质量(表中为每升海水析出的各种盐的克数。单位g/L)如下:
海水从密度为1.21 g/mL浓缩到密度为1.22g/mL时发生的变化是:
| 海水密度 (g/mL) | CaSO4 | NaCl | MgCl2 | MgSO4 | NaBr |
| 1.13 | 0.56 | ||||
| 1.20 | 0.91 | ||||
| 1.21 | 0.05 | 3.26 | 0.04 | 0.008 | |
| 1.22 | 0.015 | 9.65 | 0.01 | 0.04 | |
| 1.26 | 0.01 | 2.64 | 0.02 | 0.02 | 0.04 |
| 1.31 | 1.40 | 0.54 | 0.03 | 0.06 |
海水从密度为1.21 g/mL浓缩到密度为1.22g/mL时发生的变化是:
| A.各种盐的溶解度增大 | B.海水中水的质量分数减小 |
| C.析出的粗盐中 NaCl的质量分数增大 | D.海水中Br-浓度不变 |
您最近一年使用:0次
2010·四川成都·一模
4 . 用NA表示阿伏加德罗常数的值。下列叙述错误的是
| A.标准状况下,1.12 LHCHO所含的原子总数是0.2NA |
| B.标准状况下,11.2LC2H2和N2的混合气分子中叁键数目为0.5NA |
C.常温常压下,4.6g Na在O2中燃烧消耗O2的分子数为0.1 NA   |
| D.25℃时, pH=1的CH3COOH溶液中的H+数为0.1 NA |
您最近一年使用:0次
2018·福建漳州·二模
名校
5 . 下图是某学校实验室买回的硫酸试剂标签的部分内容。判断下列说法正确的是:


| A.该硫酸与等体积的水混合质量分数小于49% |
| B.配制200mL4.6mol.L-1的稀H2SO4需该H2SO4 50.0mL |
| C.该硫酸的浓度为9.2mol.L-1 |
| D.配制稀H2SO4时,往盛有浓H2SO4的烧杯中慢慢注入水,并不断搅拌 |
您最近一年使用:0次
10-11高一上·浙江宁波·期中
6 . 将标准状况下的a升氯化氢气体溶于1000克水中,得到的盐酸的密度为b克/毫升,则该盐酸的物质的量的浓度是
A. | B. | C.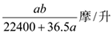 | D. |
您最近一年使用:0次
2019·安徽·一模
7 . 下图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此,下列说法不正确的是
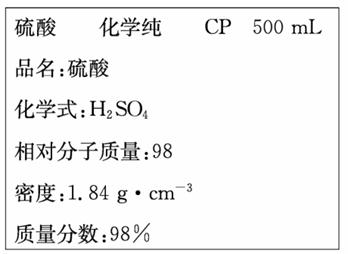

| A.该硫酸的物质的量浓度为18.4mol/L |
| B.1 mol Zn与足量的该硫酸反应,标准状况下产生22.4L气体时,转移的电子数为2NA |
| C.配制200mL4.6mol/L的稀硫酸需取该硫酸50 mL |
| D.该硫酸与等体积的水混合后所得溶液的物质的量浓度等于9.2mol/L |
您最近一年使用:0次



