名校
1 . 利用所学知识进行填空(用NA表示阿伏加德罗常数的值)。
(1)0.4mol氨气中含有NH3分子数是___________ ,其质量是___________ g。
(2)标准状况下,44.8LCH4对应的物质的量是___________ ,其电子数为___________ 。
(3)现有物质:①NaOH溶液;②铜;③熔融KHSO4;④BaCO3固体;⑤液态HCl;⑥CO2,以上物质中属于混合物的是___________  填序号
填序号 ,以上物质中属于电解质的
,以上物质中属于电解质的___________  填序号
填序号 ;以上物质中能导电的是
;以上物质中能导电的是___________  填序号
填序号 。
。
(4)现有CO与O2两种气态物质,试回答下列问题:
①同温同压下,CO与O2的密度之比为___________ 。
②相同温度和压强下,等质量的CO和O2.二者体积比为___________ 。
(5)将4gNaOH溶于水配成1L溶液,然后取出10mL,这10mL溶液的物质的量浓度为___________ 。
(6)18.6gNa2X含有0.6molNa+,则Na2X的物质的量是___________ ,Na2X的摩尔质量是___________ 。
(7)已知O2和CO2的混合气体,在标准状况下体积为11.2L,质量为18g,则混合气体的平均相对分子质量是___________ ,混合气体中O2和CO2物质的量之比为___________ 。
(1)0.4mol氨气中含有NH3分子数是
(2)标准状况下,44.8LCH4对应的物质的量是
(3)现有物质:①NaOH溶液;②铜;③熔融KHSO4;④BaCO3固体;⑤液态HCl;⑥CO2,以上物质中属于混合物的是
 填序号
填序号 ,以上物质中属于电解质的
,以上物质中属于电解质的 填序号
填序号 ;以上物质中能导电的是
;以上物质中能导电的是 填序号
填序号 。
。(4)现有CO与O2两种气态物质,试回答下列问题:
①同温同压下,CO与O2的密度之比为
②相同温度和压强下,等质量的CO和O2.二者体积比为
(5)将4gNaOH溶于水配成1L溶液,然后取出10mL,这10mL溶液的物质的量浓度为
(6)18.6gNa2X含有0.6molNa+,则Na2X的物质的量是
(7)已知O2和CO2的混合气体,在标准状况下体积为11.2L,质量为18g,则混合气体的平均相对分子质量是
您最近一年使用:0次
名校
2 . 下列有关叙述正确的是
A.标准状况下,等体积的 和 和 所含分子数相等 所含分子数相等 |
B.等物质的量的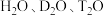 所含中子数相等 所含中子数相等 |
C. 和 和 分别与足量稀硫酸反应失去的电子数相等 分别与足量稀硫酸反应失去的电子数相等 |
D. 分别与足量 分别与足量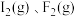 完全反应生成的HX(X为I或F)分子数相等 完全反应生成的HX(X为I或F)分子数相等 |
您最近一年使用:0次
2023-11-22更新
|
224次组卷
|
3卷引用:河南省驻马店市遂平县第一高级中学2023-2024学年高三上学期10月月考化学试题
名校
3 . 完成下列问题:
(1)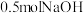 中含有离子的物质的量是
中含有离子的物质的量是_____  ,在
,在_____ 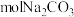 中所含
中所含 数目与上述
数目与上述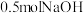 所含
所含 数目相等。
数目相等。
(2)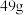 的
的 中含有
中含有_____  氧原子,能与
氧原子,能与_____  恰好完全反应。
恰好完全反应。
(3) 含
含 ,则
,则 的摩尔质量为
的摩尔质量为_____ , 的相对原子质量为
的相对原子质量为_____ ,含 的质共为
的质共为 的
的 ,其物质的量为
,其物质的量为_____ 。
(4)如图所示,气缸的总体积一定,内部被活塞隔成Ⅰ、Ⅱ两部分,活塞可以自由移动,也可以固定。 时向Ⅰ中充入
时向Ⅰ中充入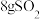 ,Ⅱ中充入
,Ⅱ中充入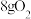 ,则当活塞不再移动时,Ⅰ、Ⅱ两部分体积比为
,则当活塞不再移动时,Ⅰ、Ⅱ两部分体积比为_____ 。

(5)某同学为了探究溶液的导电性与离子浓度的关系,做了如图实验,烧杯中为 溶液,滴定管是用于滴加
溶液,滴定管是用于滴加 溶液。若往烧杯中滴加少量
溶液。若往烧杯中滴加少量 溶液后,灯泡明亮程度有何变化?
溶液后,灯泡明亮程度有何变化?_____ 。

(1)
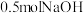 中含有离子的物质的量是
中含有离子的物质的量是 ,在
,在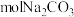 中所含
中所含 数目与上述
数目与上述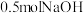 所含
所含 数目相等。
数目相等。(2)
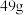 的
的 中含有
中含有 氧原子,能与
氧原子,能与 恰好完全反应。
恰好完全反应。(3)
 含
含 ,则
,则 的摩尔质量为
的摩尔质量为 的相对原子质量为
的相对原子质量为 的质共为
的质共为 的
的 ,其物质的量为
,其物质的量为(4)如图所示,气缸的总体积一定,内部被活塞隔成Ⅰ、Ⅱ两部分,活塞可以自由移动,也可以固定。
 时向Ⅰ中充入
时向Ⅰ中充入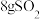 ,Ⅱ中充入
,Ⅱ中充入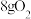 ,则当活塞不再移动时,Ⅰ、Ⅱ两部分体积比为
,则当活塞不再移动时,Ⅰ、Ⅱ两部分体积比为
(5)某同学为了探究溶液的导电性与离子浓度的关系,做了如图实验,烧杯中为
 溶液,滴定管是用于滴加
溶液,滴定管是用于滴加 溶液。若往烧杯中滴加少量
溶液。若往烧杯中滴加少量 溶液后,灯泡明亮程度有何变化?
溶液后,灯泡明亮程度有何变化?
您最近一年使用:0次
名校
4 . 过氧乙酸消毒液是一种常见的消毒剂,下图为实验室中过氧乙酸消毒液试剂瓶标签上的有关数据,下列说法错误的是
| 过氧乙酸消毒液 【化学式】 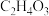 【规格】  【质量分数】15.2% 【密度】 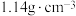 |
A. 个过氧乙酸分子中所含碳原子的物质的量为 个过氧乙酸分子中所含碳原子的物质的量为 |
B.过氧乙酸中C、H、O三种元素的质量之比为 |
C.过氧乙酸消毒液的物质的量的浓度为 |
D.该消毒液中过氧乙酸的物质的量为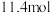 |
您最近一年使用:0次
名校
解题方法
5 . 物质的量是中学化学中常用的物理量。回答下列问题:
(1)0.2molH2SO4所含的分子数约为________ 个。
(2)________ molCO2中含有3g碳。
(3)含有相同氧原子数的CO与CO2的质量之比为________ 。
(4)工业炼铁的化学方程式为Fe2O3+3CO 2Fe+3CO2,反应若消耗1molFe2O3,理论上生成标准状况下
2Fe+3CO2,反应若消耗1molFe2O3,理论上生成标准状况下________ LCO2。
(5)阿莫西林(化学式为C16H19N3O5S,其相对分子质量为365)是常见的抗生素,是目前应用较为广泛的口服半合成青霉素之一,其结构简式如图所示。取7.3g阿莫西林(假设不含其余杂质)
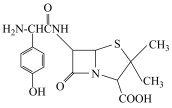
①7.3g阿莫西林的物质的量为________ 。
②阿莫西林中碳、氮元素的质量之比为________ 。
(6)分别向三个完全相同的恒容密闭容器中充入等质量的C2H4、CO、N2三种气体,当温度一定时,三个容器中气体压强之比为________ 。
(1)0.2molH2SO4所含的分子数约为
(2)
(3)含有相同氧原子数的CO与CO2的质量之比为
(4)工业炼铁的化学方程式为Fe2O3+3CO
 2Fe+3CO2,反应若消耗1molFe2O3,理论上生成标准状况下
2Fe+3CO2,反应若消耗1molFe2O3,理论上生成标准状况下(5)阿莫西林(化学式为C16H19N3O5S,其相对分子质量为365)是常见的抗生素,是目前应用较为广泛的口服半合成青霉素之一,其结构简式如图所示。取7.3g阿莫西林(假设不含其余杂质)

①7.3g阿莫西林的物质的量为
②阿莫西林中碳、氮元素的质量之比为
(6)分别向三个完全相同的恒容密闭容器中充入等质量的C2H4、CO、N2三种气体,当温度一定时,三个容器中气体压强之比为
您最近一年使用:0次
名校
6 . 回答系列问题。
(1)有下列物质:① 氢气;②
氢气;② 二氧化碳;③
二氧化碳;③ 个氯化氢分子。请回答(填序号):物质的量最大的是
个氯化氢分子。请回答(填序号):物质的量最大的是___________ ;含有原子个数最多的是___________ 。
(2)以下为中学化学中常见的几种物质:
①液氨;②熔融 ;③
;③ 固体;④铜;⑤
固体;④铜;⑤ 溶液;⑥乙醇;⑦澄清石灰水。
溶液;⑥乙醇;⑦澄清石灰水。
能导电的有___________ (填序号,下同);属于电解质有___________ ;焰色为黄色的有___________ ;写出③在溶液中的电离方程式___________ ;写出③和⑤混合反应的离子方程式___________ 。
(1)有下列物质:①
 氢气;②
氢气;② 二氧化碳;③
二氧化碳;③ 个氯化氢分子。请回答(填序号):物质的量最大的是
个氯化氢分子。请回答(填序号):物质的量最大的是(2)以下为中学化学中常见的几种物质:
①液氨;②熔融
 ;③
;③ 固体;④铜;⑤
固体;④铜;⑤ 溶液;⑥乙醇;⑦澄清石灰水。
溶液;⑥乙醇;⑦澄清石灰水。能导电的有
您最近一年使用:0次
7 . 下列有关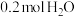 的说法正确的是
的说法正确的是
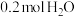 的说法正确的是
的说法正确的是| A.其相对分子质量和摩尔质量相同 | B.标准状况下,其体积是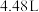 |
C.其质量是 | D.其含有的原子总数是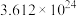 |
您最近一年使用:0次
8 . 下列叙述正确的是
A.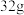 甲醇分子中含有 甲醇分子中含有 键的数目为 键的数目为 |
B.等质量的葡萄糖和乳酸[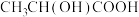 ]所含原子总数相等 ]所含原子总数相等 |
C.聚氯乙烯分子的平均摩尔质量为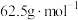 |
D.等物质的量的乙烷、丙酸在氧气中完全燃烧消耗 的分子数之比为1∶2 的分子数之比为1∶2 |
您最近一年使用:0次
9 . 科学研究发现氧元素能在一定条件下形成以亚稳态存在的分子四聚氧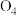 ,也能在一个大气压和-218.79℃以下形成红氧
,也能在一个大气压和-218.79℃以下形成红氧 ,判断以下说法正确的是
,判断以下说法正确的是
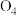 ,也能在一个大气压和-218.79℃以下形成红氧
,也能在一个大气压和-218.79℃以下形成红氧 ,判断以下说法正确的是
,判断以下说法正确的是A.等质量的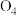 和 和 所含的原子个数后者多 所含的原子个数后者多 |
B.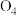 和 和 互为同分异构体 互为同分异构体 |
C.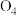 和 和 都含有非极性共价键 都含有非极性共价键 |
D.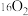 和 和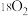 互为同位素 互为同位素 |
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
10 . 可用氢还原重量法测定产品的纯度,其原理为2RuCl3+3H2=2Ru+6HCl。某同学对产品纯度进行测定,所得数据记录如下:
则产品的纯度为_______ (用百分数表示,保留两位有效数字)。
| 实验序号 | 产品质量/g | 固体Ru质量/g |
| ① | 1.2500 | 0.4900 |
| ② | 1.2500 | 0.5100 |
| ③ | 1.2500 | 0.5000 |
您最近一年使用:0次



