1 . Ⅰ.按要求回答下列问题:
(1)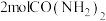 中含
中含__________ molH,所含氧原子跟__________  所含氧原子个数相等,它们所含氢原子数之比是
所含氧原子个数相等,它们所含氢原子数之比是__________ 。
(2)漳浦盐场是福建省第三大国有盐场,盐田面积达700万平方米,年产食盐5万多吨。漳州市海水水资源丰富,海水化学资源(主要为 和
和 及
及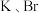 等元素)的利用具有非常广阔的前景。假设该海域海水中
等元素)的利用具有非常广阔的前景。假设该海域海水中 浓度
浓度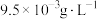 ,欲获得
,欲获得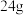 金属镁需要
金属镁需要__________ L海水。
Ⅱ.按要求写出下列化学用语:
(3)在考古上可通过测定某碳原子的同位素的比例,从而测算出它的年代,其微粒符号可表示为__________ 。
(4)最外层电子数是次外层电子数的3倍的原子,其原子结构示意图可表示为__________ 。
(5)某元素原子K层和M层电子总数等于其L层电子数,该元素符号为_________ 。
(1)
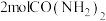 中含
中含 所含氧原子个数相等,它们所含氢原子数之比是
所含氧原子个数相等,它们所含氢原子数之比是(2)漳浦盐场是福建省第三大国有盐场,盐田面积达700万平方米,年产食盐5万多吨。漳州市海水水资源丰富,海水化学资源(主要为
 和
和 及
及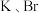 等元素)的利用具有非常广阔的前景。假设该海域海水中
等元素)的利用具有非常广阔的前景。假设该海域海水中 浓度
浓度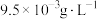 ,欲获得
,欲获得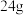 金属镁需要
金属镁需要Ⅱ.按要求写出下列化学用语:
(3)在考古上可通过测定某碳原子的同位素的比例,从而测算出它的年代,其微粒符号可表示为
(4)最外层电子数是次外层电子数的3倍的原子,其原子结构示意图可表示为
(5)某元素原子K层和M层电子总数等于其L层电子数,该元素符号为
您最近一年使用:0次
2024-04-04更新
|
24次组卷
|
2卷引用:福建省漳州市东山第二中学等校2023-2024学年高一上学期期中联考化学试题
2 . 以物质的量为中心的计算在高中化学学习中很重要。请完成下列题目。
(1)1gH2中含有_______ 个H。
(2)6.02×1023个CO2分子与16gO2,二者在标况下的体积之比_______ 。
(3)从2L0.5mol·L-1NaOH溶液中取出1L,则所取出的溶液中含NaOH的质量是_______ g。
(1)1gH2中含有
(2)6.02×1023个CO2分子与16gO2,二者在标况下的体积之比
(3)从2L0.5mol·L-1NaOH溶液中取出1L,则所取出的溶液中含NaOH的质量是
您最近一年使用:0次
名校
3 . 现有一瓶标准状况下的44.8 L HCl气体,回答下列各小题:
(1)所含HCl的物质的量是______ 。
(2)所含HCl的质量是_______ 。
(3)所含电子的数目是_______ 。(用NA表示)
(4)与_____ g NH3所含原子数相等。
(5)将所含的HCl全部溶于水配成1 L溶液,则c(Cl-)是______ ,与_____ mol/L的CuCl2溶液中的Cl-浓度相同。
(1)所含HCl的物质的量是
(2)所含HCl的质量是
(3)所含电子的数目是
(4)与
(5)将所含的HCl全部溶于水配成1 L溶液,则c(Cl-)是
您最近一年使用:0次
名校
4 . 物质的量是国际单位制中7个基本物理量之一、利用物质的量及其导出量可以大大简化相关的化学计算。
(1)标准状况下,与0.5molH3PO4含有相同数目氧原子的CO2气体的体积为___________ L。
(2)标准状况下,N2的密度为_______ g∙L-1;同温同体积下,相同质量的N2与O2的压强之比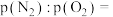
________ 。
(3)酸式(或碱式)滴定管是实验室常见的一种计量溶液体积的精确仪器。已知:从滴定管中滴出的25滴水即为1.00mL。若该实验条件下,水的密度为1 g∙cm-3,则滴定管滴出的半滴水中H2O分子数目为___________ (保留两位有效数字)。
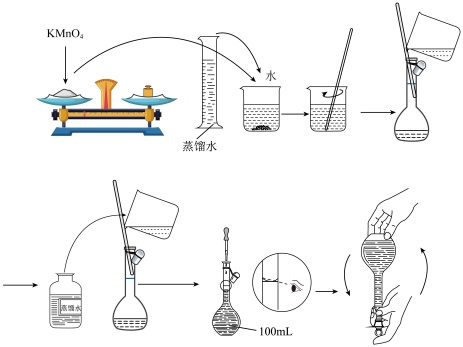
(4) KMnO4是一种重要的氧化剂,实验室若要配制100mL0.50mol∙L-1 KMnO4溶液,则需用托盘天平称取KMnO4固体质量为___________  ;其中确定100mL溶液体积的容器是
;其中确定100mL溶液体积的容器是___________ (填名称);若按照下图所示操作配制KMnO4溶液,则KMnO4溶液浓度将___________ (填“偏高、偏低或无影响”)。
(1)标准状况下,与0.5molH3PO4含有相同数目氧原子的CO2气体的体积为
(2)标准状况下,N2的密度为
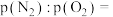
(3)酸式(或碱式)滴定管是实验室常见的一种计量溶液体积的精确仪器。已知:从滴定管中滴出的25滴水即为1.00mL。若该实验条件下,水的密度为1 g∙cm-3,则滴定管滴出的半滴水中H2O分子数目为
(4) KMnO4是一种重要的氧化剂,实验室若要配制100mL0.50mol∙L-1 KMnO4溶液,则需用托盘天平称取KMnO4固体质量为
 ;其中确定100mL溶液体积的容器是
;其中确定100mL溶液体积的容器是
您最近一年使用:0次
5 . 常温时,向两个均为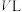 的恒容容器中分别充入
的恒容容器中分别充入 和
和 (如图所示),使得两容器内压强均为
(如图所示),使得两容器内压强均为 。分别比较两容器中的下列物理量,不正确的是
。分别比较两容器中的下列物理量,不正确的是
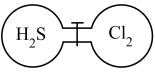
 的恒容容器中分别充入
的恒容容器中分别充入 和
和 (如图所示),使得两容器内压强均为
(如图所示),使得两容器内压强均为 。分别比较两容器中的下列物理量,不正确的是
。分别比较两容器中的下列物理量,不正确的是
| 选项 | A | B | C | D |
| 物理量 | 气体分子数 | 气体密度 | 气体质量 | 电子总数 |
| 结论 | 左=右 | 左<右 | 左<右 | 左>右 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 在49g硫酸中含有______ 个硫酸分子,中和这些硫酸需要氢氧化钠______ mol。
您最近一年使用:0次
名校
7 . 物质的量是高中化学常用的物理量,请完成以下问题:
(1)等质量的CO和 ,物质的量之比为
,物质的量之比为__________ ;氧原子个数之比为__________ 。
(2)同温同压下,同体积的 和A气体的质量分别为1.0g和16.0g,则A的摩尔质量为
和A气体的质量分别为1.0g和16.0g,则A的摩尔质量为__________ 。
(3)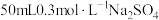 溶液和
溶液和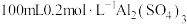 溶液混合后(混合体积变化忽略不计),溶液中
溶液混合后(混合体积变化忽略不计),溶液中 的物质的量浓度为
的物质的量浓度为__________ 。
(4)加热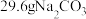 和
和 的混合物至质量不再变化,产生
的混合物至质量不再变化,产生 (标准状况下)1.12L(假设气体全部选出),试计算:混合物中
(标准状况下)1.12L(假设气体全部选出),试计算:混合物中 和
和 的物质的量之比为
的物质的量之比为__________ 。
(5)将18g铁铝合金投入足量NaOH溶液中,完全反应后生成2.24L氢气(标准状况),计算此铁铝合金中铝的质量分数。(假设合金中其他成分不与NaOH反应)__________ 。
(1)等质量的CO和
 ,物质的量之比为
,物质的量之比为(2)同温同压下,同体积的
 和A气体的质量分别为1.0g和16.0g,则A的摩尔质量为
和A气体的质量分别为1.0g和16.0g,则A的摩尔质量为(3)
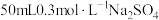 溶液和
溶液和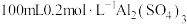 溶液混合后(混合体积变化忽略不计),溶液中
溶液混合后(混合体积变化忽略不计),溶液中 的物质的量浓度为
的物质的量浓度为(4)加热
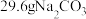 和
和 的混合物至质量不再变化,产生
的混合物至质量不再变化,产生 (标准状况下)1.12L(假设气体全部选出),试计算:混合物中
(标准状况下)1.12L(假设气体全部选出),试计算:混合物中 和
和 的物质的量之比为
的物质的量之比为(5)将18g铁铝合金投入足量NaOH溶液中,完全反应后生成2.24L氢气(标准状况),计算此铁铝合金中铝的质量分数。(假设合金中其他成分不与NaOH反应)
您最近一年使用:0次
名校
8 . 物质的量是联系宏观和微观的桥梁:
(1)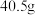 某金属氯化物
某金属氯化物 中含
中含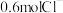 ,则该氯化物的摩尔质量为
,则该氯化物的摩尔质量为________ 。
(2)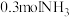 分子中所含原子数与
分子中所含原子数与________ 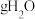 分子中所含原子数相等。
分子中所含原子数相等。
(3)由 两气体组成的混合气体
两气体组成的混合气体 ,标准状况下,体积为
,标准状况下,体积为 ,则
,则 的物质的量之比为
的物质的量之比为________ 。
(4)某溶液中只含有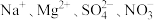 四种离子,已知前三种离子的个数比为2∶3∶1,则溶液中
四种离子,已知前三种离子的个数比为2∶3∶1,则溶液中 和
和 的离子个数比为
的离子个数比为________ 。
(5)碳酸铜和碱式碳酸铜【 】均能在高温下分解生成氧化铜。取一定量上述混合物充分煅烧后,剩余固体质量
】均能在高温下分解生成氧化铜。取一定量上述混合物充分煅烧后,剩余固体质量 。则溶解等质量的的上述混合物,需
。则溶解等质量的的上述混合物,需 硫酸
硫酸________  。
。
(1)
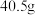 某金属氯化物
某金属氯化物 中含
中含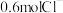 ,则该氯化物的摩尔质量为
,则该氯化物的摩尔质量为(2)
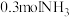 分子中所含原子数与
分子中所含原子数与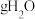 分子中所含原子数相等。
分子中所含原子数相等。(3)由
 两气体组成的混合气体
两气体组成的混合气体 ,标准状况下,体积为
,标准状况下,体积为 ,则
,则 的物质的量之比为
的物质的量之比为(4)某溶液中只含有
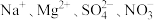 四种离子,已知前三种离子的个数比为2∶3∶1,则溶液中
四种离子,已知前三种离子的个数比为2∶3∶1,则溶液中 和
和 的离子个数比为
的离子个数比为(5)碳酸铜和碱式碳酸铜【
 】均能在高温下分解生成氧化铜。取一定量上述混合物充分煅烧后,剩余固体质量
】均能在高温下分解生成氧化铜。取一定量上述混合物充分煅烧后,剩余固体质量 。则溶解等质量的的上述混合物,需
。则溶解等质量的的上述混合物,需 硫酸
硫酸 。
。
您最近一年使用:0次
2023-12-12更新
|
57次组卷
|
2卷引用:福建省福州市福建师范大学附属中学2023-2024学年高一上学期期中考试化学试题
9 . 按要求完成下列题目。
(1)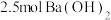 中约含有
中约含有_______ 个 。
。
(2)含 个
个 分子的
分子的 气体,在标准状况下其体积为
气体,在标准状况下其体积为_______ 。
(3)标准状况下,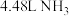 的质量为
的质量为_______ 。
(4)标准状况下,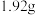 某气体的体积为
某气体的体积为 ,则此气体的相对分子质量为
,则此气体的相对分子质量为_______ 。
(5) 分子所含电子数为
分子所含电子数为_______ (用含 的值表示)。
的值表示)。
(6)标准状况下,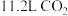 所含的质子数为
所含的质子数为_______ (用含 的值表示)。
的值表示)。
(7) 与足量的稀盐酸反应,失去的电子数目为
与足量的稀盐酸反应,失去的电子数目为_______ (用含 的值表示)。
的值表示)。
(8)同温同压下,等质量的 和
和 ,其体积比为
,其体积比为_______ 。
(9)某气体在标准状况下的密度为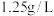 ,则
,则 该气体所含有的分子数为
该气体所含有的分子数为_______ 。
(10)同温同压下,A气体与 的相对密度是16,则A的摩尔质量为
的相对密度是16,则A的摩尔质量为_______ 。
(11)在一恒温恒容容器中,充入 与
与 ,两者恰好发生反应
,两者恰好发生反应 ,待冷却至室温时,反应前后体系中气体的压强比为
,待冷却至室温时,反应前后体系中气体的压强比为_______ 。
(12)在标准状况下 由
由 和
和 组成的混合气体,其质量为
组成的混合气体,其质量为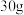 ,其中氧气的质量为
,其中氧气的质量为_______ 。
(1)
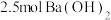 中约含有
中约含有 。
。(2)含
 个
个 分子的
分子的 气体,在标准状况下其体积为
气体,在标准状况下其体积为(3)标准状况下,
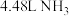 的质量为
的质量为(4)标准状况下,
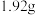 某气体的体积为
某气体的体积为 ,则此气体的相对分子质量为
,则此气体的相对分子质量为(5)
 分子所含电子数为
分子所含电子数为 的值表示)。
的值表示)。(6)标准状况下,
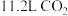 所含的质子数为
所含的质子数为 的值表示)。
的值表示)。(7)
 与足量的稀盐酸反应,失去的电子数目为
与足量的稀盐酸反应,失去的电子数目为 的值表示)。
的值表示)。(8)同温同压下,等质量的
 和
和 ,其体积比为
,其体积比为(9)某气体在标准状况下的密度为
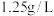 ,则
,则 该气体所含有的分子数为
该气体所含有的分子数为(10)同温同压下,A气体与
 的相对密度是16,则A的摩尔质量为
的相对密度是16,则A的摩尔质量为(11)在一恒温恒容容器中,充入
 与
与 ,两者恰好发生反应
,两者恰好发生反应 ,待冷却至室温时,反应前后体系中气体的压强比为
,待冷却至室温时,反应前后体系中气体的压强比为(12)在标准状况下
 由
由 和
和 组成的混合气体,其质量为
组成的混合气体,其质量为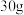 ,其中氧气的质量为
,其中氧气的质量为
您最近一年使用:0次
名校
10 . 利用所学知识进行填空(用NA表示阿伏加德罗常数的值)。
(1)0.4mol氨气中含有NH3分子数是___________ ,其质量是___________ g。
(2)标准状况下,44.8LCH4对应的物质的量是___________ ,其电子数为___________ 。
(3)现有物质:①NaOH溶液;②铜;③熔融KHSO4;④BaCO3固体;⑤液态HCl;⑥CO2,以上物质中属于混合物的是___________  填序号
填序号 ,以上物质中属于电解质的
,以上物质中属于电解质的___________  填序号
填序号 ;以上物质中能导电的是
;以上物质中能导电的是___________  填序号
填序号 。
。
(4)现有CO与O2两种气态物质,试回答下列问题:
①同温同压下,CO与O2的密度之比为___________ 。
②相同温度和压强下,等质量的CO和O2.二者体积比为___________ 。
(5)将4gNaOH溶于水配成1L溶液,然后取出10mL,这10mL溶液的物质的量浓度为___________ 。
(6)18.6gNa2X含有0.6molNa+,则Na2X的物质的量是___________ ,Na2X的摩尔质量是___________ 。
(7)已知O2和CO2的混合气体,在标准状况下体积为11.2L,质量为18g,则混合气体的平均相对分子质量是___________ ,混合气体中O2和CO2物质的量之比为___________ 。
(1)0.4mol氨气中含有NH3分子数是
(2)标准状况下,44.8LCH4对应的物质的量是
(3)现有物质:①NaOH溶液;②铜;③熔融KHSO4;④BaCO3固体;⑤液态HCl;⑥CO2,以上物质中属于混合物的是
 填序号
填序号 ,以上物质中属于电解质的
,以上物质中属于电解质的 填序号
填序号 ;以上物质中能导电的是
;以上物质中能导电的是 填序号
填序号 。
。(4)现有CO与O2两种气态物质,试回答下列问题:
①同温同压下,CO与O2的密度之比为
②相同温度和压强下,等质量的CO和O2.二者体积比为
(5)将4gNaOH溶于水配成1L溶液,然后取出10mL,这10mL溶液的物质的量浓度为
(6)18.6gNa2X含有0.6molNa+,则Na2X的物质的量是
(7)已知O2和CO2的混合气体,在标准状况下体积为11.2L,质量为18g,则混合气体的平均相对分子质量是
您最近一年使用:0次



