名校
解题方法
1 . 将100g25%的硝酸钾溶液稀释,取10g稀释后的溶液,经测定得知其溶质质量分数为10%,则稀释原溶液时所用水的质量是
| A.50g | B.100g | C.150g | D.200g |
您最近一年使用:0次
23-24高一上·浙江·期末
解题方法
2 . 下列对某些问题的认识正确的是
| A.98%的浓硫酸用等体积的水稀释后,硫酸的质量分数为49% |
| B.Na能与水反应,因此不能利用钠的置换反应制备其他金属单质X |
| C.纯碱属于盐,其水溶液不宜用带玻璃塞的玻璃瓶盛放 |
| D.铝合金、 不锈钢、足球烯(C60)都是重要的金属材料 |
您最近一年使用:0次
名校
解题方法
3 . 关于如图所示过程的说法正确的是
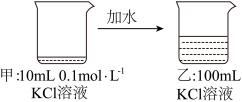

| A.甲比乙中溶质的质量分数小 | B.乙中 |
| C.乙比甲中KCl的溶解度大 | D.乙中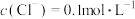 |
您最近一年使用:0次
2023-01-05更新
|
225次组卷
|
3卷引用:北京市东城区2022-2023学年高一上学期期末统一检测化学试卷
4 . 硫酸铁是水处理行业用作净水的混凝剂和污泥的处理剂,广泛用于水的处理。一种以黄铁矿烧渣(主要成分为 、
、 ,
, 等)为原料制取硫酸铁晶体的工艺流程如下:
等)为原料制取硫酸铁晶体的工艺流程如下:
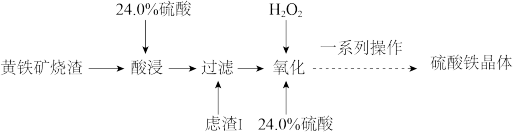
回答下列问题:
(1)“酸浸”前将黄铁矿烧渣粉碎的目的是___________ 。
(2)已知: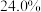 硫酸的密度
硫酸的密度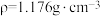 ,则
,则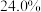 硫酸的物质的量浓度为
硫酸的物质的量浓度为___________ ;若实验室用 的浓硫酸配制
的浓硫酸配制 硫酸,则需用量筒量
硫酸,则需用量筒量 的浓硫酸的体积为
的浓硫酸的体积为___________  。
。
(3)在实验操作中常需要在加入 之前,对过滤后的滤液进行取样分析,取样分析的目的是
之前,对过滤后的滤液进行取样分析,取样分析的目的是___________ 。
(4)“酸浸”后过滤所得滤液中所含的阳离子有___________ (填离子符号)。
(5)“氧化”过程发生的反应的离子方程式为___________ ;“氧化”时可用硝酸代替氧化剂 ,优点是原料成本低,缺点是
,优点是原料成本低,缺点是___________ 。
(6)从“氧化”后的溶液中获得硫酸铁晶体,需经“一系列操作”,则“一系列操作”为___________ 、过滤洗涤、烘干。
 、
、 ,
, 等)为原料制取硫酸铁晶体的工艺流程如下:
等)为原料制取硫酸铁晶体的工艺流程如下:
回答下列问题:
(1)“酸浸”前将黄铁矿烧渣粉碎的目的是
(2)已知:
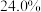 硫酸的密度
硫酸的密度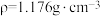 ,则
,则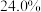 硫酸的物质的量浓度为
硫酸的物质的量浓度为 的浓硫酸配制
的浓硫酸配制 硫酸,则需用量筒量
硫酸,则需用量筒量 的浓硫酸的体积为
的浓硫酸的体积为 。
。(3)在实验操作中常需要在加入
 之前,对过滤后的滤液进行取样分析,取样分析的目的是
之前,对过滤后的滤液进行取样分析,取样分析的目的是(4)“酸浸”后过滤所得滤液中所含的阳离子有
(5)“氧化”过程发生的反应的离子方程式为
 ,优点是原料成本低,缺点是
,优点是原料成本低,缺点是(6)从“氧化”后的溶液中获得硫酸铁晶体,需经“一系列操作”,则“一系列操作”为
您最近一年使用:0次
名校
5 . 共和国勋章获得者钟南山院士强调,要注意疫情防控常态化,坚持做好日常消毒工作。常见的消毒剂有漂白粉、84消毒液(有效成分NaClO)、双氧水等。
Ⅰ.已知某“84消毒液”瓶体部分标签如下所示:84消毒液:(有效成分)NaClO;(规格)1000mL;(质量分数)25%;(密度)1.19g/cm3
(1)该“84消毒液”的物质的量浓度为_______  (计算结果保留两位有效数字)。
(计算结果保留两位有效数字)。
(2)“84消毒液”与“洁厕灵”(主要成分为盐酸)一起使用反而会弄巧成拙,产生有毒的气体,造成中毒事件。写出反应的离子方程式:_______ ;
(3)实验室用 的浓盐酸配制
的浓盐酸配制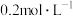 的盐酸240mL;得浓盐酸的体积为
的盐酸240mL;得浓盐酸的体积为_______ mL;使用的定量仪器有_______ 。
(4)84消毒液若与双氧水溶液混合减弱或失去杀菌消毒功能(反应产物之一是 ),解释原因
),解释原因_______ 。
Ⅱ.实验室制备84消毒液的装置如图1所示:
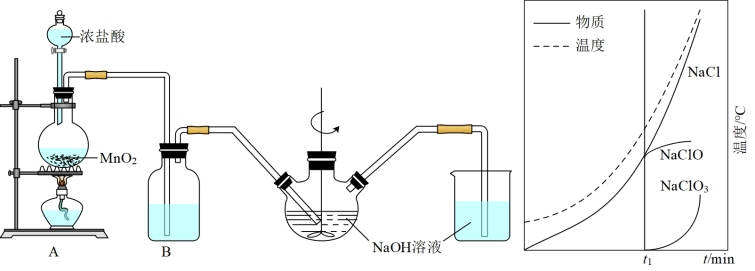
(5)装置B中盛放的试剂是_______ ;简述该装置对制取NaClO的作用_______ 。
(6)三颈烧瓶中生成各物质的物质的量和溶液的温度随时间的变化如图2所示。 分钟后所发生主要反应的化学方程式为
分钟后所发生主要反应的化学方程式为_______ 。
Ⅰ.已知某“84消毒液”瓶体部分标签如下所示:84消毒液:(有效成分)NaClO;(规格)1000mL;(质量分数)25%;(密度)1.19g/cm3
(1)该“84消毒液”的物质的量浓度为
 (计算结果保留两位有效数字)。
(计算结果保留两位有效数字)。(2)“84消毒液”与“洁厕灵”(主要成分为盐酸)一起使用反而会弄巧成拙,产生有毒的气体,造成中毒事件。写出反应的离子方程式:
(3)实验室用
 的浓盐酸配制
的浓盐酸配制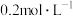 的盐酸240mL;得浓盐酸的体积为
的盐酸240mL;得浓盐酸的体积为(4)84消毒液若与双氧水溶液混合减弱或失去杀菌消毒功能(反应产物之一是
 ),解释原因
),解释原因Ⅱ.实验室制备84消毒液的装置如图1所示:

(5)装置B中盛放的试剂是
(6)三颈烧瓶中生成各物质的物质的量和溶液的温度随时间的变化如图2所示。
 分钟后所发生主要反应的化学方程式为
分钟后所发生主要反应的化学方程式为
您最近一年使用:0次
2022高一·上海·专题练习
名校
解题方法
6 . 现有1 L含SO3为30%的发烟硫酸(密度为1.95 g/cm3),要把它稀释成质量分数为95%的浓硫酸,需加水约为
| A.120 mL | B.180 mL | C.240 mL | D.300 mL |
您最近一年使用:0次
20-21高一下·浙江·阶段练习
解题方法
7 . 某种胃药的有效成分为碳酸钙,某实验小组为测定其中碳酸钙的含量,取10粒药片(0.1 g/粒)研碎后溶解。加入25.00 mL 1.0 mol/L的稀盐酸反应,最后用1.0 mol/LNaOH溶液中和过量的盐酸,测定所消耗的NaOH的溶液体积如下:
(1)配制100 mL 1.0 mol/L的稀盐酸,需要2.5 mol/L的盐酸的体积为___________ mL。
(2)药片中碳酸钙的质量分数为___________ 。
| 测定次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| V(NaOH)/mL | 13.00 | 12.90 | 11.40 | 13.10 |
(1)配制100 mL 1.0 mol/L的稀盐酸,需要2.5 mol/L的盐酸的体积为
(2)药片中碳酸钙的质量分数为
您最近一年使用:0次



