名校
解题方法
1 . 对下列图像与相关陈述对应的是
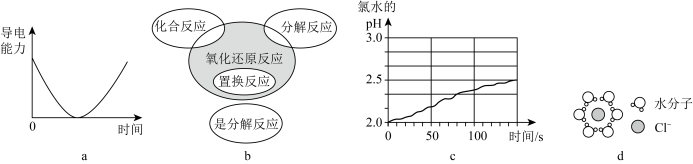
| A.图a:向稀硫酸中逐滴加入BaCl2溶液,混合液导电能力随时间变化的曲线 |
| B.图b:8Al+3Fe3O4 = 4Al2O3+9Fe的反应类型属于图中阴影部分 |
| C.图c:光照过程中氯水的pH随时间变化的曲线 |
| D.图d:NaCl固体溶解形成的水合氯离子示意图 |
您最近一年使用:0次
名校
解题方法
2 . 下列说法中正确的是
①硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物
②溶液,浊液,胶体的本质区别是分散质粒径大小
③蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质
④“嫦娥五号”卫星所用的碳纤维与石墨互为同素异形体
⑤“贵妃明镜剪青丝,后母戊鼎树丰碑”,后母戊鼎材料为青铜,其硬度比纯铜小
⑥榨苹果汁时加入维生素C,可减缓其在空气中发生颜色变化
①硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物
②溶液,浊液,胶体的本质区别是分散质粒径大小
③蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质
④“嫦娥五号”卫星所用的碳纤维与石墨互为同素异形体
⑤“贵妃明镜剪青丝,后母戊鼎树丰碑”,后母戊鼎材料为青铜,其硬度比纯铜小
⑥榨苹果汁时加入维生素C,可减缓其在空气中发生颜色变化
| A.3个 | B.4个 | C.5个 | D.6个 |
您最近一年使用:0次
3 . 化学中常用图象直观地描述化学反应的进程或结果。下列图象描述正确的是
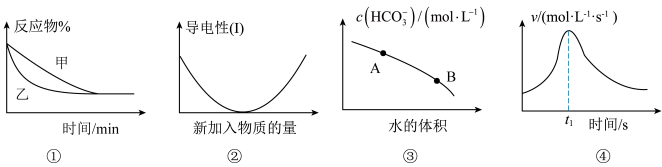
A.图①表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强大 3C(g)+D(s)的影响,乙的压强大 |
| B.图②可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 |
C.图③是在0.1mol⋅L﹣1的Na2CO3溶液中加水稀释,随着加入水的体积的增大,溶液中c( )的变化曲线,Na2CO3的水解程度:A点小于B点 )的变化曲线,Na2CO3的水解程度:A点小于B点 |
| D.图④是铁条与盐酸反应的反应速率随反应时间变化的曲线,t1时刻溶液的温度最高 |
您最近一年使用:0次
名校
解题方法
4 . 下列物质分类全部正确的组合是
分类组合 | 混合物 | 碱 | 电解质 | 碱性氧化物 |
A |
|
|
|
|
B | 盐酸 |
|
|
|
C | 镁铝合金 |
|
|
|
D | 矿泉水 |
| 稀硫酸 |
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 向某浓度的 溶液中,滴入稀
溶液中,滴入稀 ,溶液电导率随时间变化的曲线如图所示。下列分析正确的是
,溶液电导率随时间变化的曲线如图所示。下列分析正确的是

 溶液中,滴入稀
溶液中,滴入稀 ,溶液电导率随时间变化的曲线如图所示。下列分析正确的是
,溶液电导率随时间变化的曲线如图所示。下列分析正确的是
A. 溶液中存在的主要微粒有: 溶液中存在的主要微粒有: 、 、 、 、 |
B. 过程中发生的离子反应是: 过程中发生的离子反应是: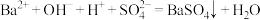 |
C. 过程中电导率增加是因为 过程中电导率增加是因为 是强电解质,会电离出 是强电解质,会电离出 和 和 |
D. 点时, 点时, 溶液与稀 溶液与稀 恰好反应 恰好反应 |
您最近一年使用:0次
6 . 以下实验的实验过程正确并可以达到实验目的的是
| 选项 | 实验目的 | 实验过程 |
| A | 探究 是否为电解质 是否为电解质 | 将一定量 通入蒸馏水中,测所得溶液是否导电 通入蒸馏水中,测所得溶液是否导电 |
| B | 探究 的氧化性 的氧化性 | 向盛有 稀溶液的试管中滴加3滴KI溶液,振荡后继续滴加2滴淀粉溶液,观察现象 稀溶液的试管中滴加3滴KI溶液,振荡后继续滴加2滴淀粉溶液,观察现象 |
| C | 制取纯净干燥的氢气 | 向稀盐酸中加入锌粒,将生成的气体依次通过NaOH溶液、浓硫酸和 溶液 溶液 |
| D | 配制浓度为 的 的 溶液 溶液 | 称取 固体 固体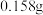 ,放入100mL容量瓶中,加水溶解并稀释至刻度 ,放入100mL容量瓶中,加水溶解并稀释至刻度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 . 下列化学表述正确的是
| A.国旗杆材料是高碳钢无缝钢管,属于金属材料 |
B.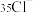 和 和 的离子结构示意图均可以表示为: 的离子结构示意图均可以表示为: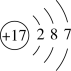 |
C.熔融状态下 的电离方程式: 的电离方程式: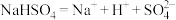 |
D. 还原 还原 反应中电子的转移: 反应中电子的转移: |
您最近一年使用:0次
名校
8 . 下列关于阿伏加德罗常数 的说法中正确的是
的说法中正确的是
 的说法中正确的是
的说法中正确的是A. 和足量水完全反应,转移电子数为 和足量水完全反应,转移电子数为 |
B.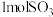 溶于足量水,所得溶液中 溶于足量水,所得溶液中 分子数为 分子数为 |
C. 乙烯 乙烯 和甲烷 和甲烷 的混合气中含有 的混合气中含有 键个数为 键个数为 |
D.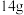 乙烯 乙烯 和丙烯 和丙烯 的混合气中,碳原子个数为 的混合气中,碳原子个数为 |
您最近一年使用:0次
名校
9 . 回答下列问题。
I.元素周期表是学习物质结构和性质的重要工具,如图是元素周期表的一部分,①⑧分别代表一种元素。回答下列问题:
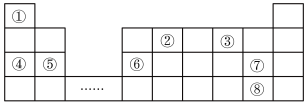
(1)元素②在元素周期表的位置为___________ ;元素②、③形成的化合物___________ (填“属于”或“不属于)电解质。
(2)元素①和③形成原子个数比为 的氢化物,写出它的电子式:
的氢化物,写出它的电子式:___________ 。
(3)元素③、⑤、⑦形成的简单离子半径由大到小的顺序为___________ (用离子符号填空)。
Ⅱ.氯气和漂白粉是现代工业和生活中常用的杀菌消毒剂,请回答下列问题:
实验室沿用舍勒的方法制取 ,反应停止后,实验小组检验烧瓶中还有
,反应停止后,实验小组检验烧瓶中还有 和盐酸。小组同学探究不继续产生
和盐酸。小组同学探究不继续产生 的原因。查阅资料表明,反应物或生成物浓度会影响氧化剂、还原剂的氧化性、还原性强弱。
的原因。查阅资料表明,反应物或生成物浓度会影响氧化剂、还原剂的氧化性、还原性强弱。
(4)【提出猜想】
猜想1: 降低,氧化剂
降低,氧化剂___________ (填化学式)氧化性减弱。
猜想2:___________ 减弱。
猜想3: 增大,氧化剂氧化性减弱。
增大,氧化剂氧化性减弱。
【实验过程】向反应后剩余物质中加入以下物质,请补充表格:
(5)利用氯气与潮湿的消石灰反应制取少量漂白粉。消石灰足量时,通入标准状况下 ,制得漂白粉中有效成分
,制得漂白粉中有效成分 的质量为
的质量为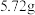 ,则
,则 制取
制取 的产率为
的产率为___________ 。
I.元素周期表是学习物质结构和性质的重要工具,如图是元素周期表的一部分,①⑧分别代表一种元素。回答下列问题:

(1)元素②在元素周期表的位置为
(2)元素①和③形成原子个数比为
 的氢化物,写出它的电子式:
的氢化物,写出它的电子式:(3)元素③、⑤、⑦形成的简单离子半径由大到小的顺序为
Ⅱ.氯气和漂白粉是现代工业和生活中常用的杀菌消毒剂,请回答下列问题:
实验室沿用舍勒的方法制取
 ,反应停止后,实验小组检验烧瓶中还有
,反应停止后,实验小组检验烧瓶中还有 和盐酸。小组同学探究不继续产生
和盐酸。小组同学探究不继续产生 的原因。查阅资料表明,反应物或生成物浓度会影响氧化剂、还原剂的氧化性、还原性强弱。
的原因。查阅资料表明,反应物或生成物浓度会影响氧化剂、还原剂的氧化性、还原性强弱。(4)【提出猜想】
猜想1:
 降低,氧化剂
降低,氧化剂猜想2:
猜想3:
 增大,氧化剂氧化性减弱。
增大,氧化剂氧化性减弱。【实验过程】向反应后剩余物质中加入以下物质,请补充表格:
| 序号 | 实验操作 | 有、无氯气 | 结论 |
| 1 | 加入浓硫酸, | 有氯气 | 猜想1正确 |
| 2 | 加入氯化钠固体,使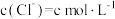 | 有氯气 | 猜想2正确 |
| 3 | 加入浓硫酸和 固体,使 固体,使 | 猜想3正确 |
(5)利用氯气与潮湿的消石灰反应制取少量漂白粉。消石灰足量时,通入标准状况下
 ,制得漂白粉中有效成分
,制得漂白粉中有效成分 的质量为
的质量为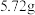 ,则
,则 制取
制取 的产率为
的产率为
您最近一年使用:0次
解题方法
10 . 下列物质属于非电解质的是
| A.CO2 | B.KI | C.NaOH | D.CH3COOH |
您最近一年使用:0次













