1 . 某小组在实验室探究 溶液与稀盐酸反应的实质。向0.2
溶液与稀盐酸反应的实质。向0.2
 溶液中滴加0.1
溶液中滴加0.1 盐酸,测定导电率的变化如图所示,回答下列问题:
盐酸,测定导电率的变化如图所示,回答下列问题:
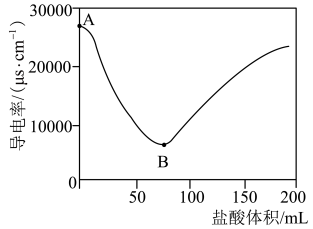
(1) 在水中以离子形式存在的实验证据是
在水中以离子形式存在的实验证据是___________ 。 的电离方程式为
的电离方程式为___________ 。
(2)A~B段反应的离子方程式为___________ 。
(3)B点恰好完全反应,此时溶液中存在的微粒有 、
、___________ 。
(4)下列化学反应的实质与 溶液与稀盐酸反应的实质相同的是
溶液与稀盐酸反应的实质相同的是___________ 。
A. 和
和 B.NaOH和
B.NaOH和 C.
C. 与
与
(5)与500mL该 溶液中
溶液中 含有相同原子数的HCl的质量为
含有相同原子数的HCl的质量为___________ 。
 溶液与稀盐酸反应的实质。向0.2
溶液与稀盐酸反应的实质。向0.2
 溶液中滴加0.1
溶液中滴加0.1 盐酸,测定导电率的变化如图所示,回答下列问题:
盐酸,测定导电率的变化如图所示,回答下列问题:
(1)
 在水中以离子形式存在的实验证据是
在水中以离子形式存在的实验证据是 的电离方程式为
的电离方程式为(2)A~B段反应的离子方程式为
(3)B点恰好完全反应,此时溶液中存在的微粒有
 、
、(4)下列化学反应的实质与
 溶液与稀盐酸反应的实质相同的是
溶液与稀盐酸反应的实质相同的是A.
 和
和 B.NaOH和
B.NaOH和 C.
C. 与
与
(5)与500mL该
 溶液中
溶液中 含有相同原子数的HCl的质量为
含有相同原子数的HCl的质量为
您最近一年使用:0次
名校
解题方法
2 . 离子反应是中学化学中重要的反应类型;离子方程式是用来表示离子反应的化学用语。
回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在___________(填标号)。
(2)从下列物质中选择合适反应物,按①~③的要求,各写出一个符合条件的离子方程式。
Na、Fe、 、
、 、HCl、
、HCl、 、NaOH、
、NaOH、 、
、 、
、
①只能表示一个具体的反应,不能代表同一类的离子反应:___________ 。
②不能表示为 的酸碱中和反应:
的酸碱中和反应:___________ 。
③难溶性的酸(碱或盐)不用画“↓”的离子反应:___________ 。
回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在___________(填标号)。
| A.单质 | B.化合物 | C.水 | D.电解质 |
Na、Fe、
 、
、 、HCl、
、HCl、 、NaOH、
、NaOH、 、
、 、
、
①只能表示一个具体的反应,不能代表同一类的离子反应:
②不能表示为
 的酸碱中和反应:
的酸碱中和反应:③难溶性的酸(碱或盐)不用画“↓”的离子反应:
您最近一年使用:0次
2022-12-17更新
|
190次组卷
|
2卷引用:山西省太原市外国语学校2021-2022学年高一上学期期中考试化学试题
3 . 四个试剂瓶中分别盛有 溶液、
溶液、 溶液、
溶液、 溶液和
溶液和 溶液,就如何检验这四种溶液分别做如下探究。
溶液,就如何检验这四种溶液分别做如下探究。
探究过程:分别取四种溶液各 于四支试管中,做下列实验。
于四支试管中,做下列实验。
(1)在四支试管中分别滴入稀硝酸,依据___________ 现象能检测出的物质是___________ 其离子方程式为___________ 。
(2)在剩余三支试管中分别滴入 溶液,依据
溶液,依据___________ 现象能检测出的物质是___________ ,其离子方程式为___________ 。
(3)在剩余两支试管中分别滴入___________ 溶液,依据___________ 现象能检测出的物质是___________ ,离子方程式为___________ 。
 溶液、
溶液、 溶液、
溶液、 溶液和
溶液和 溶液,就如何检验这四种溶液分别做如下探究。
溶液,就如何检验这四种溶液分别做如下探究。探究过程:分别取四种溶液各
 于四支试管中,做下列实验。
于四支试管中,做下列实验。(1)在四支试管中分别滴入稀硝酸,依据
(2)在剩余三支试管中分别滴入
 溶液,依据
溶液,依据(3)在剩余两支试管中分别滴入
您最近一年使用:0次
名校
4 . 离子反应与氧化还原反应在生活生产中用途广泛,请按要求完成方程式并配平。
(1)过氧化钠与二氧化碳反应的化学方程式__________________________ 。
(2)烧碱与小苏打溶液反应的化学方程式__________________ 。
(3)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打,能治疗胃酸过多,请写出其反应的离子方程式___________ ;如果病人同时患胃溃疡,为防止胃壁穿孔,此时其实最好服用含氢氧化铝的胃药(如胃舒平),写出该反应的离子方程式________________ 。
(4)离子的共存与溶液酸碱性密切相关。如S2-和SO32-在碱性条件下可以共存,但在酸性条件下,因反应生成淡黄色单质沉淀而不能大量共存。请写出S2-和SO32-在酸性环境中发生反应的离子方程式_____________________ 。
(5)高铁酸钠(Na2FeO4)有强氧化性,可以有效杀灭水中的细菌和病毒。已知湿法制备高铁酸钠的反应体系有六种微粒:Fe(OH)3、ClO-、H2O 、OH-、FeO42-、Cl-。写出制备高铁酸钠的离子方程式__________________________ 。
(1)过氧化钠与二氧化碳反应的化学方程式
(2)烧碱与小苏打溶液反应的化学方程式
(3)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打,能治疗胃酸过多,请写出其反应的离子方程式
(4)离子的共存与溶液酸碱性密切相关。如S2-和SO32-在碱性条件下可以共存,但在酸性条件下,因反应生成淡黄色单质沉淀而不能大量共存。请写出S2-和SO32-在酸性环境中发生反应的离子方程式
(5)高铁酸钠(Na2FeO4)有强氧化性,可以有效杀灭水中的细菌和病毒。已知湿法制备高铁酸钠的反应体系有六种微粒:Fe(OH)3、ClO-、H2O 、OH-、FeO42-、Cl-。写出制备高铁酸钠的离子方程式
您最近一年使用:0次
2019-12-16更新
|
95次组卷
|
2卷引用:山西省长治市第二中学2019-2020学年高一上学期12月月考化学试题
名校
解题方法
5 . 已知A和B两支试管的溶液中共含有K+、Ag+、Mg2+、Cl﹣、OH﹣、NO3﹣六种离子,向试管A的溶液中滴入酚酞试液呈红色.请回答下列问题:
(1)试管A的溶液中所含上述离子共有____ 种.
(2)若向某试管中滴入稀盐酸产生沉淀,则该试管为_____ (填“A”或“B”).
(3)若向试管B的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是_____ (填化学式).
(4)若向由试管A的溶液中阳离子组成的硫酸氢盐溶液中,滴入 Ba(OH)2溶液至溶液显中性,则发生反应的离子方程式为___________________________ .
(1)试管A的溶液中所含上述离子共有
(2)若向某试管中滴入稀盐酸产生沉淀,则该试管为
(3)若向试管B的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是
(4)若向由试管A的溶液中阳离子组成的硫酸氢盐溶液中,滴入 Ba(OH)2溶液至溶液显中性,则发生反应的离子方程式为
您最近一年使用:0次
解题方法
6 . 将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。
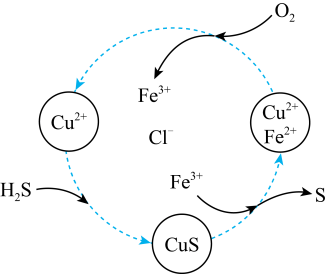
(1)写出CuCl2与H2S反应的离子方程式:_____ 。
(2)通过上述流程图的分析,整个流程的总反应为____ 。

(1)写出CuCl2与H2S反应的离子方程式:
(2)通过上述流程图的分析,整个流程的总反应为
您最近一年使用:0次
2019-09-17更新
|
1376次组卷
|
3卷引用:山西省河津市第二中学2022-2023学年高一上学期9月月考 化学试题
山西省河津市第二中学2022-2023学年高一上学期9月月考 化学试题第一章 章末检测(2)《高中新教材同步备课》(人教版 必修第一册)(已下线)第一章章末检测(1)——《高中新教材同步备课》(人教版 必修第一册)
11-12高一上·广东佛山·期中
7 . 某同学现要对一份废液中所含的离子作出一些判定。已知溶液中可能是含有SO42-、Na+、CO32-、HCO3—、H+、NO3-、Cu2+、Cl—等离子中的若干种。经观察知:溶液无色、澄清。然后他又作了如下的分析:
①取少量溶液,用PH试纸检验,得PH="1" 可知该溶液有强酸性
②重新取原溶液,用稀HCl 和BaCl2检验该溶液,有白色沉淀生成.
③将②所得的浊液静置,取上层清液,往清液中加入少量的AgNO3溶液和稀HNO3,结果又有白色沉淀生成
可得出结论:原溶液中一定有___________ 离子;一定没有______________ 离子;可能有__________ 离子
写出步骤②的离子反应方程式:_____________________________
写出步骤③的离子反应方程式:_____________________________
①取少量溶液,用PH试纸检验,得PH="1" 可知该溶液有强酸性
②重新取原溶液,用稀HCl 和BaCl2检验该溶液,有白色沉淀生成.
③将②所得的浊液静置,取上层清液,往清液中加入少量的AgNO3溶液和稀HNO3,结果又有白色沉淀生成
可得出结论:原溶液中一定有
写出步骤②的离子反应方程式:
写出步骤③的离子反应方程式:
您最近一年使用:0次
2016-12-08更新
|
907次组卷
|
4卷引用:山西省晋中市平遥县第二中学校2022-2023学年高一上学期10月月考化学试题
山西省晋中市平遥县第二中学校2022-2023学年高一上学期10月月考化学试题(已下线)2010—2011学年广东省佛山市南海一中高一上学期期中考试化学试卷湖南省衡阳县第四中学2019-2020学年高一(菁华班)10月月考化学试题(已下线)第14单元 物质的分离、提纯与检验(B卷 滚动提升检测)-2021年高考化学一轮复习单元滚动双测卷
8 . 某溶液中可能含有大量下列阴离子:OH-、SO42-、CO32-、Cl-。
(1)当溶液中存在大量H+时,则溶液中不可能有__________ 。
(2)当溶液中有大量的Ba2+存在时,则溶液中不可能有__________ 。
(1)当溶液中存在大量H+时,则溶液中不可能有
(2)当溶液中有大量的Ba2+存在时,则溶液中不可能有
您最近一年使用:0次



