1 . 下列实验操作与现象以及得出相关结论都正确的是
选项 | 操作与现象 | 结论 |
A | 取实验室存放的KI溶液少量于试管中,滴加淀粉溶液,变蓝 | KI已变质 |
B | 向某溶液中滴加 | 原溶液有 |
C | 向甲乙两支盛有硫代硫酸钠溶液的试管中分别滴加浓度均为3  溶液和 溶液和 溶液,甲未见浑浊,乙变浑浊 溶液,甲未见浑浊,乙变浑浊 | 增大 |
D | 向新制氯水中滴加紫色石蕊试液,溶液变红色 | HClO是弱酸 |
| A.A | B.B | C.C | D.D |
A. 通入品红溶液中,品红褪色 通入品红溶液中,品红褪色 |
| B.新制的氯水长期放置,溶液由黄绿色变为无色 |
C.将稀硫酸加入 溶液中,溶液由黄色变为橙色 溶液中,溶液由黄色变为橙色 |
D.将盛满 的密闭烧瓶浸入冰水中,气体红棕色变浅 的密闭烧瓶浸入冰水中,气体红棕色变浅 |
3 . 下列操作可行的是
| A.将未用完的小钠块直接扔入垃圾桶 | B.金属镁着火时用泡沫灭火器灭火 |
C.用 试纸测定氯水的 试纸测定氯水的 | D.在烧杯中做钠与水反应的实验 |
4 . 下列实验设计、现象和结论都正确的是
选项 | 实验 | 现象 | 结论 |
A | 将CO2通入BaCl2溶液中 | 有白色沉淀生成 | 白色沉淀是BaCO3 |
B | 向两支试管中各加入1 mL 1 mol/L的酸性KMnO4溶液,再向两支试管分别加入2 mL 1 mol/L的H2C2O4溶液和2mL0.5mol/L的H2C2O4溶液,记录高锰酸钾溶液褪色所需时间 | 1 mol/L的H2C2O4溶液中高锰酸钾溶液褪色快 | 浓度越大,反应速率越快 |
C | 向含AgCl和AgBr的饱和溶液中加入足量浓AgNO3溶液 | 产生两种颜色沉淀,但以白色为主 |
|
D | 向滴有酚酞的氨水中滴加氯水 | 溶液的红色褪去 | 氯水具有漂白性 |
| A.A | B.B | C.C | D.D |
| A.溶液的酸性和导电性均增强 |
| B.溶液的漂白性增强 |
| C.水、亚硫酸钠、氯水均为电解质 |
| D.向反应后的溶液中加入硝酸银溶液,产生白色沉淀,证明该溶液中存在氯离子 |

| A.氯水具有漂白性,能用作棉、麻和纸张的漂白剂 |
B.往氯水中滴加 溶液,会有白色沉淀生成 溶液,会有白色沉淀生成 |
| C.光照时,容器内氧气的体积分数会持续减小 |
| D.光照后的氯水的酸性强于新制氯水 |
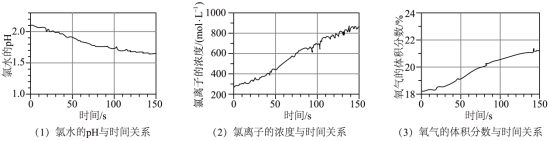
| A.图(1)说明强光照射下,氯水中H+浓度增加 |
| B.图(2)说明强光照射下,氯水中Cl-浓度增加 |
| C.图(3)说明强光照射下,氯水中有氧气生成 |
D.溶液中发生反应的化学方程式为2HClO 2H2O+Cl2↑ 2H2O+Cl2↑ |
8 . 把氯气溶于水得到黄绿色的溶液——氯水。
(1)写出
 与水反应的离子方程式:
与水反应的离子方程式:(2)分析下列性质与氯水中含有的哪种粒子有关(填化学式):
①黄绿色→
②漂白性→
③酸性→
④加入 溶液有沉淀生成→
溶液有沉淀生成→
(3)向该新制的氯水中加入紫色石蕊溶液,观察到的现象为:
(4)若把该氯水放在日光下照射足够长时间,再滴加石蕊溶液,现象为
| 选项 | 实验操作 | 现象 | 结论 |
| A | 分别测等物质的量浓度的 和 和 溶液的 溶液的 |  溶液使 溶液使 试纸呈现更深的颜色 试纸呈现更深的颜色 | 非金属性 |
| B | 铜与足量浓硫酸在加热条件下反应一段时间,冷却后,向反应后的溶液中慢慢倒入适量蒸馏水 | 溶液呈蓝色 | 铜与浓硫酸反应生成了硫酸铜 |
| C | 向KI溶液中持续滴加氯水 | 溶液先由无色变为棕黄色,一段时间后褪色 | 氯水具有氧化性和漂白性 |
| D | 灼烧铜丝使其表面变黑,伸入盛有某有机物的试管中 | 铜丝恢复亮红色 | 该有机物中可能有醇羟基或羧基 |
| A.A | B.B | C.C | D.D |
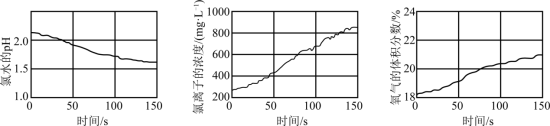
A.pH减小的主要原因是光照引起 逸出,溶液中 逸出,溶液中 浓度增大 浓度增大 |
| B.光照过程中,氧气的体积分数不断增大的原因是HClO分解生成氧气 |
| C.随着对氯水光照时间的延长,氯水的漂白性将增强 |
D.新制氯水中没有 ,光照过程中生成 ,光照过程中生成 |

 溶液,产生黑色沉淀
溶液,产生黑色沉淀 ,无
,无
 能加快反应
能加快反应


