1 . 氯气与水的反应为 。氯水具有多种性质,研究小组同学用氯水分别与紫色石蕊溶液,
。氯水具有多种性质,研究小组同学用氯水分别与紫色石蕊溶液, 溶液反应。请完成下列问题:
溶液反应。请完成下列问题:
(1)向紫色石蕊溶液中滴加氯水的现象是___________ ,证明氯水中含有的微粒有___________ 。
(2)向 溶液中滴加少量氯水,证明氯水有氧化性的实验方案是:取适量反应后溶液于试管中,
溶液中滴加少量氯水,证明氯水有氧化性的实验方案是:取适量反应后溶液于试管中,___________ ,则证明氯水具有氧化性。
(3)氯水光照时黄绿色会逐渐变浅直至消失,并产生无色气体,请用平衡理论解释黄绿色变浅的原因:________ 。
 。氯水具有多种性质,研究小组同学用氯水分别与紫色石蕊溶液,
。氯水具有多种性质,研究小组同学用氯水分别与紫色石蕊溶液, 溶液反应。请完成下列问题:
溶液反应。请完成下列问题:(1)向紫色石蕊溶液中滴加氯水的现象是
(2)向
 溶液中滴加少量氯水,证明氯水有氧化性的实验方案是:取适量反应后溶液于试管中,
溶液中滴加少量氯水,证明氯水有氧化性的实验方案是:取适量反应后溶液于试管中,(3)氯水光照时黄绿色会逐渐变浅直至消失,并产生无色气体,请用平衡理论解释黄绿色变浅的原因:
您最近一年使用:0次
名校
解题方法
2 . 由下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 新制氯水中滴入硝酸银溶液会产生白色沉淀 | 新制氯水中有氯离子 |
| B | 将湿润的蓝色石蕊试纸放入盛有干燥氯气的集气瓶内,石蕊试纸先变红后褪色 | 氯气具有漂白性 |
| C | 盛满氯气的试管倒扣在水槽中,静置一段时间,试管中液面上升一段距离,溶液呈浅黄绿色 | 氯气能与水反应 |
| D | 氯水中加入少量铁粉,溶液变为黄色 | 氯气能与铁粉反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 下列物质放置在敞口烧杯较长时间后,成分改变正确的是
| A | B | C | D | |
| 物质 | 84消毒液 | 漂白粉 | 氯水 | 钠 |
| 久置后 | 只含碳酸钠溶液 | 只含碳酸钙固体 | 稀盐酸溶液 | 氢氧化钠固体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 下列实验装置及实验结果合理的是
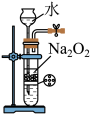 | 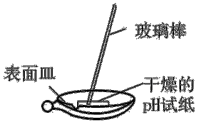 |
图1 | 图2 |
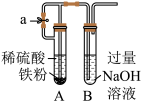 | 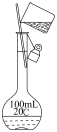 |
图3 | 图4 |
| A.实验室用图1所示装置制备少量氧气 |
| B.实验室用图2所示装置测定氯水的pH |
| C.实验室用图3所示装置制备少量Fe(OH)2,先打开止水夹a,一段时间后再关闭a |
| D.实验室用图4所示装置稀释浓硫酸 |
您最近一年使用:0次
名校
解题方法
5 . 由下列实验及现象不能推出相应结论的是
选项 | 实验 | 现象 | 结论 |
A | 向含有浓度相同的Na2S和NaCl的混合溶液中滴入少量AgNO3溶液 | 先产生黑色沉淀 | 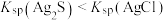 |
B | 某钾盐晶体中滴加浓盐酸,产生的气体通入品红溶液中 | 品红溶液褪色 | 产生的气体可能是Cl2 |
C | 将SO2通入Ca(ClO)2溶液 | 出现白色沉淀 | SO2是酸性氧化物 |
D | 向盛有CuO的试管中加入足量HI溶液,充分振荡后滴入3滴淀粉溶液 | 固体由黑色变为白色,溶液变为黄色,滴入淀粉后溶液变蓝 | HI既体现了还原性又体现了酸性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 氯及其化合物在生产生活中都有重要的用途,下列关于氯及其化合物说法正确的是
| A.自来水厂用Cl2消毒,是因为Cl2有毒 |
| B.Cl2因具有强氧化性,所以不能用钢瓶盛放 |
| C.可以将氯气通入氢氧化钠溶液中制得漂白粉 |
| D.ClO2可用于杀菌消毒 |
您最近一年使用:0次
7 . 下列图示的实验或操作正确的是
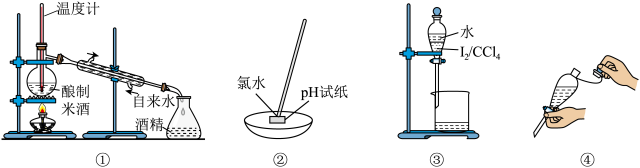

| A.酿制的米酒获取酒精用装置① | B.检测氯水的pH用装置② |
| C.分离出碘的CCl4溶液用装置③ | D.装置④是萃取振荡时放气 |
您最近一年使用:0次
8 . 验证次氯酸光照分解的产物可以设计成数字化实验(同时开始采集数据),此实验可以测定光照过程中氯水的pH、氯水中氯离子的浓度、广口瓶中氧气的体积分数的变化。三者变化趋势如图所示,回答下列问题:
(1)如图所示:
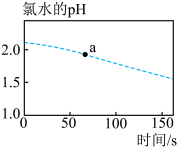
①新制氯水中所含微粒的种类有___________ 种。
②往a点对应的溶液中滴入淀粉碘化钾溶液,可能观察到的现象为___________ 。
③0~150s的过程中,氯水的pH逐渐减小的原因为___________ (用离子方程式表示)。
(2)如图所示:
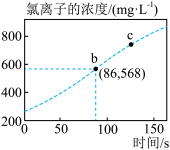
①b点对应的溶液中,所含氯离子的浓度为___________  。
。
②c点对应的溶液中,加入少量的 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为___________ 。
(3)如图所示:
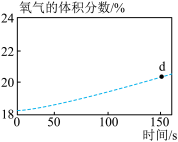
①写出一种 的用途:
的用途:___________ 。
②相同原子个数的 与
与 的质量之比为
的质量之比为___________ 。
③标准状况下,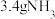 与
与___________ g 所含的电子总数相同。
所含的电子总数相同。
(1)如图所示:

①新制氯水中所含微粒的种类有
②往a点对应的溶液中滴入淀粉碘化钾溶液,可能观察到的现象为
③0~150s的过程中,氯水的pH逐渐减小的原因为
(2)如图所示:

①b点对应的溶液中,所含氯离子的浓度为
 。
。②c点对应的溶液中,加入少量的
 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为(3)如图所示:

①写出一种
 的用途:
的用途:②相同原子个数的
 与
与 的质量之比为
的质量之比为③标准状况下,
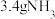 与
与 所含的电子总数相同。
所含的电子总数相同。
您最近一年使用:0次
9 . 有科学家提出,使用氯气对自来水消毒时,氯气会与水中、的有机物发生反应,生成的有机氯可能对人体有害,下列说法正确的是
A.常温下,氯气与水发生的反应为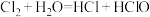 |
B.可用硝酸酸化的硝酸银来检验久置后的氯水中是否含有 |
C. 能使湿润的有色布条褪色,则氯气具有漂白性 能使湿润的有色布条褪色,则氯气具有漂白性 |
D.实验室制备氯气发生反应的化学方程式为 |
您最近一年使用:0次
解题方法
10 . Ⅰ.1810年,英国化学家戴维以大量事实为依据,确认一种黄绿色气体是一种新元素组成的单质——氯气。某化学兴趣小组同学利用装置A制取 ,其原理是
,其原理是 ,同时对氯气的性质进行探究。
,同时对氯气的性质进行探究。
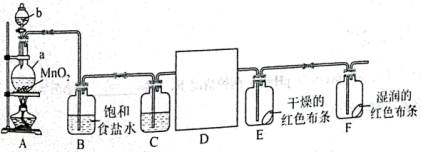
(1)仪器b的名称为_____________ 。某同学认为该实验装置存在一处明显的不足,其改进措施为___________ 。
(2)B中饱和食盐水的作用是_____________ 。根据氯气的性质D中的收集装置可以选择___________ (填序号)。

(3)下列有关该实验的说法中不正确的是______________________ (填字母)。
A. B装置中饱和食盐水可以用饱和碳酸氢钠代替
B. C中试剂是浓硫酸,目的是干燥氯气
C. E中红色布条不褪色,F中红色布条褪色证明氯气具有漂白性
(4)利用数字化实验探究次氯酸的化学性质,用强光照射盛有氯水的密闭广口瓶;并用传感器测定广口瓶中数据,得到如下图曲线。请用化学方程式解释曲线中氯离子的浓度和氧气体积分数变化的原因:______________________ 。
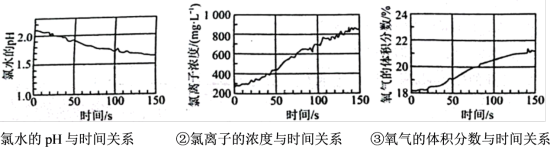
Ⅱ.新制氯水常用于杀菌消毒,在25℃时将氯气溶于水形成氯气-氯水体系,该体系中 (aq)、HClO和
(aq)、HClO和 的物质的量分数(
的物质的量分数( )随pH变化的关系如图所示。
)随pH变化的关系如图所示。
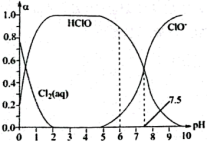
(5)由图分析,用氯气处理饮用水时,pH=6与pH=7.5两种情况下,pH=___________ 时杀菌效果强。当pH=7.5时,氯水中含氯元素的微粒有______________________ 。
 ,其原理是
,其原理是 ,同时对氯气的性质进行探究。
,同时对氯气的性质进行探究。
(1)仪器b的名称为
(2)B中饱和食盐水的作用是

(3)下列有关该实验的说法中不正确的是
A. B装置中饱和食盐水可以用饱和碳酸氢钠代替
B. C中试剂是浓硫酸,目的是干燥氯气
C. E中红色布条不褪色,F中红色布条褪色证明氯气具有漂白性
(4)利用数字化实验探究次氯酸的化学性质,用强光照射盛有氯水的密闭广口瓶;并用传感器测定广口瓶中数据,得到如下图曲线。请用化学方程式解释曲线中氯离子的浓度和氧气体积分数变化的原因:

Ⅱ.新制氯水常用于杀菌消毒,在25℃时将氯气溶于水形成氯气-氯水体系,该体系中
 (aq)、HClO和
(aq)、HClO和 的物质的量分数(
的物质的量分数( )随pH变化的关系如图所示。
)随pH变化的关系如图所示。
(5)由图分析,用氯气处理饮用水时,pH=6与pH=7.5两种情况下,pH=
您最近一年使用:0次



