1 . 海水中含有大量的卤族元素,具有十分巨大的开发利用潜力。
Ⅰ.向硫酸酸化的浓缩海水中通入 ,可获得含
,可获得含 的海水,
的海水,
(1)其反应的离子方程式为_______ ,由此可知氧化性:
_______  (填“>”或“<”)。
(填“>”或“<”)。
Ⅱ.氯是非常重要的非金属元素,如图是探究氯气性质和用途的实验装置。

(2)写出B中的化学反应方程式_______ 。
(3)该实验中设置装置C、D、E的主要目的是_______ ,与该实验目的直接相关的实验现象是_______ 。
(4)装置F可用于制漂白粉,漂白粉的有效成分是_______ (填化学式)。
(5)烧杯G的作用是_______ (用离子方程式表示)。
Ⅰ.向硫酸酸化的浓缩海水中通入
 ,可获得含
,可获得含 的海水,
的海水,(1)其反应的离子方程式为

 (填“>”或“<”)。
(填“>”或“<”)。Ⅱ.氯是非常重要的非金属元素,如图是探究氯气性质和用途的实验装置。

(2)写出B中的化学反应方程式
(3)该实验中设置装置C、D、E的主要目的是
(4)装置F可用于制漂白粉,漂白粉的有效成分是
(5)烧杯G的作用是
您最近一年使用:0次
2 . Cl2及其化合物在生产、生活中具有广泛的用途。
(1)25℃时将氯气溶于水形成氯气-氯水体系,该体系中Cl2(aq)、HClO和ClO-分别在三 者中所占分数(α)随pH变化的关系如图1所示:
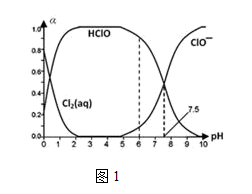
①已知HClO的杀菌能力比ClO-强,由图分析,用氯气处理饮用水时,pH=7.5与 pH=6时杀菌效果强的是_________________ 。
②氯气-氯水体系中,存在多个含氯元素的平衡关系,分别用平衡方程式表示为__________ 。
(2)ClO2是一种新的消毒剂,工业上可用Cl2氧化NaClO2溶液制取ClO2,写出该反应 的化学方程式_________________ 。
(3)工业上还可用下列方法制备ClO2,在80℃时电解氯化钠溶液得到NaClO3,然后与盐酸反应得到ClO2.电解时,NaClO3在______ 极(填阴或阳)生成,生成 的电极反应式为
的电极反应式为_________ 。
(4)一定条件下,在水溶液中 1mol Cl-、1mol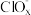 (x=1,2,3,4)的能量大小与化合价的关系如图2所示:
(x=1,2,3,4)的能量大小与化合价的关系如图2所示:

①从能量角度看,C、D、E中最不稳定的离子是_________________ (填离子符号)。
②B→A+D反应的热化学方程式为_________________ (用离子符号表示)。
(1)25℃时将氯气溶于水形成氯气-氯水体系,该体系中Cl2(aq)、HClO和ClO-分别在三 者中所占分数(α)随pH变化的关系如图1所示:

①已知HClO的杀菌能力比ClO-强,由图分析,用氯气处理饮用水时,pH=7.5与 pH=6时杀菌效果强的是
②氯气-氯水体系中,存在多个含氯元素的平衡关系,分别用平衡方程式表示为
(2)ClO2是一种新的消毒剂,工业上可用Cl2氧化NaClO2溶液制取ClO2,写出该反应 的化学方程式
(3)工业上还可用下列方法制备ClO2,在80℃时电解氯化钠溶液得到NaClO3,然后与盐酸反应得到ClO2.电解时,NaClO3在
 的电极反应式为
的电极反应式为(4)一定条件下,在水溶液中 1mol Cl-、1mol
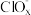 (x=1,2,3,4)的能量大小与化合价的关系如图2所示:
(x=1,2,3,4)的能量大小与化合价的关系如图2所示:
①从能量角度看,C、D、E中最不稳定的离子是
②B→A+D反应的热化学方程式为
您最近一年使用:0次
2019-01-30更新
|
225次组卷
|
6卷引用:2015届北京市石景山区高三上学期期末考试化学试卷



