名校
解题方法
1 . 某研究性学习小组利用下图装置制备漂白粉。
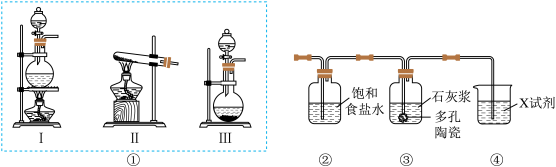
回答下列问题:
(1)若用二氧化锰和浓盐酸为原料制取氯气,则装置①应选用___________ (填“I”“Ⅱ”或“Ⅲ”),其反应的离子方程式为___________ 。
(2)装置②中饱和食盐水的作用是___________ ;装置④中的X试剂为___________ 。
(3)装置③中发生反应的化学方程式为___________ ;该反应是放热反应,反应温度较高时有副反应发生,为减少副反应发生可将装置③置于___________ (填“冷水浴”或“热水浴”)中进行反应。
(4)向装置①中加入200mL浓盐酸(密度为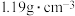 、质量分数为36.5%)与
、质量分数为36.5%)与 反应,产生了5.6L的氯气(已换算成标准状况下的体积)。该浓盐酸的物质的量浓度为
反应,产生了5.6L的氯气(已换算成标准状况下的体积)。该浓盐酸的物质的量浓度为___________ 。

回答下列问题:
(1)若用二氧化锰和浓盐酸为原料制取氯气,则装置①应选用
(2)装置②中饱和食盐水的作用是
(3)装置③中发生反应的化学方程式为
(4)向装置①中加入200mL浓盐酸(密度为
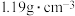 、质量分数为36.5%)与
、质量分数为36.5%)与 反应,产生了5.6L的氯气(已换算成标准状况下的体积)。该浓盐酸的物质的量浓度为
反应,产生了5.6L的氯气(已换算成标准状况下的体积)。该浓盐酸的物质的量浓度为
您最近一年使用:0次
名校
2 . 用NA表示阿伏伽德罗常数,下列说法中正确的有
A.若Cl2与足量NaOH的溶液反应生成 0.1 mol,则生成的 0.1 mol,则生成的 数目为0.2NA 数目为0.2NA |
| B.常温常压下,17 g NH3的体积约为22.4L |
| C.1 mol/L的CaCl2溶液中含Cl-的数目为2NA |
| D.在50g质量分数为46%的乙醇水溶液中,含氢原子总数为6NA |
您最近一年使用:0次
2023-10-09更新
|
92次组卷
|
2卷引用:河南省郑州市第四高级中学2023-2024学年高一上学期第一次月考化学试题
解题方法
3 . 根据要求回答下列问题:
(1)amol单质碳和16g氧气恰好在某恒容密闭容器中发生反应: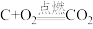 、
、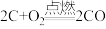 ,当恢复到原来的温度时,测得容器内的压强增大了0.5倍(忽略固体对压强的影响)。
,当恢复到原来的温度时,测得容器内的压强增大了0.5倍(忽略固体对压强的影响)。
①a=_______ ;16g氧气的体积为_______ L(标准状况下)
②若将反应后的气体通过盛有足量Na2O2的U形管,发生反应的化学方程式为_______ 。
(2)二氧化氯(ClO2)是一种广谱杀菌消毒剂。某工厂以213gNaClO3固体、117gNaCl固体和876g一定溶质质量分数的稀硫酸为原料制取ClO2,反应的化学方程式为2NaClO3+2NaCl+2H2SO4=2ClO2 +Cl2↑+2H2O+2Na2SO4,假设反应物均恰好完全反应。
+Cl2↑+2H2O+2Na2SO4,假设反应物均恰好完全反应。
①NaClO2中Cl的化合价是_______
②“84消毒液”也是一种含氯消毒剂,写出实验室制备“84消毒液”的化学方程式:_______
③876g稀硫酸中H2SO4的质量分数是_______ %(结果保留1位小数)。
④30℃时,将所得的硫酸钠溶液蒸发掉_______ g水可以恰好形成该温度下的饱和溶液(已知:30℃时,Na2SO4的溶解度为40g)。
(1)amol单质碳和16g氧气恰好在某恒容密闭容器中发生反应:
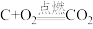 、
、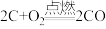 ,当恢复到原来的温度时,测得容器内的压强增大了0.5倍(忽略固体对压强的影响)。
,当恢复到原来的温度时,测得容器内的压强增大了0.5倍(忽略固体对压强的影响)。①a=
②若将反应后的气体通过盛有足量Na2O2的U形管,发生反应的化学方程式为
(2)二氧化氯(ClO2)是一种广谱杀菌消毒剂。某工厂以213gNaClO3固体、117gNaCl固体和876g一定溶质质量分数的稀硫酸为原料制取ClO2,反应的化学方程式为2NaClO3+2NaCl+2H2SO4=2ClO2
 +Cl2↑+2H2O+2Na2SO4,假设反应物均恰好完全反应。
+Cl2↑+2H2O+2Na2SO4,假设反应物均恰好完全反应。①NaClO2中Cl的化合价是
②“84消毒液”也是一种含氯消毒剂,写出实验室制备“84消毒液”的化学方程式:
③876g稀硫酸中H2SO4的质量分数是
④30℃时,将所得的硫酸钠溶液蒸发掉
您最近一年使用:0次
4 . 短周期A、B、C、D、E、F六种元素,它们的原子序数由A到F依次增大。在周期表中,A的原子半径最小。B元素的原子最外层电子数是内层电子数的两倍,C为地壳中含量最多的元素,D是原子半径最大的短周期主族元素,D的单质在高温下与C的单质充分反应,可以得到与E单质颜色相同的淡黄色固态化合物。D与F形成的化合物DF是常用的调味品。试根据以上叙述回答:
(1)写出下列元素名称:A_______ ,B_______ ,C_______ ,D_______ 。
(2)E在元素周期表中的位置:_______ 。
(3)F的离子结构示意图:_______ 。
(4)B、C、D的原子半径由大到小的顺序是_______ 。(用元素符号表示)
(5)C、D按原子个数比1∶1组成的一种化合物与水发生反应的化学方程式为_______ 。
(6)D单质制备漂白液的化学反应方程式_______ 。
(1)写出下列元素名称:A
(2)E在元素周期表中的位置:
(3)F的离子结构示意图:
(4)B、C、D的原子半径由大到小的顺序是
(5)C、D按原子个数比1∶1组成的一种化合物与水发生反应的化学方程式为
(6)D单质制备漂白液的化学反应方程式
您最近一年使用:0次
2023-03-07更新
|
138次组卷
|
2卷引用:河南省郑州市六校联盟2022-2023学年高一下学期4月期中考试化学试题
5 . 某化学小组同学在学习Cl2的实验室制法后,发现用加热浓盐酸与MnO2混合物的方法制Cl2既浪费能源又不易控制温度,他们现欲对该实验进行改进并验证Cl2的部分性质,进行了如下探究活动。
查阅资料:KMnO4和KClO3的氧化性都比MnO2强,在不加热的条件下即可与浓盐酸发生反应,从而实现制取Cl2的目的。
(1)确定反应原理:___________
(2)选择实验装置:现有如图所示的装置,可以选择其中的___________ (填序号)进行实验。
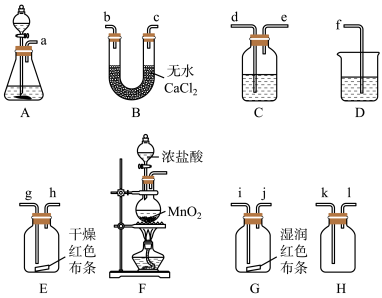
(3)装置的正确连接顺序为___________ (用小写字母序号表示)。
(4)①实验时C中所装液体是___________ 。
②在制氯气前,必须进行的一项操作是___________ 。
③D中所装试剂是___________ ,发生反应的离子方程式是___________ 。
(5)有一种“地康法”制取氯气的反应原理如图所示:

①反应I属于___________ 反应(填四种基本反应类型之一)
②在450℃条件下,反应II的化学方程式为___________
③工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:3Cl2+____ =_____ +N2
查阅资料:KMnO4和KClO3的氧化性都比MnO2强,在不加热的条件下即可与浓盐酸发生反应,从而实现制取Cl2的目的。
(1)确定反应原理:
(2)选择实验装置:现有如图所示的装置,可以选择其中的

(3)装置的正确连接顺序为
(4)①实验时C中所装液体是
②在制氯气前,必须进行的一项操作是
③D中所装试剂是
(5)有一种“地康法”制取氯气的反应原理如图所示:

①反应I属于
②在450℃条件下,反应II的化学方程式为
③工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:3Cl2+
您最近一年使用:0次
2022-03-17更新
|
86次组卷
|
2卷引用:河南省顶级名校2023-2024学年高一上学期12月月考化学试题



