解题方法
1 . 某同学利用如图实验装置制备少量的漂白粉。回答下列问题:
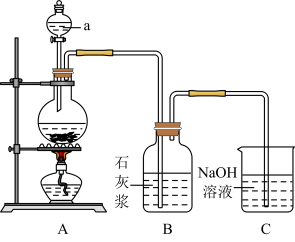
(1)漂白粉的有效成分是__________ (填名称);
(2)仪器a的名称是__________ 。装置A为实验室制取氯气的装置,其发生的化学方式为_______________ ;
(3)装置B中反应放热会使体系温度升高,导致氯气和石灰浆发生副反应产生Ca(ClO3)2,该副反应的化学方程式为______________ ;
(4)装置C的作用_________ ,装置C中发生反应的离子方程式为________ 。

(1)漂白粉的有效成分是
(2)仪器a的名称是
(3)装置B中反应放热会使体系温度升高,导致氯气和石灰浆发生副反应产生Ca(ClO3)2,该副反应的化学方程式为
(4)装置C的作用
您最近半年使用:0次
解题方法
2 . 下列关于氯气及含氯化合物的叙述中正确的是
| A.可以用向下排空气法收集少量的氯气 |
| B.氯气可以溶于水,但是不能与水发生化学反应 |
| C.在加热的条件下,过量的铁与氯气反应生成氯化铁 |
| D.氯气与氢氧化钠溶液反应时只做氧化剂 |
您最近半年使用:0次
3 . 实验室用浓盐酸和 制
制 ,并以干燥的
,并以干燥的 为原料制备无水
为原料制备无水 。已知
。已知 易升华,易吸收水分而潮解。装置如下图所示。
易升华,易吸收水分而潮解。装置如下图所示。

(1)装置A中发生的化学方程式为__________ ,装置B、C中应盛放的试剂名称为__________ 。
(2)从A装置导出的气体若不经过B、C装置而直接进入D管,将对实验产生的不良后果是__________ 。
(3)实验时,先点燃__________ 处的酒精灯,其目的是__________ ,写出D中反应的化学方程式:__________ 。
(4)F装置所起的作用是__________ 和防止空气中的水蒸气进入E中。
(5)生产84消毒液是将氯气通入NaOH溶液中,发生反应的离子方程式为__________ 。
(6)84消毒液稀释后喷洒在空气中,可以生成有漂白性的物质,请写出此过程的化学方程式:__________ 。
 制
制 ,并以干燥的
,并以干燥的 为原料制备无水
为原料制备无水 。已知
。已知 易升华,易吸收水分而潮解。装置如下图所示。
易升华,易吸收水分而潮解。装置如下图所示。
(1)装置A中发生的化学方程式为
(2)从A装置导出的气体若不经过B、C装置而直接进入D管,将对实验产生的不良后果是
(3)实验时,先点燃
(4)F装置所起的作用是
(5)生产84消毒液是将氯气通入NaOH溶液中,发生反应的离子方程式为
(6)84消毒液稀释后喷洒在空气中,可以生成有漂白性的物质,请写出此过程的化学方程式:
您最近半年使用:0次
解题方法
4 . 氯气制取84消毒液反应方程式:____________ 。
您最近半年使用:0次
5 . 氯气的实验室制法
(1)反应原理:实验室用 和浓盐酸加热反应制取
和浓盐酸加热反应制取 。反应的化学方程式为
。反应的化学方程式为___________ 。
(2)实验装置如下图:

发生装置盛放反应试剂的仪器的名称:A___________ 、B___________ 。
(3)气体的净化装置:饱和食盐水的作用为___________ ;浓硫酸的作用为___________ 。
(4)尾气处理装置;NaOH溶液的作用为___________ ,相关离子方程式为___________ 。
(1)反应原理:实验室用
 和浓盐酸加热反应制取
和浓盐酸加热反应制取 。反应的化学方程式为
。反应的化学方程式为(2)实验装置如下图:

发生装置盛放反应试剂的仪器的名称:A
(3)气体的净化装置:饱和食盐水的作用为
(4)尾气处理装置;NaOH溶液的作用为
您最近半年使用:0次
6 . 写出下列反应中转移的电子数目。
(1)1molCl2和NaOH反应转移电子数_______ 。
(2)3molNO2和H2O反应转移电子数_______ 。
(1)1molCl2和NaOH反应转移电子数
(2)3molNO2和H2O反应转移电子数
您最近半年使用:0次
解题方法
7 . 写出下列物质的主要成分
①漂白粉:___________ ②“84”消毒液:___________
③漂白液:___________ ④洁厕灵:___________
①漂白粉:
③漂白液:
您最近半年使用:0次
8 . 将 通入含amolNaOH的溶液中,反应会放热,温度升高后发生反应:
通入含amolNaOH的溶液中,反应会放热,温度升高后发生反应: 。当
。当 完全反应时,下列说法正确的是
完全反应时,下列说法正确的是
 通入含amolNaOH的溶液中,反应会放热,温度升高后发生反应:
通入含amolNaOH的溶液中,反应会放热,温度升高后发生反应: 。当
。当 完全反应时,下列说法正确的是
完全反应时,下列说法正确的是A.反应中作氧化剂的 有 有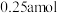 |
B.若反应后溶液中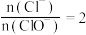 ,则 ,则 |
C. 与 与 的物质的量之和可能为 的物质的量之和可能为 |
D.反应中转移电子的物质的量可能为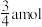 |
您最近半年使用:0次
名校
解题方法
9 . 用久置于空气中的生石灰【主要成分为 ,还含有
,还含有 、
、 和某些难溶物】制取
和某些难溶物】制取 的流程如下图所示。下列有关说法不正确的是
的流程如下图所示。下列有关说法不正确的是

 ,还含有
,还含有 、
、 和某些难溶物】制取
和某些难溶物】制取 的流程如下图所示。下列有关说法不正确的是
的流程如下图所示。下列有关说法不正确的是
| A.“打浆”的目的是为了提高“氯化”时的反应速率 |
B.“氯化”中主要发生的反应为: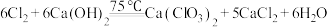 |
C.氯化中通入过量的 ,“过滤”后的滤渣中主要为 ,“过滤”后的滤渣中主要为 |
D.“转化”时发生的化学反应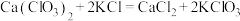 不属于氧化还原反应 不属于氧化还原反应 |
您最近半年使用:0次
名校
解题方法
10 . 某研究性学习小组利用下图装置制备漂白粉。
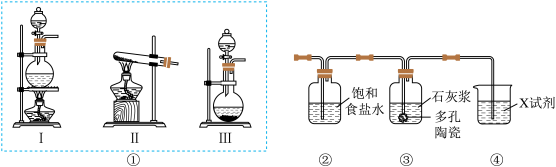
回答下列问题:
(1)若用二氧化锰和浓盐酸为原料制取氯气,则装置①应选用___________ (填“I”“Ⅱ”或“Ⅲ”),其反应的离子方程式为___________ 。
(2)装置②中饱和食盐水的作用是___________ ;装置④中的X试剂为___________ 。
(3)装置③中发生反应的化学方程式为___________ ;该反应是放热反应,反应温度较高时有副反应发生,为减少副反应发生可将装置③置于___________ (填“冷水浴”或“热水浴”)中进行反应。
(4)向装置①中加入200mL浓盐酸(密度为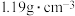 、质量分数为36.5%)与
、质量分数为36.5%)与 反应,产生了5.6L的氯气(已换算成标准状况下的体积)。该浓盐酸的物质的量浓度为
反应,产生了5.6L的氯气(已换算成标准状况下的体积)。该浓盐酸的物质的量浓度为___________ 。

回答下列问题:
(1)若用二氧化锰和浓盐酸为原料制取氯气,则装置①应选用
(2)装置②中饱和食盐水的作用是
(3)装置③中发生反应的化学方程式为
(4)向装置①中加入200mL浓盐酸(密度为
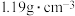 、质量分数为36.5%)与
、质量分数为36.5%)与 反应,产生了5.6L的氯气(已换算成标准状况下的体积)。该浓盐酸的物质的量浓度为
反应,产生了5.6L的氯气(已换算成标准状况下的体积)。该浓盐酸的物质的量浓度为
您最近半年使用:0次



