解题方法
1 . 氯气制取84消毒液反应方程式:____________ 。
您最近一年使用:0次
2 . 写出下列反应中转移的电子数目。
(1)1molCl2和NaOH反应转移电子数_______ 。
(2)3molNO2和H2O反应转移电子数_______ 。
(1)1molCl2和NaOH反应转移电子数
(2)3molNO2和H2O反应转移电子数
您最近一年使用:0次
解题方法
3 . 写出下列物质的主要成分
①漂白粉:___________ ②“84”消毒液:___________
③漂白液:___________ ④洁厕灵:___________
①漂白粉:
③漂白液:
您最近一年使用:0次
4 . 微型实验可节约药品,因而在中学化学教学中应用广泛。下图为实验室制备 并探究
并探究 是否具有漂白性的实验。下列说法正确的是
是否具有漂白性的实验。下列说法正确的是 (浓)
(浓)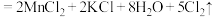 。
。
②白色干棉花球中有 粉末,主要作用是干燥气体。
粉末,主要作用是干燥气体。
 并探究
并探究 是否具有漂白性的实验。下列说法正确的是
是否具有漂白性的实验。下列说法正确的是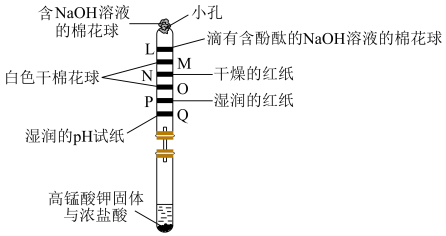
 (浓)
(浓)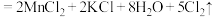 。
。②白色干棉花球中有
 粉末,主要作用是干燥气体。
粉末,主要作用是干燥气体。| A.Q处pH试纸变红且颜色一直保持不变 | B.P处红纸逐渐褪色,表明氯气具有漂白性 |
| C.N处红纸不变色 | D.向褪色后的L处棉花球滴入盐酸,红色重现 |
您最近一年使用:0次
2024-01-18更新
|
222次组卷
|
3卷引用:河南省洛阳市宜阳县第一高级中学2023-2024学年高一上学期(研学班)期末考试化学试卷
名校
解题方法
5 . 某实验小组使用 与浓盐酸制备并收集少量
与浓盐酸制备并收集少量 ,实验装置如下所示:
,实验装置如下所示:

(1)实验室常用二氧化锰与浓盐酸制取氯气写出该反应的化学方程式:_______ 。
(2)在实验过程中,装置C的作用为_______ ,装置D中观察到的现象是_______ 。
(3)小组成员观察到装置E中的现象:_______ ,根据实验现象小明同学设计了如下图的实验研究氯气是否具有漂白性。已知通入的氯气中含有空气和水蒸气,浓硫酸用于吸收氯气中的水蒸气。回答下列问题:
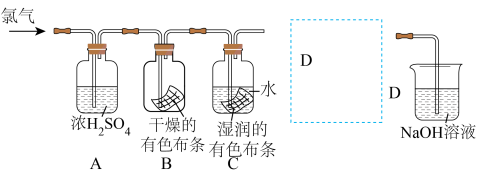
①实验现象:B中布条_______ ,C中布条_______ (填“褪色”或“不褪色”),写出相关的化学方程式:_______ 。
②写出D中反应的离子方程式:_______ ,若有标况下22.4L氯气与500mLNaOH溶液恰好完全反应,则NaOH溶液中溶质的物质的量浓度为_______ 。
 与浓盐酸制备并收集少量
与浓盐酸制备并收集少量 ,实验装置如下所示:
,实验装置如下所示:
(1)实验室常用二氧化锰与浓盐酸制取氯气写出该反应的化学方程式:
(2)在实验过程中,装置C的作用为
(3)小组成员观察到装置E中的现象:

①实验现象:B中布条
②写出D中反应的离子方程式:
您最近一年使用:0次
6 . 氯及其化合物在生活中应用广泛。如图是一些含氯产品
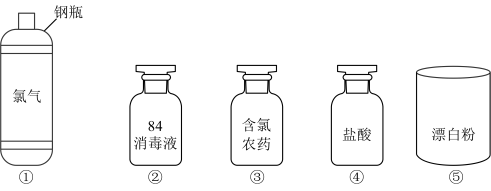
请回答下列问题:
(1)84消毒液的有效成分是次氯酸钠,从物质的分类上看,次氯酸钠属于___________ (填序号)
A.酸 B.碱 C.盐 D.非电解质 E.电解质 F.弱电解质
(2)如果发生了氯气泄漏,以下自救方法得当的是___________(填序号)。
(3)使用84消毒液漂白衣物时,在空气中放置一段时间,漂白效果更好,原因是________ ;
(4)将氯气通入冷的石灰乳中可制备漂白粉,用化学方程式表示制备原理___________ 。

请回答下列问题:
(1)84消毒液的有效成分是次氯酸钠,从物质的分类上看,次氯酸钠属于
A.酸 B.碱 C.盐 D.非电解质 E.电解质 F.弱电解质
(2)如果发生了氯气泄漏,以下自救方法得当的是___________(填序号)。
| A.向地势低的地方撤离 |
| B.观察风向,顺风撤离 |
| C.用蘸有肥皂水的毛巾捂住口鼻撤离 |
| D.用洁净抹布浸透氢氧化钠溶液捂住嘴和鼻 |
(3)使用84消毒液漂白衣物时,在空气中放置一段时间,漂白效果更好,原因是
(4)将氯气通入冷的石灰乳中可制备漂白粉,用化学方程式表示制备原理
您最近一年使用:0次
2023-11-08更新
|
107次组卷
|
2卷引用:河南省郑州市2023-2024学年高一上学期11月期中大联考化学试题
名校
解题方法
7 . 氯气与NaOH溶液在条件1、条件2下依次发生反应1、反应2,其氧化产物都只有一种。各反应中,生成NaCl与消耗 的物质的量之间的关系如图所示:
的物质的量之间的关系如图所示:

下列叙述错误的是
 的物质的量之间的关系如图所示:
的物质的量之间的关系如图所示:
下列叙述错误的是
| A.在反应1条件下制备“84”消毒液 |
B.反应1和2中,消耗等物质的量的 ,生成的氧化产物的物质的量相等 ,生成的氧化产物的物质的量相等 |
C.反应2中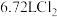 (标准状况)完全反应时转移0.5mol电子 (标准状况)完全反应时转移0.5mol电子 |
D.在反应2条件下可以发生反应: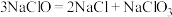 |
您最近一年使用:0次
2023-10-09更新
|
149次组卷
|
3卷引用:河南省濮阳市油田第一中学2024届高三上学期第一次考试理科综合化学试题
8 . 水合肼( )是一种用途广泛的化工原料。利用尿素制备
)是一种用途广泛的化工原料。利用尿素制备 的实验流程如下图所示。
的实验流程如下图所示。

已知:① 与碱反应放热;NaClO遇热水会分解生成
与碱反应放热;NaClO遇热水会分解生成 。
。
② 沸点约为118℃,有较强还原性的碱性液体,在空气中会与
沸点约为118℃,有较强还原性的碱性液体,在空气中会与 反应产生烟雾。
反应产生烟雾。
回答下列问题:
(1)步骤Ⅰ制备NaClO,装置如下图所示。

①装置D中盛装的试剂是___________ 。为了提高NaClO的产率,防止副反应发生,装置E需要控制一定温度,采用的方式为___________ (填“热水浴”或“冰水浴”)。
②实验过程中,需要不断地通入空气,A装置的作用是___________ 。若通入的空气没有经过装置A处理,产生的不利影响是___________ 。
(2)由步骤Ⅱ和步骤Ⅲ获得 的装置如下图所示,利用NaClO与
的装置如下图所示,利用NaClO与 的NaOH溶液反应制备;最后,再通过减压蒸馏在锥形瓶H中收集。
的NaOH溶液反应制备;最后,再通过减压蒸馏在锥形瓶H中收集。
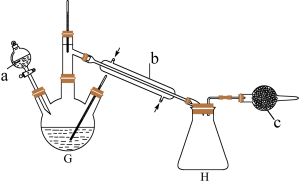
①仪器a的名称为___________ ,干燥管c中盛装的试剂为___________ 。
②实验中通过仪器a缓慢滴加的溶液是___________ [填“NaClO溶液”或“含 的NaOH溶液],原因是
的NaOH溶液],原因是___________ ,三颈烧瓶中合成 反应的化学方程式为
反应的化学方程式为___________ 。
 )是一种用途广泛的化工原料。利用尿素制备
)是一种用途广泛的化工原料。利用尿素制备 的实验流程如下图所示。
的实验流程如下图所示。
已知:①
 与碱反应放热;NaClO遇热水会分解生成
与碱反应放热;NaClO遇热水会分解生成 。
。②
 沸点约为118℃,有较强还原性的碱性液体,在空气中会与
沸点约为118℃,有较强还原性的碱性液体,在空气中会与 反应产生烟雾。
反应产生烟雾。回答下列问题:
(1)步骤Ⅰ制备NaClO,装置如下图所示。

①装置D中盛装的试剂是
②实验过程中,需要不断地通入空气,A装置的作用是
(2)由步骤Ⅱ和步骤Ⅲ获得
 的装置如下图所示,利用NaClO与
的装置如下图所示,利用NaClO与 的NaOH溶液反应制备;最后,再通过减压蒸馏在锥形瓶H中收集。
的NaOH溶液反应制备;最后,再通过减压蒸馏在锥形瓶H中收集。
①仪器a的名称为
②实验中通过仪器a缓慢滴加的溶液是
 的NaOH溶液],原因是
的NaOH溶液],原因是 反应的化学方程式为
反应的化学方程式为
您最近一年使用:0次
2023-06-24更新
|
135次组卷
|
2卷引用:河南省新未来联盟2022-2023学年高一下学期6月联考化学试题
名校
9 . R、T、X、Y、Z是短周期中的5种主族元素,它们在元素周期表中的位置如下:
已知:R的一种同位素常用来测定一些文物的年代,请回答下列问题:
(1)R、T、X的原子半径从大到小的顺序是_______ (用元素符号表示)。
(2)下列能说明Z的非金属性强于Y的是_______(填字母选项)。
(3)T的最常见氢化物(1分子内含有10个电子)。
①实验室制取该物质的反应的化学方程式为_______ 。
②该物质经催化氧化可得到T的某种氧化物,工业上经过一系列反应,最终可以制得硝酸。请写出该物质催化氧化的化学方程式_______ 。
(4)将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀;然后再加入适量浓硫酸,迅速搅拌,观察到蔗糖逐渐变黑,体积膨胀,并产生YX2气体。产生YX2气体的反应的化学方程式为_______ 。
(5)在常温下,将Z2通入NaOH溶液中,可以得到一种漂白液。该反应的离子方程式为_______ 。
| R | T | X | |
| Y | Z |
(1)R、T、X的原子半径从大到小的顺序是
(2)下列能说明Z的非金属性强于Y的是_______(填字母选项)。
| A.Z的气态氢化物比Y的气态氢化物稳定 |
| B.Z单质能从Na2Y溶液中置换出Y单质 |
C. 的还原性强于 的还原性强于 |
| D.Z的氧化物对应水合物的酸性强于Y的氧化物对应水合物的酸性 |
①实验室制取该物质的反应的化学方程式为
②该物质经催化氧化可得到T的某种氧化物,工业上经过一系列反应,最终可以制得硝酸。请写出该物质催化氧化的化学方程式
(4)将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀;然后再加入适量浓硫酸,迅速搅拌,观察到蔗糖逐渐变黑,体积膨胀,并产生YX2气体。产生YX2气体的反应的化学方程式为
(5)在常温下,将Z2通入NaOH溶液中,可以得到一种漂白液。该反应的离子方程式为
您最近一年使用:0次
名校
10 . 已知KMnO4在常温下与浓盐酸迅速反应生成Cl2,某兴趣小组设计下图装置用NaOH溶液吸收Cl2制得漂白液并探究NaClO的性质。
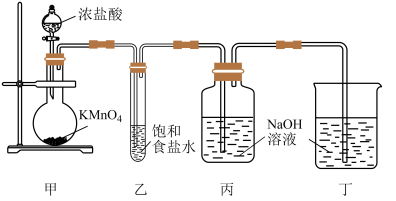
(1)甲装置中发生反应的离子方程式为_______ 。
(2)乙装置的作用为_______ 。
(3)丙装置中发生反应的离子方程式为_______ 。
(4)为探究NaClO溶液的性质,某兴趣小组进行以下实验:
i.取丙中溶液于试管中,滴入几滴紫色石蕊试液,溶液变蓝。
ii.将步骤i中蓝色溶液滴入浓盐酸中,蓝色迅速褪去,同时产生少量黄绿色气体。
iii.取丙中溶液于试管中,滴入稀H2SO4溶液,光照,产生无色气泡。
iv.取丙中溶液于试管中,滴入几滴淀粉KI溶液,溶液变蓝。
①步骤ii中蓝色迅速褪去的原因是_______ ;产生黄绿色气体的离子方程式为_______ 。
②步骤iii 中光照产生无色气泡的原因是_______ (用化学方程式表示)。
③步骤iv说明NaClO具有_______ 性。

(1)甲装置中发生反应的离子方程式为
(2)乙装置的作用为
(3)丙装置中发生反应的离子方程式为
(4)为探究NaClO溶液的性质,某兴趣小组进行以下实验:
i.取丙中溶液于试管中,滴入几滴紫色石蕊试液,溶液变蓝。
ii.将步骤i中蓝色溶液滴入浓盐酸中,蓝色迅速褪去,同时产生少量黄绿色气体。
iii.取丙中溶液于试管中,滴入稀H2SO4溶液,光照,产生无色气泡。
iv.取丙中溶液于试管中,滴入几滴淀粉KI溶液,溶液变蓝。
①步骤ii中蓝色迅速褪去的原因是
②步骤iii 中光照产生无色气泡的原因是
③步骤iv说明NaClO具有
您最近一年使用:0次
2023-02-09更新
|
130次组卷
|
5卷引用:河南省安阳市重点高中2022-2023学年一下学期开学考试化学试题
河南省安阳市重点高中2022-2023学年一下学期开学考试化学试题河南省安阳市第一中学2022-2023学年高一下学期开学考试化学试题河南郑州市2022-2023学年高一下学期开学考试化学试题(已下线)期中测试卷二【测试范围:第一、二章】-2023-2024学年高一化学上学期期中考点大串讲(人教版2019必修第一册)四川省泸州市泸县第四中学2023-2024学年高一下学期开学化学试题



