1 . 某化学研究性学习小组以干燥、纯净的 和铁粉为原料,模拟工业制备无水
和铁粉为原料,模拟工业制备无水 ,装置如图。
,装置如图。
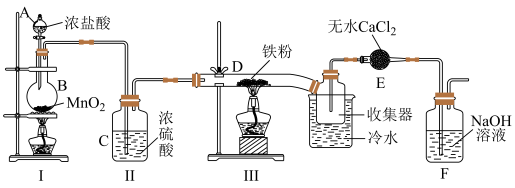
经查阅资料得知:无水 在潮湿环境中易潮解:加热易升华,遇冷易凝华。
在潮湿环境中易潮解:加热易升华,遇冷易凝华。
(1)Ⅰ中装置A的名称___________ ,烧瓶B中发生反应的离子方程式为:___________ 。
(2)开始实验时,先点燃装置___________ (填Ⅰ或Ⅲ)处酒精灯,再点燃另一处酒精灯:上述装置中有一处明显的缺陷,如何改进___________ 。
(3)E装置的作用是___________ ,F中发生反应的离子方程式___________ 。
(4)取少许产品溶于蒸馏水,静置后,向上层清液中滴加KSCN溶液,溶液不变红,产生此现象的可能原因___________ (请用必要的文字或化学方程式解释)
 和铁粉为原料,模拟工业制备无水
和铁粉为原料,模拟工业制备无水 ,装置如图。
,装置如图。
经查阅资料得知:无水
 在潮湿环境中易潮解:加热易升华,遇冷易凝华。
在潮湿环境中易潮解:加热易升华,遇冷易凝华。(1)Ⅰ中装置A的名称
(2)开始实验时,先点燃装置
(3)E装置的作用是
(4)取少许产品溶于蒸馏水,静置后,向上层清液中滴加KSCN溶液,溶液不变红,产生此现象的可能原因
您最近一年使用:0次
名校
2 .  是实验室中一种常见的化学试剂,也是生产生活中常用的净水剂。
是实验室中一种常见的化学试剂,也是生产生活中常用的净水剂。 熔点为306℃,沸点为315℃,易吸收空气中的水分而潮解。巴中中学某化学兴趣设计以下装置,制备
熔点为306℃,沸点为315℃,易吸收空气中的水分而潮解。巴中中学某化学兴趣设计以下装置,制备 。
。
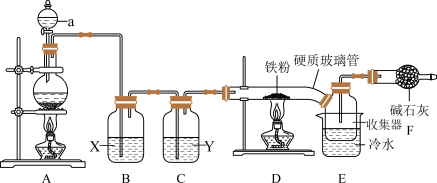
回答下列问题:
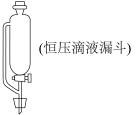
(1)A中发生的化学反应方程式是___________ 。为使实验顺利进行,可将仪器a更换为恒压滴液漏斗(如上图),更换后优点是___________ 。
(2)试剂“X”是___________ ,其作用是___________ 。
(3)硬质玻璃管直接连接收集器的优点___________ 。
(4)实验开始时,应先点燃A处酒精灯,当___________ 时,再点燃D处酒精灯。
(5)装置F作用是吸收多余氯气和___________ ,氯气和碱石灰反应时,若有0.71g氯气被氧化成次氯酸盐,1.42g氯气被氧化成氯酸盐,则被还原的氯原子的物质的量为___________ 。
 是实验室中一种常见的化学试剂,也是生产生活中常用的净水剂。
是实验室中一种常见的化学试剂,也是生产生活中常用的净水剂。 熔点为306℃,沸点为315℃,易吸收空气中的水分而潮解。巴中中学某化学兴趣设计以下装置,制备
熔点为306℃,沸点为315℃,易吸收空气中的水分而潮解。巴中中学某化学兴趣设计以下装置,制备 。
。

回答下列问题:
(1)A中发生的化学反应方程式是
(2)试剂“X”是
(3)硬质玻璃管直接连接收集器的优点
(4)实验开始时,应先点燃A处酒精灯,当
(5)装置F作用是吸收多余氯气和
您最近一年使用:0次
名校
3 . 寒冬袭来,病毒肆虐,含氯消毒剂在控制病原微生物污染和传播等方面有着重要作用。某校课外化学小组设计如图所示装置制备少量氯气并进行系列实验(夹持仪器已略)。
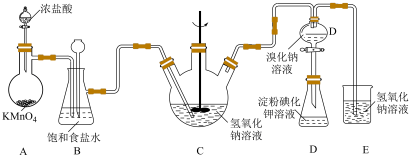
已知淀粉溶液遇碘单质变蓝;卤素单质在水中的颜色如表所示:
(1)请写出实验室用 与浓盐酸制氯气的化学方程式
与浓盐酸制氯气的化学方程式___________ ;
(2)装置B的作用是___________ ;
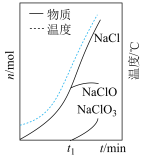
(3)装置C中生成各物质的物质的量和溶液的温度随时间的变化如下图所示。写出 分钟后氧化产物只有
分钟后氧化产物只有 的反应,对应的化学方程式
的反应,对应的化学方程式___________ ;
(4)设计装置D、E的目的是验证氧化性 。当向D中缓缓通入一定量氯气时,可以看到D中无色溶液逐渐变为
。当向D中缓缓通入一定量氯气时,可以看到D中无色溶液逐渐变为___________ 色,若打开装置D的活塞,使D中溶液滴入装置E,可以观察到的现象是___________ ,经认真考虑,有同学提出该实验方案仍有不足,你若同意该建议,请说明其中不足的原因是___________ ;(若不同意,则该空不用写)
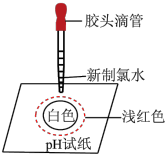
(5)某同学在pH试纸上滴几滴新制的氯水,现象如图所示,下列有关该实验的说法中正确的是___________。

已知淀粉溶液遇碘单质变蓝;卤素单质在水中的颜色如表所示:
| 卤素单质 |  |  |  |
| 水溶液颜色 | 黄绿色 | 橙黄色 | 棕黄色 |
(1)请写出实验室用
 与浓盐酸制氯气的化学方程式
与浓盐酸制氯气的化学方程式(2)装置B的作用是
(3)装置C中生成各物质的物质的量和溶液的温度随时间的变化如下图所示。写出
 分钟后氧化产物只有
分钟后氧化产物只有 的反应,对应的化学方程式
的反应,对应的化学方程式
(4)设计装置D、E的目的是验证氧化性
 。当向D中缓缓通入一定量氯气时,可以看到D中无色溶液逐渐变为
。当向D中缓缓通入一定量氯气时,可以看到D中无色溶液逐渐变为(5)某同学在pH试纸上滴几滴新制的氯水,现象如图所示,下列有关该实验的说法中正确的是___________。

A.该实验说明 分子具有漂白性 分子具有漂白性 |
B.该实验说明 扩散速率比HClO分子快 扩散速率比HClO分子快 |
| C.将实验后变白的pH试纸再滴入盐酸又会变红 |
| D.若用久置的氯水进行实验,现象相同 |
您最近一年使用:0次
2024-01-25更新
|
85次组卷
|
2卷引用:四川省绵阳市绵阳中学2023-2024学年高一上学期期末模拟测试化学试题
名校
4 . 国际化学年的中国宣传口号是“化学——我们的生活,我们的未来”。学习化学应该明白“从生活中来,到生活中去”的道理。请填空:
(1)金属钠等活泼金属着火时,应该用___________ 来灭火,不能用水灭火的原因是___________ 。
(2)用下面方法可以制得白色的 沉淀。
沉淀。
用不含 的
的 溶液与用不含
溶液与用不含 的蒸馏水配制的NaOH溶液反应制备。
的蒸馏水配制的NaOH溶液反应制备。
①用硫酸亚铁晶体配制上述 溶液时还需加入
溶液时还需加入___________ 。
②除去蒸馏水中溶解的 常采用
常采用___________ 的方法。
③如果没有除去氧气会看到白色沉淀变为红褐色沉淀,该反应的化学方程式为___________ 。
(3)某化工厂的贮氯罐意外发生泄漏,消防员向贮氯罐周围空气中喷洒稀NaOH溶液,发生反应的离子方程式是___________ 。为了安全,组织群众疏散的地方应是___________ (填序号)。
A.顺风高坡处 B.逆风高坡处 C.顺风低洼处 D.逆风低洼处
(4)二氧化氯( )是一种在水处理等方面有广泛应用的高效安全消毒剂,而且与
)是一种在水处理等方面有广泛应用的高效安全消毒剂,而且与 相比不会产生对人体有潜在危害的有机氯代物。可以由
相比不会产生对人体有潜在危害的有机氯代物。可以由 、
、 、
、 制备
制备 :
:
①配平下列方程式:___________


②上述反应中氧化剂是___________ 。
③若反应中有0.1mol电子转移,则产生的 气体在标准状况下的体积约为
气体在标准状况下的体积约为___________ L。
(1)金属钠等活泼金属着火时,应该用
(2)用下面方法可以制得白色的
 沉淀。
沉淀。用不含
 的
的 溶液与用不含
溶液与用不含 的蒸馏水配制的NaOH溶液反应制备。
的蒸馏水配制的NaOH溶液反应制备。①用硫酸亚铁晶体配制上述
 溶液时还需加入
溶液时还需加入②除去蒸馏水中溶解的
 常采用
常采用③如果没有除去氧气会看到白色沉淀变为红褐色沉淀,该反应的化学方程式为
(3)某化工厂的贮氯罐意外发生泄漏,消防员向贮氯罐周围空气中喷洒稀NaOH溶液,发生反应的离子方程式是
A.顺风高坡处 B.逆风高坡处 C.顺风低洼处 D.逆风低洼处
(4)二氧化氯(
 )是一种在水处理等方面有广泛应用的高效安全消毒剂,而且与
)是一种在水处理等方面有广泛应用的高效安全消毒剂,而且与 相比不会产生对人体有潜在危害的有机氯代物。可以由
相比不会产生对人体有潜在危害的有机氯代物。可以由 、
、 、
、 制备
制备 :
:①配平下列方程式:


②上述反应中氧化剂是
③若反应中有0.1mol电子转移,则产生的
 气体在标准状况下的体积约为
气体在标准状况下的体积约为
您最近一年使用:0次
5 . 人类对氯的认识经历了漫长的过程。回答下列问题:
(1)18世纪70年代,瑞典化学家舍勒将软锰矿(主要成分是MnO2)与浓盐酸混合加热,首次制得Cl2,该反应的离子方程式是___________ 。
(2)1785年,贝托雷最早利用氯气的水溶液做漂白剂,可以永久性地漂白纸张和鲜花,且在阳光下能够分解产生氧气。某实验小组利用如下实验装置探究氯气是否具有漂白性。___________ ,装置接口的连接顺序是a→______→______→______→______→f。___________
②装置乙中的试剂Y是___________ 。
③实验开始后,关闭装置乙中的开关K,观察到干燥有色布条___________ (填“褪色”或“不褪色”);打开开关K,观察到干燥有色布条___________ (填“褪色”或“不褪色”),证明氯气没有漂白性,但氯气与水反应的产物___________ 具有漂白性。
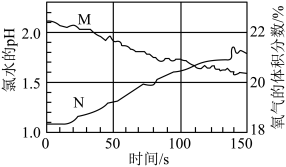
④实验小组利用数字传感器测定广口瓶中的氯水在光照条件下的pH和瓶中氧气的体积分数变化曲线如下图所示,其中表示氯水的pH变化的曲线是___________ (填“M”或“N”),据此分析,此时广口瓶中发生反应的化学方程式是___________ 。___________ 。
(1)18世纪70年代,瑞典化学家舍勒将软锰矿(主要成分是MnO2)与浓盐酸混合加热,首次制得Cl2,该反应的离子方程式是
(2)1785年,贝托雷最早利用氯气的水溶液做漂白剂,可以永久性地漂白纸张和鲜花,且在阳光下能够分解产生氧气。某实验小组利用如下实验装置探究氯气是否具有漂白性。

②装置乙中的试剂Y是
③实验开始后,关闭装置乙中的开关K,观察到干燥有色布条
④实验小组利用数字传感器测定广口瓶中的氯水在光照条件下的pH和瓶中氧气的体积分数变化曲线如下图所示,其中表示氯水的pH变化的曲线是
您最近一年使用:0次
2024-01-24更新
|
45次组卷
|
2卷引用:四川省凉山州宁南中学2023-2024学年高一上学期期末考试化学模拟试题(一)
名校
6 . 下列有关氯及其化合物的说法,正确的是
A.纯净的 在 在 中安静的燃烧,发出淡蓝色的火焰 中安静的燃烧,发出淡蓝色的火焰 |
B.由 和Fe直接化合可制得 和Fe直接化合可制得 |
C.常温下,将 通入NaOH溶液中,可以得到以NaClO为有效成分的漂白液 通入NaOH溶液中,可以得到以NaClO为有效成分的漂白液 |
| D.氯水放置较长时间,其漂白性增强 |
您最近一年使用:0次
2023-11-09更新
|
255次组卷
|
2卷引用:四川省广安市育才学校2023-2024学年高一上学期期中考试化学试题
7 . 以 为原料制备
为原料制备 和
和 ,并利用
,并利用 冶炼金属钛(Ti)的工艺流程如下:
冶炼金属钛(Ti)的工艺流程如下:
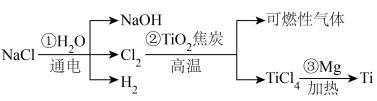
已知:高温条件下Ti的性质很活泼。
回答下列问题:
(1)在实际生产中,应避免步骤①的产物 与
与 接触发生副反应,降低
接触发生副反应,降低 纯度,解释其原因,用离子方程式表示为
纯度,解释其原因,用离子方程式表示为___________ 。
(2) 在
在 中燃烧的现象是
中燃烧的现象是___________ ,恰好完全反应后,将产物溶于水制得密度为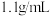 ,质量分数为
,质量分数为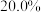 的盐酸溶液,其物质的量浓度为
的盐酸溶液,其物质的量浓度为___________ 。
(3)步骤②发生反应的化学方程式为___________ ,该反应中氧化产物与还原产物的物质的量之比为___________ 。
(4)步骤③须在稀有气体(如氩)的氛围下进行,稀有气体的作用是___________ 。
 为原料制备
为原料制备 和
和 ,并利用
,并利用 冶炼金属钛(Ti)的工艺流程如下:
冶炼金属钛(Ti)的工艺流程如下:
已知:高温条件下Ti的性质很活泼。
回答下列问题:
(1)在实际生产中,应避免步骤①的产物
 与
与 接触发生副反应,降低
接触发生副反应,降低 纯度,解释其原因,用离子方程式表示为
纯度,解释其原因,用离子方程式表示为(2)
 在
在 中燃烧的现象是
中燃烧的现象是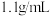 ,质量分数为
,质量分数为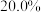 的盐酸溶液,其物质的量浓度为
的盐酸溶液,其物质的量浓度为(3)步骤②发生反应的化学方程式为
(4)步骤③须在稀有气体(如氩)的氛围下进行,稀有气体的作用是
您最近一年使用:0次
名校
8 . 按下图装置进行实验,探究氯气的性质,下列说法正确的是
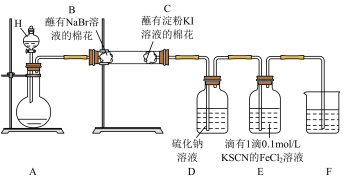

| A.仪器H的名称为分液漏斗,可用长颈漏斗替换 |
| B.C中棉花变蓝,说明氯气置换出碘,则非金属性:Cl>I, |
| C.E中溶液先变红后褪色,说明Cl2有漂白性 |
| D.F中溶液为NaOH溶液,进行尾气处理 |
您最近一年使用:0次
2023-08-08更新
|
307次组卷
|
2卷引用:四川省仁寿第一中学校南校区2023-2024学年高三上学期开学考试化学试题
解题方法
9 . 化学与生产、生活密切相关,回答下列问题。
(1)某品牌奶制品的外包装上有如图所示的说明。从食品添加剂的主要功能考虑,配料中作防腐剂的是___________ ,用化学反应速率的知识说明避免高温贮存该奶制品的理由___________ 。
(2)常温下,将 通入
通入 溶液可制得漂白液,反应的离子方程式为
溶液可制得漂白液,反应的离子方程式为___________ 。
(3)工业上用氨氧化制取硝酸的流程如下:
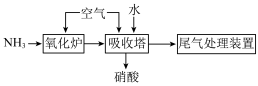
①氮在元素周期表的位置是___________ ,氧化炉中发生反应的化学方程式为___________ 。
②向吸收塔中通入空气的作用是___________ ,如果没有“尾气处理装置”,可能产生的环境问题是___________ 。
③实验室中硝酸一般盛放在棕色试剂瓶中,请用化学方程式说明其原因___________ 。
(1)某品牌奶制品的外包装上有如图所示的说明。从食品添加剂的主要功能考虑,配料中作防腐剂的是
| 【配料】水、白砂糖、脱脂乳粉、山梨酸钾、碳酸钙、食用香精、维生素A 【贮存条件】阴凉干燥处,避免高温 |
 通入
通入 溶液可制得漂白液,反应的离子方程式为
溶液可制得漂白液,反应的离子方程式为(3)工业上用氨氧化制取硝酸的流程如下:

①氮在元素周期表的位置是
②向吸收塔中通入空气的作用是
③实验室中硝酸一般盛放在棕色试剂瓶中,请用化学方程式说明其原因
您最近一年使用:0次
名校
10 . 利用如图所示装置进行 的制备及性质探究实验时,下列说法不正确的是
的制备及性质探究实验时,下列说法不正确的是

 的制备及性质探究实验时,下列说法不正确的是
的制备及性质探究实验时,下列说法不正确的是
| A.甲中反应的氧化剂与还原剂的物质的量之比为1∶4 |
B.乙的作用为除去 中的HCl 中的HCl |
| C.丙中紫色石蕊试液先变红后褪色 |
D.为吸收多余的 ,丁中可盛放NaOH溶液 ,丁中可盛放NaOH溶液 |
您最近一年使用:0次
2023-02-19更新
|
1760次组卷
|
6卷引用:四川省成都市第七中学2023-2024学年高一上学期期中考试化学试题
四川省成都市第七中学2023-2024学年高一上学期期中考试化学试题四川省广安市华蓥中学2023-2024学年高一上学期12月月考化学试题广东省深圳市2022-2023学年高三第一次调研考试化学试题(已下线)广东省深圳市2022-2023学年高三第一次调研考试变式题(选择题6-10)安徽省定远县第三中学2022-2023学年高三下学期二模化学试题(已下线)专题13 化学实验基础



