解题方法
1 . 实验室用下图装置制备并收集干燥纯净 的Cl2。

回答以下问题:
(1)装置A中反应的化学方程式是___________ 。
(2)装置B的作用是___________ 。
(3)装置C中盛放的物质是___________ ,其作用是___________ 。
(4)装置D用于收集Cl2,请将图中装置D的导气管补充完整 ___________ 。
(5)装置E用于吸收尾气,E中反应的化学方程式是___________ 。

回答以下问题:
(1)装置A中反应的化学方程式是
(2)装置B的作用是
(3)装置C中盛放的物质是
(4)装置D用于收集Cl2,请将图中装置D的导气管
(5)装置E用于吸收尾气,E中反应的化学方程式是
您最近半年使用:0次
2 . 写出要求的方程式

(1)①离子方程式____________________________ ;
(2)②离子方程式______________________ ;
(3)③化学方程式____________________________ ;
(4)④溶液中,离子方程式______________________ ;
(5)⑤固体,化学方程式______________________ ;
(6)⑥溶液中,离子方程式______________________ ;
(7)⑦化学方程式____________________________ ;
(8)⑧离子方程式______________________ ;
(9)⑨离子方程式______________________ ;

(1)①离子方程式
(2)②离子方程式
(3)③化学方程式
(4)④溶液中,离子方程式
(5)⑤固体,化学方程式
(6)⑥溶液中,离子方程式
(7)⑦化学方程式
(8)⑧离子方程式
(9)⑨离子方程式
您最近半年使用:0次
名校
解题方法
3 . 食盐是生活中的调味剂,从多角度认识食盐及主要成分 。
。
(1)从组成和结构的角度看, 由
由___________ (填“原子”“分子”或“离子”构成,属于___________ (填“酸”“䂸”或“盐”)。
(2)从水溶液或熔融状态下是否电离的角度看, 属于
属于___________ ,其电离方程式为___________ 。
(3)对于水溶液体系,从离子角度认识其性质,向 溶液中滴加硝酸银溶液,预测现象为
溶液中滴加硝酸银溶液,预测现象为___________ ,反应的离子方程式___________ 。
(4)用洁净的铂丝蘸取食盐在酒精灯火焰上灼烧,火焰的颜色是___________ 。
(5)某同学发现家里的食盐包装袋标签上,标注成分中有氯化钠、碘酸钾、柠檬酸铁铵,同学查阅资料得知,柠檬酸铁铵在水溶液中能电离出 ,从化合价的角度,你预测有
,从化合价的角度,你预测有 具有的性质是
具有的性质是___________ ,设计实验证明此性质,你选择 与
与___________ (填具体反应物或物质类别均可)发生反应。
(6) 在自然界含量丰富,工业电解饱和食盐水制得氯气、氢气和氢氧化钠,此反应的化学方程式为
在自然界含量丰富,工业电解饱和食盐水制得氯气、氢气和氢氧化钠,此反应的化学方程式为___________ ,如果氯元素完全转化为氯气,理论上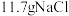 能制取的氯气在标准状况下的体积是
能制取的氯气在标准状况下的体积是___________ 。
(7)工业制得的氯气用途广泛,将氯气通入石灰乳制取漂白粉,化学反应方程式为___________ 。
(8)某居民因混合使用“洁厕灵”(主要成分是盐酸)与“84”消毒液发生氯气中毒。试根据你的化学知识分析,用离子方程式解释原因___________ 。
 。
。(1)从组成和结构的角度看,
 由
由(2)从水溶液或熔融状态下是否电离的角度看,
 属于
属于(3)对于水溶液体系,从离子角度认识其性质,向
 溶液中滴加硝酸银溶液,预测现象为
溶液中滴加硝酸银溶液,预测现象为(4)用洁净的铂丝蘸取食盐在酒精灯火焰上灼烧,火焰的颜色是
(5)某同学发现家里的食盐包装袋标签上,标注成分中有氯化钠、碘酸钾、柠檬酸铁铵,同学查阅资料得知,柠檬酸铁铵在水溶液中能电离出
 ,从化合价的角度,你预测有
,从化合价的角度,你预测有 具有的性质是
具有的性质是 与
与(6)
 在自然界含量丰富,工业电解饱和食盐水制得氯气、氢气和氢氧化钠,此反应的化学方程式为
在自然界含量丰富,工业电解饱和食盐水制得氯气、氢气和氢氧化钠,此反应的化学方程式为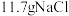 能制取的氯气在标准状况下的体积是
能制取的氯气在标准状况下的体积是(7)工业制得的氯气用途广泛,将氯气通入石灰乳制取漂白粉,化学反应方程式为
(8)某居民因混合使用“洁厕灵”(主要成分是盐酸)与“84”消毒液发生氯气中毒。试根据你的化学知识分析,用离子方程式解释原因
您最近半年使用:0次
名校
解题方法
4 . 下列离子方程式正确的是
A.实验室用大理石和稀盐酸制取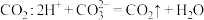 |
B.氯气与水反应: |
C.氯化铁溶液加入氨水: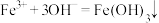 |
D.用氢氧化钠检验氯化铵溶液中铵根离子: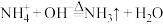 |
您最近半年使用:0次
名校
解题方法
5 . 实验小组同学制备KClO3并探究其性质,过程如下:

下列说法不正确 的是

下列说法
| A.可用饱和NaOH溶液净化氯气 |
B.生成KClO3的离子方程式为3Cl2+6OH- ClO ClO +5Cl-+3H2O +5Cl-+3H2O |
| C.推测若取无色溶液a于试管中,滴加稀H2SO4后再加入少量CCl4,下层液体变紫色 |
| D.上述实验说明碱性条件下氧化性:Cl2>KClO3,酸性条件下氧化性:Cl2<KClO3 |
您最近半年使用:0次
名校
解题方法
6 . 下列离子方程式正确的是
A. 溶液通入氯气: 溶液通入氯气: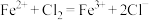 |
B.实验室制氯气尾气用 溶液吸收: 溶液吸收: |
C. 使澄清石灰水变浑浊: 使澄清石灰水变浑浊: |
D. 溶液和 溶液和 溶液混合: 溶液混合: |
您最近半年使用:0次
7 . 亚氯酸钠 是一种重要的含氯消毒剂,易溶于水,在碱性溶液中比较稳定,遇酸放出
是一种重要的含氯消毒剂,易溶于水,在碱性溶液中比较稳定,遇酸放出 。一种由
。一种由 制备
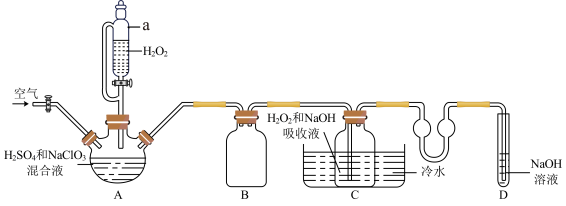
制备 晶体的实验装置如图(夹持装置略去)所示:
晶体的实验装置如图(夹持装置略去)所示:
已知:①饱和 溶液中析出的晶体成分与温度的关系如下表所示:
溶液中析出的晶体成分与温度的关系如下表所示:
② 易溶于水,在温度过高、浓度过大时易发生分解。
易溶于水,在温度过高、浓度过大时易发生分解。
回答下列问题:
(1)装置A为 发生装置,其中发生反应的离子方程式为
发生装置,其中发生反应的离子方程式为_______ 。
(2) 在装置C中生成
在装置C中生成 ,化学反应方程式为
,化学反应方程式为_______ , 的另一个作用是
的另一个作用是_______ ,装置C中冷水的作用是_______ 。
(3)从装置C中获得 晶体的方法是:在
晶体的方法是:在_______ (填“温度范围”)、_______ (填“常压”、“减压”)蒸发结晶、_______ (填“趁热”、“冷却”)过滤,50℃左右热水洗涤,低于60℃条件下烘干,得到 晶体。
晶体。
 是一种重要的含氯消毒剂,易溶于水,在碱性溶液中比较稳定,遇酸放出
是一种重要的含氯消毒剂,易溶于水,在碱性溶液中比较稳定,遇酸放出 。一种由
。一种由 制备
制备 晶体的实验装置如图(夹持装置略去)所示:
晶体的实验装置如图(夹持装置略去)所示:
已知:①饱和
 溶液中析出的晶体成分与温度的关系如下表所示:
溶液中析出的晶体成分与温度的关系如下表所示:| 温度/℃ |  | 38~60 |  |
| 晶体成分 |  |  |  分解成 分解成 和 和 |
 易溶于水,在温度过高、浓度过大时易发生分解。
易溶于水,在温度过高、浓度过大时易发生分解。回答下列问题:
(1)装置A为
 发生装置,其中发生反应的离子方程式为
发生装置,其中发生反应的离子方程式为(2)
 在装置C中生成
在装置C中生成 ,化学反应方程式为
,化学反应方程式为 的另一个作用是
的另一个作用是(3)从装置C中获得
 晶体的方法是:在
晶体的方法是:在 晶体。
晶体。
您最近半年使用:0次
名校
8 . 某小组设计了如图所示的实验装置来探究过氧化钠的强氧化性。
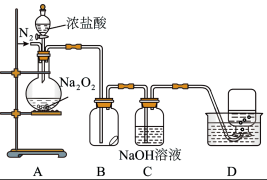
实验步骤及现象如下:
①检查装置气密性后,装入药品并连接装置A、B、C。
②缓慢通入一定量的 后,将装置D连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,A中剧烈反应,有黄绿色气体产生。
后,将装置D连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,A中剧烈反应,有黄绿色气体产生。
③待装置D中导管口产生连续气泡后,将导管末端伸入集气瓶中,收集到无色气体。
④反应一段时间后,停止滴加浓盐酸,再通一段时间 ,直至装置中气体变为无色。
,直至装置中气体变为无色。
(1)装置D中收集的无色气体X能使带火星的木条复燃,据此推断该气体X是_______ 。
(2)装置B中湿润的淀粉碘化钾试纸变蓝。甲同学认为是黄绿色气体造成试纸颜色发生改变。乙同学认为X气体也能使试纸变蓝,写出可能发生的化学反应方程式_______ 。
(3)A中生成黄绿色气体的化学反应方程式为_______ 。

实验步骤及现象如下:
①检查装置气密性后,装入药品并连接装置A、B、C。
②缓慢通入一定量的
 后,将装置D连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,A中剧烈反应,有黄绿色气体产生。
后,将装置D连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,A中剧烈反应,有黄绿色气体产生。③待装置D中导管口产生连续气泡后,将导管末端伸入集气瓶中,收集到无色气体。
④反应一段时间后,停止滴加浓盐酸,再通一段时间
 ,直至装置中气体变为无色。
,直至装置中气体变为无色。(1)装置D中收集的无色气体X能使带火星的木条复燃,据此推断该气体X是
(2)装置B中湿润的淀粉碘化钾试纸变蓝。甲同学认为是黄绿色气体造成试纸颜色发生改变。乙同学认为X气体也能使试纸变蓝,写出可能发生的化学反应方程式
(3)A中生成黄绿色气体的化学反应方程式为
您最近半年使用:0次
名校
解题方法
9 . 电解饱和食盐水是工业制备氯气和 的重要方法,其原理如图所示。下列说法不正确的是
的重要方法,其原理如图所示。下列说法不正确的是

 的重要方法,其原理如图所示。下列说法不正确的是
的重要方法,其原理如图所示。下列说法不正确的是
A.产生气体x的电极反应: |
B.溶液A为较浓的 溶液 溶液 |
C.理论上每生成 气体y,有 气体y,有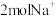 通过交换膜 通过交换膜 |
D.若不使用交换膜,会使 的产量降低。 的产量降低。 |
您最近半年使用:0次
名校
解题方法
10 . 高铁酸钾( ,其中Fe元素为+6价)是新型绿色水处理剂,其制备方法如下图所示(部分步骤已略去)。
,其中Fe元素为+6价)是新型绿色水处理剂,其制备方法如下图所示(部分步骤已略去)。
已知:在碱性溶液中的溶解度: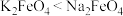
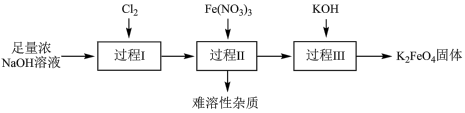
(1)过程Ⅰ的目的是制备 ,
, 中氯元素的化合价为
中氯元素的化合价为______ 。
(2)过程Ⅱ为碱性条件下制备高铁酸钠(Na2FeO4)。
①补全过程Ⅱ中发生反应的离子方程式:____
 。
。
②除 外,过程Ⅱ中还可能生成一种含铁元素的难溶性杂质,该物质的化学式为
外,过程Ⅱ中还可能生成一种含铁元素的难溶性杂质,该物质的化学式为_____ 。
(3)过程Ⅲ中,发生反应的化学方程式为______ 。
(4)过程Ⅰ~Ⅲ中,需要进行过滤操作的是______ (填序号)。
(5) 可将氨氮废水中的
可将氨氮废水中的 转化为
转化为 除去。从价态角度分析,
除去。从价态角度分析, 能处理氨氮废水的原因是
能处理氨氮废水的原因是______ 。
 ,其中Fe元素为+6价)是新型绿色水处理剂,其制备方法如下图所示(部分步骤已略去)。
,其中Fe元素为+6价)是新型绿色水处理剂,其制备方法如下图所示(部分步骤已略去)。已知:在碱性溶液中的溶解度:
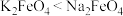

(1)过程Ⅰ的目的是制备
 ,
, 中氯元素的化合价为
中氯元素的化合价为(2)过程Ⅱ为碱性条件下制备高铁酸钠(Na2FeO4)。
①补全过程Ⅱ中发生反应的离子方程式:
 。
。②除
 外,过程Ⅱ中还可能生成一种含铁元素的难溶性杂质,该物质的化学式为
外,过程Ⅱ中还可能生成一种含铁元素的难溶性杂质,该物质的化学式为(3)过程Ⅲ中,发生反应的化学方程式为
(4)过程Ⅰ~Ⅲ中,需要进行过滤操作的是
(5)
 可将氨氮废水中的
可将氨氮废水中的 转化为
转化为 除去。从价态角度分析,
除去。从价态角度分析, 能处理氨氮废水的原因是
能处理氨氮废水的原因是
您最近半年使用:0次



