名校
解题方法
1 . 高铁酸钾( ,其中Fe元素为+6价)是新型绿色水处理剂,其制备方法如下图所示(部分步骤已略去)。
,其中Fe元素为+6价)是新型绿色水处理剂,其制备方法如下图所示(部分步骤已略去)。
已知:在碱性溶液中的溶解度: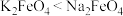
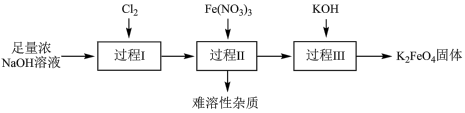
(1)过程Ⅰ的目的是制备 ,
, 中氯元素的化合价为
中氯元素的化合价为______ 。
(2)过程Ⅱ为碱性条件下制备高铁酸钠(Na2FeO4)。
①补全过程Ⅱ中发生反应的离子方程式:____
 。
。
②除 外,过程Ⅱ中还可能生成一种含铁元素的难溶性杂质,该物质的化学式为
外,过程Ⅱ中还可能生成一种含铁元素的难溶性杂质,该物质的化学式为_____ 。
(3)过程Ⅲ中,发生反应的化学方程式为______ 。
(4)过程Ⅰ~Ⅲ中,需要进行过滤操作的是______ (填序号)。
(5) 可将氨氮废水中的
可将氨氮废水中的 转化为
转化为 除去。从价态角度分析,
除去。从价态角度分析, 能处理氨氮废水的原因是
能处理氨氮废水的原因是______ 。
 ,其中Fe元素为+6价)是新型绿色水处理剂,其制备方法如下图所示(部分步骤已略去)。
,其中Fe元素为+6价)是新型绿色水处理剂,其制备方法如下图所示(部分步骤已略去)。已知:在碱性溶液中的溶解度:
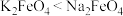

(1)过程Ⅰ的目的是制备
 ,
, 中氯元素的化合价为
中氯元素的化合价为(2)过程Ⅱ为碱性条件下制备高铁酸钠(Na2FeO4)。
①补全过程Ⅱ中发生反应的离子方程式:
 。
。②除
 外,过程Ⅱ中还可能生成一种含铁元素的难溶性杂质,该物质的化学式为
外,过程Ⅱ中还可能生成一种含铁元素的难溶性杂质,该物质的化学式为(3)过程Ⅲ中,发生反应的化学方程式为
(4)过程Ⅰ~Ⅲ中,需要进行过滤操作的是
(5)
 可将氨氮废水中的
可将氨氮废水中的 转化为
转化为 除去。从价态角度分析,
除去。从价态角度分析, 能处理氨氮废水的原因是
能处理氨氮废水的原因是
您最近一年使用:0次
名校
解题方法
2 . 下列方程式与所给事实不相符 的是
A.浓硝酸保存于棕色试剂瓶中是为了防止: |
B.向 饱和溶液中依次通入过量 饱和溶液中依次通入过量 、 、 ,析出沉淀: ,析出沉淀: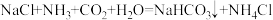 |
C.将 通入冷的石灰乳中,制得漂白粉: 通入冷的石灰乳中,制得漂白粉: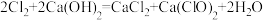 |
D.电解饱和食盐水,两极(碳棒)均产生气体: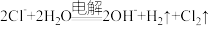 |
您最近一年使用:0次
2023-05-07更新
|
749次组卷
|
3卷引用:北京市朝阳区2022-2023年高三下学期第二次模拟考试化学试题
名校
解题方法
3 . 将Cl2通入过量石灰乳[Ca(OH)2]中即可制得以Ca(ClO)2为有效成分的漂白粉。下列解释事实的方程式中,不正确 的是
| A.生成Ca(ClO)2:2Ca(OH)2+2Cl2=Ca(ClO)2+CaCl2+2H2O |
| B.漂白粉溶液与盐酸混合产生Cl2:ClO﹣+Cl﹣+2H+=Cl2↑+H2O |
| C.漂白粉溶液吸收CO2后产生白色沉淀:Ca2++CO2+H2O=CaCO3↓+2H+ |
| D.漂白粉溶液加入适量醋酸在短时间内能达到漂白效果:Ca(OH)2+2CH3COOH=Ca(CH3COO)2+2H2O、Ca(ClO)2+2CH3COOH=Ca(CH3COO)2+2HClO |
您最近一年使用:0次
2022-01-16更新
|
646次组卷
|
6卷引用:清华大学附属中学朝阳学校2023-2024学年高一上学期期中考试化学试题
名校
解题方法
4 . “84消毒液”广泛应用于杀菌消毒,其有效成分是NaClO。实验小组制备消毒液,并利用其性质探索制备碘水的方法。
资料:i.HClO的电离常数为Ka=4.7×10-8;
H2CO3的电离常数为K1=4.3×10-7、K2=5.6×10-11。
ii.碘的化合物主要以I-和IO3-的形式存在,IO3-+5I-+6H+=3I2+3H2O。
iii.碘单质能与I-反应:I2+I- I3-(I3-低浓度时显黄色,高浓度时为棕色)。
I3-(I3-低浓度时显黄色,高浓度时为棕色)。
Ⅰ.制备消毒液(夹持装置略)
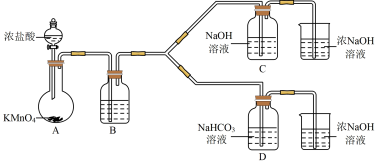
(1)制备NaClO消毒液的装置是__________ (填C或D)。
(2)制备完成后,向C装置的溶液中添加NaOH、Na2SiO3等物质,得到与某品牌成分相同的消毒液,用平衡移动原理解释NaOH的作用___________________ 。
(3)结合资料i,写出D中反应的化学方程式______________________ 。
Ⅱ.利用消毒液的性质探究碘水的制备方法
将某品牌“84消毒液”稀释10倍,各取100mL于三个烧杯中,设计如下实验方案制备碘水:
(4)对比不同方案的实验现象,得出制取碘水的最佳方法要关注的因素是________ 。
(5)针对烧杯3“滴加淀粉溶液不变蓝”的原因,提出两种假设:
假设1:过量的NaClO将反应生成的I2氧化为IO3-。
设计实验证实了假设1成立。NaClO氧化I2生成IO3-的离子方程式是_____________ 。
假设2:生成的I2在碱性溶液中不能存在。
设计实验a证实了假设2成立,实验a的操作及现象是______________________ 。
(6)某小组检验烧杯3所得溶液中含IO3-:取烧杯3所得无色溶液少许,加入稀硫酸酸化的KI溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在IO3-,说明理由______________________ 。
(7)预测烧杯1反应后加淀粉溶液的实验现象,结合方程式说明预测依据________ 。
资料:i.HClO的电离常数为Ka=4.7×10-8;
H2CO3的电离常数为K1=4.3×10-7、K2=5.6×10-11。
ii.碘的化合物主要以I-和IO3-的形式存在,IO3-+5I-+6H+=3I2+3H2O。
iii.碘单质能与I-反应:I2+I-
 I3-(I3-低浓度时显黄色,高浓度时为棕色)。
I3-(I3-低浓度时显黄色,高浓度时为棕色)。Ⅰ.制备消毒液(夹持装置略)

(1)制备NaClO消毒液的装置是
(2)制备完成后,向C装置的溶液中添加NaOH、Na2SiO3等物质,得到与某品牌成分相同的消毒液,用平衡移动原理解释NaOH的作用
(3)结合资料i,写出D中反应的化学方程式
Ⅱ.利用消毒液的性质探究碘水的制备方法
将某品牌“84消毒液”稀释10倍,各取100mL于三个烧杯中,设计如下实验方案制备碘水:
| 方案 | 操作 | 现象 | 反应后加淀粉溶液 |
| 1 | 烧杯1溶液中加入9gKI固体 | 溶液为橙黄色 | …… |
| 2 | 烧杯2溶液中加入9gKI固体再加入1mo/L盐酸10mL | 溶液颜色快速加深,呈紫红色 | 变蓝 |
| 3 | 烧杯3溶液中加入少量KI固体(小于0.5g) | 振荡后溶液保持无色 | 不变蓝 |
(5)针对烧杯3“滴加淀粉溶液不变蓝”的原因,提出两种假设:
假设1:过量的NaClO将反应生成的I2氧化为IO3-。
设计实验证实了假设1成立。NaClO氧化I2生成IO3-的离子方程式是
假设2:生成的I2在碱性溶液中不能存在。
设计实验a证实了假设2成立,实验a的操作及现象是
(6)某小组检验烧杯3所得溶液中含IO3-:取烧杯3所得无色溶液少许,加入稀硫酸酸化的KI溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在IO3-,说明理由
(7)预测烧杯1反应后加淀粉溶液的实验现象,结合方程式说明预测依据
您最近一年使用:0次
2020-05-07更新
|
447次组卷
|
4卷引用:北京市第八十中学2024届高三上学期10月月考化学试题
北京市第八十中学2024届高三上学期10月月考化学试题北京市石景山区2020届高三第一次模拟化学试题(已下线)北京市2019-2020学年高三各区一模化学考试分类汇编:科学探究北京首都师范大学附属中学2022届高三下学期三模化学试题



