名校
1 . 用下图装置制取纯净的氯气,有关说法正确的是
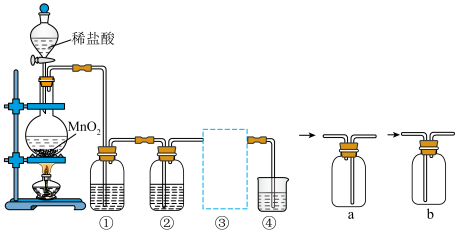
| A.①中盛放浓硫酸 | B.②的作用是除去 气体 气体 |
| C.③收集气体,应选择装置a | D.④中盛放NaOH溶液 |
您最近半年使用:0次
解题方法
2 . 实验室用下图装置制备并收集干燥纯净 的Cl2。

回答以下问题:
(1)装置A中反应的化学方程式是___________ 。
(2)装置B的作用是___________ 。
(3)装置C中盛放的物质是___________ ,其作用是___________ 。
(4)装置D用于收集Cl2,请将图中装置D的导气管补充完整 ___________ 。
(5)装置E用于吸收尾气,E中反应的化学方程式是___________ 。

回答以下问题:
(1)装置A中反应的化学方程式是
(2)装置B的作用是
(3)装置C中盛放的物质是
(4)装置D用于收集Cl2,请将图中装置D的导气管
(5)装置E用于吸收尾气,E中反应的化学方程式是
您最近半年使用:0次
3 . 写出要求的方程式

(1)①离子方程式____________________________ ;
(2)②离子方程式______________________ ;
(3)③化学方程式____________________________ ;
(4)④溶液中,离子方程式______________________ ;
(5)⑤固体,化学方程式______________________ ;
(6)⑥溶液中,离子方程式______________________ ;
(7)⑦化学方程式____________________________ ;
(8)⑧离子方程式______________________ ;
(9)⑨离子方程式______________________ ;

(1)①离子方程式
(2)②离子方程式
(3)③化学方程式
(4)④溶液中,离子方程式
(5)⑤固体,化学方程式
(6)⑥溶液中,离子方程式
(7)⑦化学方程式
(8)⑧离子方程式
(9)⑨离子方程式
您最近半年使用:0次
名校
解题方法
4 . 食盐是生活中的调味剂,从多角度认识食盐及主要成分 。
。
(1)从组成和结构的角度看, 由
由___________ (填“原子”“分子”或“离子”构成,属于___________ (填“酸”“䂸”或“盐”)。
(2)从水溶液或熔融状态下是否电离的角度看, 属于
属于___________ ,其电离方程式为___________ 。
(3)对于水溶液体系,从离子角度认识其性质,向 溶液中滴加硝酸银溶液,预测现象为
溶液中滴加硝酸银溶液,预测现象为___________ ,反应的离子方程式___________ 。
(4)用洁净的铂丝蘸取食盐在酒精灯火焰上灼烧,火焰的颜色是___________ 。
(5)某同学发现家里的食盐包装袋标签上,标注成分中有氯化钠、碘酸钾、柠檬酸铁铵,同学查阅资料得知,柠檬酸铁铵在水溶液中能电离出 ,从化合价的角度,你预测有
,从化合价的角度,你预测有 具有的性质是
具有的性质是___________ ,设计实验证明此性质,你选择 与
与___________ (填具体反应物或物质类别均可)发生反应。
(6) 在自然界含量丰富,工业电解饱和食盐水制得氯气、氢气和氢氧化钠,此反应的化学方程式为
在自然界含量丰富,工业电解饱和食盐水制得氯气、氢气和氢氧化钠,此反应的化学方程式为___________ ,如果氯元素完全转化为氯气,理论上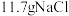 能制取的氯气在标准状况下的体积是
能制取的氯气在标准状况下的体积是___________ 。
(7)工业制得的氯气用途广泛,将氯气通入石灰乳制取漂白粉,化学反应方程式为___________ 。
(8)某居民因混合使用“洁厕灵”(主要成分是盐酸)与“84”消毒液发生氯气中毒。试根据你的化学知识分析,用离子方程式解释原因___________ 。
 。
。(1)从组成和结构的角度看,
 由
由(2)从水溶液或熔融状态下是否电离的角度看,
 属于
属于(3)对于水溶液体系,从离子角度认识其性质,向
 溶液中滴加硝酸银溶液,预测现象为
溶液中滴加硝酸银溶液,预测现象为(4)用洁净的铂丝蘸取食盐在酒精灯火焰上灼烧,火焰的颜色是
(5)某同学发现家里的食盐包装袋标签上,标注成分中有氯化钠、碘酸钾、柠檬酸铁铵,同学查阅资料得知,柠檬酸铁铵在水溶液中能电离出
 ,从化合价的角度,你预测有
,从化合价的角度,你预测有 具有的性质是
具有的性质是 与
与(6)
 在自然界含量丰富,工业电解饱和食盐水制得氯气、氢气和氢氧化钠,此反应的化学方程式为
在自然界含量丰富,工业电解饱和食盐水制得氯气、氢气和氢氧化钠,此反应的化学方程式为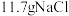 能制取的氯气在标准状况下的体积是
能制取的氯气在标准状况下的体积是(7)工业制得的氯气用途广泛,将氯气通入石灰乳制取漂白粉,化学反应方程式为
(8)某居民因混合使用“洁厕灵”(主要成分是盐酸)与“84”消毒液发生氯气中毒。试根据你的化学知识分析,用离子方程式解释原因
您最近半年使用:0次
名校
5 . 某小组同学探究不同条件下氯气与二价锰化合物的反应
资料:
ⅰ. 在一定条件下被
在一定条件下被  或
或 氧化成
氧化成  (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。
ⅱ.浓碱条件下, 可被
可被  还原为
还原为  。
。
ⅲ. 的氧化性与溶液的酸碱性无关,
的氧化性与溶液的酸碱性无关, 的氧化性随碱性增强而减弱。
的氧化性随碱性增强而减弱。
实验装置如图(夹持装置略)
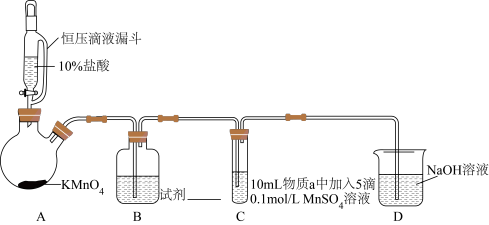
(1) 装置中制备
装置中制备  的化学反应方程式是
的化学反应方程式是__________ 。
(2) 中试剂是
中试剂是__________ 。
(3)通入 前,Ⅱ、Ⅲ中沉淀由白色变为黑色的化学方程式为
前,Ⅱ、Ⅲ中沉淀由白色变为黑色的化学方程式为__________ 。
(4)根据资料ⅱ,Ⅲ中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符原因:
原因一:可能是通入 导致溶液的碱性减弱。
导致溶液的碱性减弱。
原因二:可能是氧化剂过量,氧化剂将 氧化为
氧化为  。
。
①化学方程式表示可能导致溶液碱性减弱的原因__________ ,但通过实验测定溶液的碱性变化很小。
②取Ⅲ中放置后的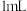 悬浊液,加入
悬浊液,加入 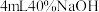 溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为
溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为__________ ,溶液绿色缓慢加深,原因是  被
被__________ (填化学式)氧化,可证明Ⅲ的悬浊液中氧化剂过量;
③取Ⅱ中放置后的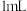 悬浊液,加入
悬浊液,加入  水,溶液紫色缓慢加深,发生的反应是
水,溶液紫色缓慢加深,发生的反应是__________ 。
资料:
ⅰ.
 在一定条件下被
在一定条件下被  或
或 氧化成
氧化成  (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。ⅱ.浓碱条件下,
 可被
可被  还原为
还原为  。
。ⅲ.
 的氧化性与溶液的酸碱性无关,
的氧化性与溶液的酸碱性无关, 的氧化性随碱性增强而减弱。
的氧化性随碱性增强而减弱。实验装置如图(夹持装置略)

序号 | 物质 | C中实验现象 | |
通入 | 通入 | ||
Ⅰ | 水 | 得到无色溶液 | 产生棕黑色沉淀,且放置后不发生变化 |
Ⅱ |
| 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
Ⅲ |
| 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
(1)
 装置中制备
装置中制备  的化学反应方程式是
的化学反应方程式是(2)
 中试剂是
中试剂是(3)通入
 前,Ⅱ、Ⅲ中沉淀由白色变为黑色的化学方程式为
前,Ⅱ、Ⅲ中沉淀由白色变为黑色的化学方程式为(4)根据资料ⅱ,Ⅲ中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符原因:
原因一:可能是通入
 导致溶液的碱性减弱。
导致溶液的碱性减弱。原因二:可能是氧化剂过量,氧化剂将
 氧化为
氧化为  。
。①化学方程式表示可能导致溶液碱性减弱的原因
②取Ⅲ中放置后的
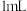 悬浊液,加入
悬浊液,加入 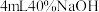 溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为
溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为 被
被③取Ⅱ中放置后的
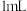 悬浊液,加入
悬浊液,加入  水,溶液紫色缓慢加深,发生的反应是
水,溶液紫色缓慢加深,发生的反应是
您最近半年使用:0次
名校
解题方法
6 . 下列离子方程式正确的是
A.实验室用大理石和稀盐酸制取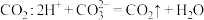 |
B.氯气与水反应: |
C.氯化铁溶液加入氨水: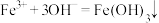 |
D.用氢氧化钠检验氯化铵溶液中铵根离子: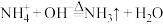 |
您最近半年使用:0次
名校
解题方法
7 . 实验小组同学制备KClO3并探究其性质,过程如下:

下列说法不正确 的是

下列说法
| A.可用饱和NaOH溶液净化氯气 |
B.生成KClO3的离子方程式为3Cl2+6OH- ClO ClO +5Cl-+3H2O +5Cl-+3H2O |
| C.推测若取无色溶液a于试管中,滴加稀H2SO4后再加入少量CCl4,下层液体变紫色 |
| D.上述实验说明碱性条件下氧化性:Cl2>KClO3,酸性条件下氧化性:Cl2<KClO3 |
您最近半年使用:0次
名校
8 . 下列解释事实的离子方程式不正确的是
| A.用过量氨水吸收烟气中的少量 SO2:NH3·H2O+SO2=NH4HSO3 |
B.铜与浓硝酸反应有红棕色气体生成:Cu+4H++2NO =Cu2++2NO2↑+2H2O =Cu2++2NO2↑+2H2O |
| C.将Cl2通入NaOH溶液中,得到漂白液:Cl2+2OH-=Cl-+C1O-+H2O |
D.常温下0.1mol/LNaClO的pH约为9.7:ClO-+H2O HClO+OH- HClO+OH- |
您最近半年使用:0次
名校
解题方法
9 . 下列离子方程式正确的是
A. 溶液通入氯气: 溶液通入氯气: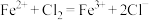 |
B.实验室制氯气尾气用 溶液吸收: 溶液吸收: |
C. 使澄清石灰水变浑浊: 使澄清石灰水变浑浊: |
D. 溶液和 溶液和 溶液混合: 溶液混合: |
您最近半年使用:0次
10 . 亚氯酸钠 是一种重要的含氯消毒剂,易溶于水,在碱性溶液中比较稳定,遇酸放出
是一种重要的含氯消毒剂,易溶于水,在碱性溶液中比较稳定,遇酸放出 。一种由
。一种由 制备
制备 晶体的实验装置如图(夹持装置略去)所示:
晶体的实验装置如图(夹持装置略去)所示:
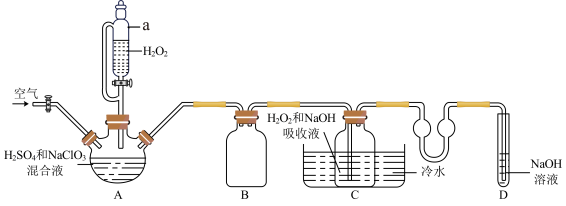
已知:①饱和 溶液中析出的晶体成分与温度的关系如下表所示:
溶液中析出的晶体成分与温度的关系如下表所示:
② 易溶于水,在温度过高、浓度过大时易发生分解。
易溶于水,在温度过高、浓度过大时易发生分解。
回答下列问题:
(1)装置A为 发生装置,其中发生反应的离子方程式为
发生装置,其中发生反应的离子方程式为_______ 。
(2) 在装置C中生成
在装置C中生成 ,化学反应方程式为
,化学反应方程式为_______ , 的另一个作用是
的另一个作用是_______ ,装置C中冷水的作用是_______ 。
(3)从装置C中获得 晶体的方法是:在
晶体的方法是:在_______ (填“温度范围”)、_______ (填“常压”、“减压”)蒸发结晶、_______ (填“趁热”、“冷却”)过滤,50℃左右热水洗涤,低于60℃条件下烘干,得到 晶体。
晶体。
 是一种重要的含氯消毒剂,易溶于水,在碱性溶液中比较稳定,遇酸放出
是一种重要的含氯消毒剂,易溶于水,在碱性溶液中比较稳定,遇酸放出 。一种由
。一种由 制备
制备 晶体的实验装置如图(夹持装置略去)所示:
晶体的实验装置如图(夹持装置略去)所示:
已知:①饱和
 溶液中析出的晶体成分与温度的关系如下表所示:
溶液中析出的晶体成分与温度的关系如下表所示:| 温度/℃ |  | 38~60 |  |
| 晶体成分 |  |  |  分解成 分解成 和 和 |
 易溶于水,在温度过高、浓度过大时易发生分解。
易溶于水,在温度过高、浓度过大时易发生分解。回答下列问题:
(1)装置A为
 发生装置,其中发生反应的离子方程式为
发生装置,其中发生反应的离子方程式为(2)
 在装置C中生成
在装置C中生成 ,化学反应方程式为
,化学反应方程式为 的另一个作用是
的另一个作用是(3)从装置C中获得
 晶体的方法是:在
晶体的方法是:在 晶体。
晶体。
您最近半年使用:0次


 溶液
溶液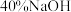 溶液
溶液

