解题方法
1 . 从海水中可提取多种化工原料,下图是工业上对海水的几项综合利用的示意图。试回答下列问题: 的化学方程式:
的化学方程式:___________ ,___________ ;
(2)以上海水的综合利用过程中,哪一种操作肯定会引起氧化还原反应的发生?___________ ;
(3)电解无水 可制取镁和氯气,其中副产品氯气和烧碱溶液可制得“84”消毒液,制“84”消毒液的离子方程式为
可制取镁和氯气,其中副产品氯气和烧碱溶液可制得“84”消毒液,制“84”消毒液的离子方程式为___________ ;
(4)海边盐碱地(含较多 、
、 )不利于植物生长,盐碱地产生碱性的原因:
)不利于植物生长,盐碱地产生碱性的原因:___________ (用离子方程式表示);农业上用石膏降低其碱性的反应原理:___________ (用化学方程式表示);
(5)用海滩上的贝壳制 ,而不从异地山中开凿石灰石制取,主要考虑到
,而不从异地山中开凿石灰石制取,主要考虑到___________ 问题。

 的化学方程式:
的化学方程式:(2)以上海水的综合利用过程中,哪一种操作肯定会引起氧化还原反应的发生?
(3)电解无水
 可制取镁和氯气,其中副产品氯气和烧碱溶液可制得“84”消毒液,制“84”消毒液的离子方程式为
可制取镁和氯气,其中副产品氯气和烧碱溶液可制得“84”消毒液,制“84”消毒液的离子方程式为(4)海边盐碱地(含较多
 、
、 )不利于植物生长,盐碱地产生碱性的原因:
)不利于植物生长,盐碱地产生碱性的原因:(5)用海滩上的贝壳制
 ,而不从异地山中开凿石灰石制取,主要考虑到
,而不从异地山中开凿石灰石制取,主要考虑到
您最近半年使用:0次
2 . 下列有关物质的工业制备反应正确的是
A.制烧碱:  |
B.炼铁:  |
C.制漂粉精: 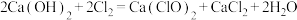 |
D.制乙烯: 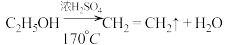 |
您最近半年使用:0次
名校
3 . 下列有关物质性质、用途的描述错误的是
A. 易液化,可用于制取漂白液 易液化,可用于制取漂白液 |
B. 有还原性,在葡萄酒中添加适量的 有还原性,在葡萄酒中添加适量的 能防止葡萄酒的氧化变质 能防止葡萄酒的氧化变质 |
C. 分解生成 分解生成 和 和 是吸热反应,故 是吸热反应,故 可用作阻燃剂 可用作阻燃剂 |
D.铁粉具有还原性,能够除去污水中的 、 、 |
您最近半年使用:0次
2024-04-17更新
|
413次组卷
|
5卷引用:广西壮族自治区部分学校2023-2024学年高三下学期教学质量监测联考(二模)化学试题
广西壮族自治区部分学校2023-2024学年高三下学期教学质量监测联考(二模)化学试题江西省部分地区2023-2024学年高三下学期3月月考化学试题甘肃省酒泉市九师联盟2023-2024学年高三下学期3月月考化学试题(已下线)题型6 元素及其化合物 化学实验基础(25题)-2024年高考化学常考点必杀300题(新高考通用)湖北省九师联盟2024届高三下学期3月质量检测(W-G)化学试卷
名校
4 . 回答下列问题
(1)过氧化钠与二氧化碳反应的化学方程式_____________ ,并用单线桥标出电子转移的方向和数目__________________ 。
(2)漂白粉的有效成分是______ (填化学式),制取漂白粉的化学方程式__________________ 。
(3)漂白粉长时间暴露在空气中就会失去效用,失效原因是(写出2个化学方程式)__________________ ;__________________ 。
(4)实验室用 制氯气的离子方程式
制氯气的离子方程式_______________ 。
(5)将钠投入到 溶液中,写出化学方程式
溶液中,写出化学方程式______________ 。
(6)除去碳酸钠中混有的碳酸氢钠应加入______ (填化学式)溶液,涉及到的反应的离子方程式为__________________ 。
(7)厨房里常用小苏打做糕点的发泡剂,写出其受热分解的化学方程式_________________ 。
(1)过氧化钠与二氧化碳反应的化学方程式
(2)漂白粉的有效成分是
(3)漂白粉长时间暴露在空气中就会失去效用,失效原因是(写出2个化学方程式)
(4)实验室用
 制氯气的离子方程式
制氯气的离子方程式(5)将钠投入到
 溶液中,写出化学方程式
溶液中,写出化学方程式(6)除去碳酸钠中混有的碳酸氢钠应加入
(7)厨房里常用小苏打做糕点的发泡剂,写出其受热分解的化学方程式
您最近半年使用:0次
解题方法
5 . 下列离子方程式与所给事实不相符的是
A.Cl2制备84消毒液(主要成分是NaClO):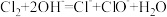 |
B.食醋去除水垢中的CaCO3: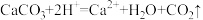 |
C.向次氯酸钙溶液通入足量二氧化碳: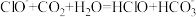 |
D.Na2S去除废水中的Hg2+: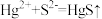 |
您最近半年使用:0次
解题方法
6 . 下列反应的离子方程式正确的是
A.等体积、等物质的量浓度的NH4HSO4溶液与NaOH溶液混合: +OH—=NH3·H2O +OH—=NH3·H2O |
| B.硫酸铜溶液中加入少量铁粉:3Cu2++2Fe=2Fe3++3Cu |
C.SO2通入酸性KMnO4溶液中:5SO2+2H2O+2 =5 =5 +4H++2Mn2+ +4H++2Mn2+ |
| D.工业制备漂白粉:2OH—+Cl2=Cl—+ClO—+H2O |
您最近半年使用:0次
名校
7 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置制备 和
和 ,探究其氧化还原性质。
,探究其氧化还原性质。

已知: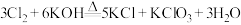
回答下列问题:
(1)盛装浓盐酸的仪器名称为________ 。 的作用
的作用________ 。
(2)b中试管内发生反应的还原剂和氧化剂的物质的量之比为________ 。 中反应的离子方程式是
中反应的离子方程式是________ 。
(3)用双线桥表示该实验制备氯气的化学方程式,并标注电子转移的方向和数目________ 。
(4)将氯气持续通入紫色石蕊试液中,溶液颜色呈如图变化:
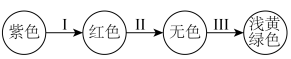
根据溶液变色情况,写出相应微粒的化学式,Ⅰ为________ 、Ⅱ为________ 、Ⅲ为________ 。
(5)某游泳池常用 来抑制藻类生长,工作人员一次错用
来抑制藻类生长,工作人员一次错用 消毒,因两种物质相互反应,使游泳池的藻类疯长。已知该反应产生了
消毒,因两种物质相互反应,使游泳池的藻类疯长。已知该反应产生了 和
和 ,写出相应的离子方程式
,写出相应的离子方程式________ 。
 和
和 ,探究其氧化还原性质。
,探究其氧化还原性质。
已知:
回答下列问题:
(1)盛装浓盐酸的仪器名称为
 的作用
的作用(2)b中试管内发生反应的还原剂和氧化剂的物质的量之比为
 中反应的离子方程式是
中反应的离子方程式是(3)用双线桥表示该实验制备氯气的化学方程式,并标注电子转移的方向和数目
(4)将氯气持续通入紫色石蕊试液中,溶液颜色呈如图变化:

根据溶液变色情况,写出相应微粒的化学式,Ⅰ为
(5)某游泳池常用
 来抑制藻类生长,工作人员一次错用
来抑制藻类生长,工作人员一次错用 消毒,因两种物质相互反应,使游泳池的藻类疯长。已知该反应产生了
消毒,因两种物质相互反应,使游泳池的藻类疯长。已知该反应产生了 和
和 ,写出相应的离子方程式
,写出相应的离子方程式
您最近半年使用:0次
2024-02-22更新
|
66次组卷
|
2卷引用:广西壮族自治区百色市2023-2024学年高一上学期1月期末化学试题
8 . 某化学兴趣小组欲在实验室探究氯气的性质及模拟工业制取漂白粉,设计了如下装置进行实验(已知:氯气几乎不溶于饱和食盐水)。回答下列问题:

(1)盛装浓盐酸的仪器名称是_______ ,将浓盐酸顺利滴入圆底烧瓶中的操作是_______ 。
(2)写出A中产生氯气的离子方程式:_______ 。
(3)装置B有安全瓶作用,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:_______ 。
(4)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入_______ (填字母)。
(5)D中反应的化学方程式为_______ 。
(6)使潮湿的 与E中
与E中 等物质的量反应,生成
等物质的量反应,生成 、气体
、气体 和另一种盐,写出该反应的化学方程式:
和另一种盐,写出该反应的化学方程式:_______ 。
(7)该兴趣小组用17.4g二氧化锰与足量的浓盐酸制备氯气,则理论上D中最多可制得次氯酸钙的质量是_______ g。

(1)盛装浓盐酸的仪器名称是
(2)写出A中产生氯气的离子方程式:
(3)装置B有安全瓶作用,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:
(4)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入
| a | b | c | d | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 浓硫酸 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(5)D中反应的化学方程式为
(6)使潮湿的
 与E中
与E中 等物质的量反应,生成
等物质的量反应,生成 、气体
、气体 和另一种盐,写出该反应的化学方程式:
和另一种盐,写出该反应的化学方程式:(7)该兴趣小组用17.4g二氧化锰与足量的浓盐酸制备氯气,则理论上D中最多可制得次氯酸钙的质量是
您最近半年使用:0次
解题方法
9 . 某校化学兴趣小组为研究 的性质,设计如图所示装置进行实验。装置D中夹持装置已略去,其中a为干燥的红色布条,b为湿润的红色布条。回答下列问题:
的性质,设计如图所示装置进行实验。装置D中夹持装置已略去,其中a为干燥的红色布条,b为湿润的红色布条。回答下列问题:

(1)仪器X的名称是_________ 。写出装置A中发生反应的化学方程式:_________ 。
(2)装置B的作用是_________ 。
(3)装置C的作用是________ ,可选用的试剂是_______ (填字母)。
a. 溶液 b.
溶液 b. 溶液 c.碱石灰 d.浓硫酸
溶液 c.碱石灰 d.浓硫酸
(4)装置D中的实验现象为________ 。
(5)若产生 足量,实验过程中装置E中的实验现象是
足量,实验过程中装置E中的实验现象是_________ 。
(6)有一种“地康法”制取氯气的反应原理如图所示:

①反应Ⅰ______ (填“是”或“不是”)氧化还原反应。
②在450℃条件下,反应Ⅱ的化学方程式为_____ 。
 的性质,设计如图所示装置进行实验。装置D中夹持装置已略去,其中a为干燥的红色布条,b为湿润的红色布条。回答下列问题:
的性质,设计如图所示装置进行实验。装置D中夹持装置已略去,其中a为干燥的红色布条,b为湿润的红色布条。回答下列问题:
(1)仪器X的名称是
(2)装置B的作用是
(3)装置C的作用是
a.
 溶液 b.
溶液 b. 溶液 c.碱石灰 d.浓硫酸
溶液 c.碱石灰 d.浓硫酸(4)装置D中的实验现象为
(5)若产生
 足量,实验过程中装置E中的实验现象是
足量,实验过程中装置E中的实验现象是(6)有一种“地康法”制取氯气的反应原理如图所示:

①反应Ⅰ
②在450℃条件下,反应Ⅱ的化学方程式为
您最近半年使用:0次
名校
10 . 某化学兴趣小组欲在实验室探究氯气的性质及模拟工业制取漂白粉,设计以下装置进行实验。
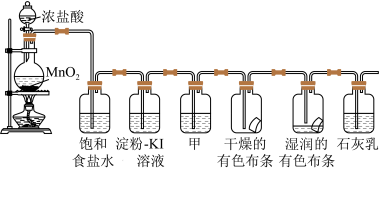
(1)圆底烧瓶内发生的化学方程式为___________ 。在该反应中,被氧化的元素是___________ ,氧化剂与还原剂的物质的量之比为___________ ,比较氧化剂和氧化产物的氧化性大小:___________ ,若产生0.1molCl2,则转移的电子数目为___________ ,该反应中浓盐酸体现了___________ 性质(选填字母编号)。
A.酸性 B.碱性 C.氧化性 D.还原性
(2)饱和食盐水的作用为___________ ,Cl2与石灰乳反应制取漂白粉的化学方程式为___________ 。
(3)若干燥的有色布条不褪色,湿润的有色布条褪色,则甲中盛放___________ (填名称)。
(4)某同学在实验室配制80mL质量分数为36.5%(密度为1.2g/cm3)的浓盐酸溶液用于上述实验。
①该同学应选择___________ mL的容量瓶,配制所得浓盐酸的浓度为___________ mol/L。
②若实验中出现以下情况,对所配溶液的物质的量浓度有何影响? (填“偏高”“偏低”或“无影响”)。容量瓶中原有少量蒸馏水___________ ;定容时俯视容量瓶瓶颈上的刻度线___________ ;向容量瓶中转移溶液时不慎将少量溶液溅出酒在容量瓶外面___________ 。
(5)将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当NaCl和NaClO3的物质的量之比为15:2时反应的离子方程式为___________ 。

(1)圆底烧瓶内发生的化学方程式为
A.酸性 B.碱性 C.氧化性 D.还原性
(2)饱和食盐水的作用为
(3)若干燥的有色布条不褪色,湿润的有色布条褪色,则甲中盛放
(4)某同学在实验室配制80mL质量分数为36.5%(密度为1.2g/cm3)的浓盐酸溶液用于上述实验。
①该同学应选择
②若实验中出现以下情况,对所配溶液的物质的量浓度有何影响? (填“偏高”“偏低”或“无影响”)。容量瓶中原有少量蒸馏水
(5)将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当NaCl和NaClO3的物质的量之比为15:2时反应的离子方程式为
您最近半年使用:0次



