1 . 下列生产生活中涉及的反应方程式正确的是
| A.用TiCl4制备TiCl4+(x+2)H2O=TiO2·xH2O↓+4HCl |
B.用食醋和淀粉-KI溶液检验加碘盐中的IO ,IO ,IO +5I-+6H+=3I2+3H2O +5I-+6H+=3I2+3H2O |
C.工业制硫酸时黄铁矿在足量氧气中煅烧:4FeS+15O2 8SO3+2Fe2O3 8SO3+2Fe2O3 |
| D.Cl2通入石灰乳中制漂白粉:Cl2+2OH-=Cl-+ClO-+H2O |
您最近半年使用:0次
2 . 部分含氯物质的分类与相应化合价关系如图所示。下列推断不合理的是
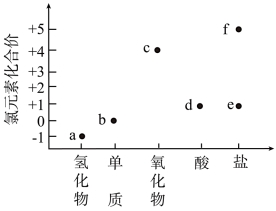

A.用气体b制取漂白粉: |
| B.b既具有氧化性,又具有还原性 |
| C.c可用于自来水消毒 |
| D.e或f分别与a的浓溶液反应均可制得b |
您最近半年使用:0次
3 . 下列变化不能直接一步实现的是
A(HCl)→B(Cl2)→C〔Ca(ClO)2〕→D(HClO)→E(CO2)
A(HCl)→B(Cl2)→C〔Ca(ClO)2〕→D(HClO)→E(CO2)
| A.A→B | B.B→C | C.C→D | D.D→E |
您最近半年使用:0次
4 . 如图是实验室制备氯气并进行相关性质检验的装置,实验装置如图:
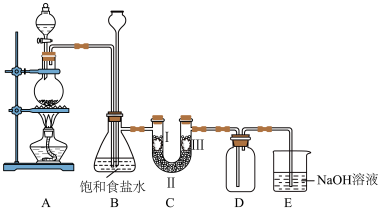
回答下列问题:
(1)①装置A中是用 和浓盐酸反应制备
和浓盐酸反应制备 ,其化学方程式为
,其化学方程式为________ 。
②B中加入饱和食盐水的目的________ 。
(2)装置B有安全瓶作用,监测实验进行时C中是否发生堵塞,请写出C发生堵塞时B中的现象________ 。
(3)设置装置C的实验目的是验证氯气是否具有漂白性,为此C中的Ⅰ、Ⅱ、Ⅲ依次应放入________ (从下表a、b、c、d中选择)。
(4)装置E的作用是________ ,发生的离子方程式是________ 。
(5)某同学设计实验探究“84”消毒液(主要成分NaClO)的漂白性。
Ⅰ.在2mL“84”消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.在2mL“84”消毒液中加入2mL醋酸后,放入红色纸片,观察到纸片迅速褪色。
Ⅲ.在不同温度时,测得“84”消毒液ORP值随时间的变化曲线如图所示。
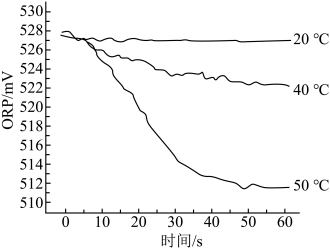
已知:ORP表示水溶液中物质的氧化性或还原性强弱,ORP值越大,氧化性越强。
①实验Ⅰ、Ⅱ现象不同的原因是________ 。
②实验Ⅲ中,随时间的变化ORP值不同的原因可能是________ 。

回答下列问题:
(1)①装置A中是用
 和浓盐酸反应制备
和浓盐酸反应制备 ,其化学方程式为
,其化学方程式为②B中加入饱和食盐水的目的
(2)装置B有安全瓶作用,监测实验进行时C中是否发生堵塞,请写出C发生堵塞时B中的现象
(3)设置装置C的实验目的是验证氯气是否具有漂白性,为此C中的Ⅰ、Ⅱ、Ⅲ依次应放入
选项 | a | b | c | d |
Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
Ⅱ | 碱石灰 | 无水氯化钙 | 碱石灰 | 无水氯化钙 |
Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(4)装置E的作用是
(5)某同学设计实验探究“84”消毒液(主要成分NaClO)的漂白性。
Ⅰ.在2mL“84”消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.在2mL“84”消毒液中加入2mL醋酸后,放入红色纸片,观察到纸片迅速褪色。
Ⅲ.在不同温度时,测得“84”消毒液ORP值随时间的变化曲线如图所示。

已知:ORP表示水溶液中物质的氧化性或还原性强弱,ORP值越大,氧化性越强。
①实验Ⅰ、Ⅱ现象不同的原因是
②实验Ⅲ中,随时间的变化ORP值不同的原因可能是
您最近半年使用:0次
2024-02-10更新
|
122次组卷
|
3卷引用:内蒙古呼和浩特市2023-2024学年高一上学期期末教学质量检测化学试卷
名校
5 . 氯气跟氢氧化钾溶液在一定条件下发生反应:Cl2+KOH→KX+KY+H2O(未配平),KX在一定条件下能自身反应:KX→KY+KZ(未配平,KY与KZ的物质的量之比为1∶3),以上KX、KY、KZ均是含氯元素的一元酸的钾盐,由以上条件推知在KX中氯元素的化合价是
| A.+1 | B.+3 | C.+5 | D.+7 |
您最近半年使用:0次
6 . 部分常见含氯物质的分类与相应化合价关系如图所示,下列推断不合理的是


| A.a可以做氧化剂,也能被氯化 |
| B.d的浓溶液与c的固体一起使用可增强漂白效果 |
C.实验室可通过加热 与d的浓溶液制得a 与d的浓溶液制得a |
| D.可存在a→c→e→d→b→a的循环转化关系 |
您最近半年使用:0次
7 . 某校化学兴趣小组学习了“氯气的实验室制法”后,利用如图所示实验装置对 的制备及性质进行探究。回答下列问题:
的制备及性质进行探究。回答下列问题:

(1)仪器a的名称为________ 。
(2)实验室若选用 固体和浓盐酸在常温条件下制取干燥的
固体和浓盐酸在常温条件下制取干燥的 ,则选用的发生装置为
,则选用的发生装置为________ (填“A”或“B”)。
(3)装置C的主要作用为________ ;装置D是用于干燥 ,故装置D中的试剂为
,故装置D中的试剂为________ (填化学式)。
(4)用装置E收集 ,进气口为
,进气口为________ (填“b”或“c”)。
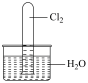
(5)工业上一般将 通入石灰乳中制取含氯漂白粉,同学们利用如图装置进行实验。
通入石灰乳中制取含氯漂白粉,同学们利用如图装置进行实验。
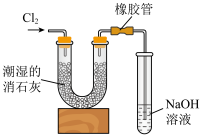
已知:① 与潮湿的消石灰反应是放热反应;
与潮湿的消石灰反应是放热反应;
②温度较高时, 与潮湿
与潮湿 的反应方程式为
的反应方程式为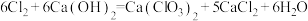 。
。
发现实验所得 产率较低,可能的原因是
产率较低,可能的原因是________ 。
 的制备及性质进行探究。回答下列问题:
的制备及性质进行探究。回答下列问题:
(1)仪器a的名称为
(2)实验室若选用
 固体和浓盐酸在常温条件下制取干燥的
固体和浓盐酸在常温条件下制取干燥的 ,则选用的发生装置为
,则选用的发生装置为(3)装置C的主要作用为
 ,故装置D中的试剂为
,故装置D中的试剂为(4)用装置E收集
 ,进气口为
,进气口为(5)工业上一般将
 通入石灰乳中制取含氯漂白粉,同学们利用如图装置进行实验。
通入石灰乳中制取含氯漂白粉,同学们利用如图装置进行实验。
已知:①
 与潮湿的消石灰反应是放热反应;
与潮湿的消石灰反应是放热反应;②温度较高时,
 与潮湿
与潮湿 的反应方程式为
的反应方程式为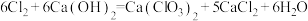 。
。发现实验所得
 产率较低,可能的原因是
产率较低,可能的原因是
您最近半年使用:0次
名校
解题方法
8 . 利用 氧化绿色的
氧化绿色的 浓强碱溶液制备
浓强碱溶液制备 的装置如下图所示(加热、夹持装置略):
的装置如下图所示(加热、夹持装置略):______________________________ 。
(2)如果d中用足量的NaOH溶液吸收多余氯气,写出相应的离子方程式:______________________________ 。
(3)一段时间后,当仪器C中溶液由绿色完全转变为紫红色即停止通氯气。熄灭A处酒精灯,再____________________ ,待冷却后拆除装置。
(4)某同学在实验中发现,若用稀盐酸代替浓盐酸与 混合加热没有氯气生成,欲探究该条件下不能生成氯气的原因,该同学提出下列假设:
混合加热没有氯气生成,欲探究该条件下不能生成氯气的原因,该同学提出下列假设:
假设1: 的浓度不够大;
的浓度不够大;
假设2:____________________ ;
假设3: 和
和 的浓度均不够大。
的浓度均不够大。
设计实验方案,进行实验。在下表中写出实验步骤以及预期现象和结论。(限选实验试剂:蒸馏水、浓 、NaCl固体、
、NaCl固体、 固体、稀盐酸、
固体、稀盐酸、 溶液、淀粉-KI溶液)
溶液、淀粉-KI溶液)
 氧化绿色的
氧化绿色的 浓强碱溶液制备
浓强碱溶液制备 的装置如下图所示(加热、夹持装置略):
的装置如下图所示(加热、夹持装置略):
(2)如果d中用足量的NaOH溶液吸收多余氯气,写出相应的离子方程式:
(3)一段时间后,当仪器C中溶液由绿色完全转变为紫红色即停止通氯气。熄灭A处酒精灯,再
(4)某同学在实验中发现,若用稀盐酸代替浓盐酸与
 混合加热没有氯气生成,欲探究该条件下不能生成氯气的原因,该同学提出下列假设:
混合加热没有氯气生成,欲探究该条件下不能生成氯气的原因,该同学提出下列假设:假设1:
 的浓度不够大;
的浓度不够大;假设2:
假设3:
 和
和 的浓度均不够大。
的浓度均不够大。设计实验方案,进行实验。在下表中写出实验步骤以及预期现象和结论。(限选实验试剂:蒸馏水、浓
 、NaCl固体、
、NaCl固体、 固体、稀盐酸、
固体、稀盐酸、 溶液、淀粉-KI溶液)
溶液、淀粉-KI溶液)实验步骤 | 预期现象与结论 |
步骤1:取少量 稀盐酸于试管A中,加入少量 稀盐酸于试管A中,加入少量 ,滴加几滴浓硫酸,充分振荡,塞紧带导管的胶塞,导管插入淀粉-KI溶液中,加热 ,滴加几滴浓硫酸,充分振荡,塞紧带导管的胶塞,导管插入淀粉-KI溶液中,加热 | ①若淀粉-KI溶液变蓝,则假设1成立 ②若淀粉-KI溶液不变蓝,则假设2或假设3成立 |
步骤2:取少量 稀盐酸于试管B中,加入少量 稀盐酸于试管B中,加入少量 ,加入少量NaCl固体,充分振荡,塞紧带导管的胶塞,导管插入淀粉-KI溶液中,加热 ,加入少量NaCl固体,充分振荡,塞紧带导管的胶塞,导管插入淀粉-KI溶液中,加热 | ①若淀粉-KI溶液变盐,则 ②若淀粉-KI溶液不变蓝,结合步骤1中的结论②,则 |
您最近半年使用:0次
2023-12-20更新
|
43次组卷
|
2卷引用:内蒙古自治区乌兰浩特第一中学2023-2024学年高一上学期第二次月考化学试题
9 . 下列化学反应对应的离子方程式正确的是
A.在 溶液中通入少量 溶液中通入少量 : :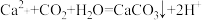 |
B.钠与 溶液反应: 溶液反应: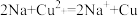 |
C.过氧化钠与水的反应: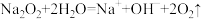 |
D.氯气与氢氧化钙溶液的反应: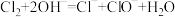 |
您最近半年使用:0次
2023-12-11更新
|
36次组卷
|
2卷引用:内蒙古赤峰市元宝山区第一中学2023-2024学年高一上学期期中考试化学试题
10 . 某同学用下列装置进行有关 的实验。下列说法
的实验。下列说法不正确 的是
 的实验。下列说法
的实验。下列说法| A | B | C | D |
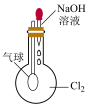 |  | 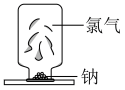 |  |
若气球变瘪,证明 可与 可与 溶液反应 溶液反应 | 证明氯气无漂白作用,氯水有漂白作用 | 剧烈燃烧,产生大量白烟 | 证明 可溶于水 可溶于水 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-11-05更新
|
435次组卷
|
3卷引用:内蒙古赤峰二中2023-2024学年高一上学期第二次月考化学试题



