解题方法
1 . 84消毒液的有效成分为
A. | B. | C. | D. |
您最近半年使用:0次
名校
解题方法
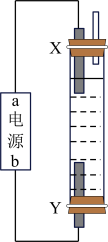
2 . 利用氢一氧燃料电池可以充当电源电解饱和食盐水制备84消毒液(如图)。则X是_____ (填电极名称),Y极电极反应式为_____ 。
您最近半年使用:0次
3 . 目前支原体肺炎流行,及时消毒有利于降低感染几率。常用的消毒剂有双氧水、医用酒精以及含氯消毒剂等,其中含氯消毒剂的家族最庞大、应用最广泛。
(1)次氯酸钠( )为“84”消毒液的有效成分,常温下用烧碱溶液吸收
)为“84”消毒液的有效成分,常温下用烧碱溶液吸收 可制备“84”消毒液,反应的化学方程式为
可制备“84”消毒液,反应的化学方程式为___________ 。
(2)但在巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿,一种可能原因是 与
与 反应产生
反应产生 促进藻类快速生长,该反应中氧化剂是
促进藻类快速生长,该反应中氧化剂是___________ ,若生成标况下44.8L的 ,转移电子的数目为
,转移电子的数目为___________ 。
(3)如果在不同温度、浓度的条件下, 与
与 溶液的反应,可以生成
溶液的反应,可以生成 或
或 。现将氯气缓缓通入冷
。现将氯气缓缓通入冷 溶液,当溶液中含有的
溶液,当溶液中含有的 与
与 的物质的量为1:1时,
的物质的量为1:1时,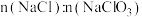 为
为___________ ,整个过程,参加反应所需 与氯气的物质的量之比为
与氯气的物质的量之比为___________ 。
若将 通入含amol
通入含amol 的溶液中,发生上述过程,回答下列问题:
的溶液中,发生上述过程,回答下列问题:
(4) 与
与 的物质的量之和可能为
的物质的量之和可能为 amol,该说法
amol,该说法___________ 。
A.正确 B.错误
(5)反应中转移电子的物质的量可能为___________。
亚氯酸钠( )为便携式消毒除菌卡的主要活性成分,一种制备
)为便携式消毒除菌卡的主要活性成分,一种制备 粗产品的工艺流程如下图,已知,纯
粗产品的工艺流程如下图,已知,纯 易分解爆炸,一般用空气稀释到10%以下。
易分解爆炸,一般用空气稀释到10%以下。
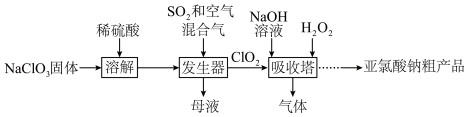
(6) 在发生器中发生
在发生器中发生________ (氧化或还原)反应,该反应的还原产物为_________ ,吸收塔中温度不宜过高,否则会导致 产率下降,原因是
产率下降,原因是___________ 。
(7)“有效氯含量”的定义是:每克含氯消毒剂的氧化能力(即得电子数)相当于多少克 的氧化能力(氯元素均被还原至
的氧化能力(氯元素均被还原至 价),则亚氯酸钠
价),则亚氯酸钠 的有效氯含量为
的有效氯含量为___________ 。(保留两位小数)。
(1)次氯酸钠(
 )为“84”消毒液的有效成分,常温下用烧碱溶液吸收
)为“84”消毒液的有效成分,常温下用烧碱溶液吸收 可制备“84”消毒液,反应的化学方程式为
可制备“84”消毒液,反应的化学方程式为(2)但在巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿,一种可能原因是
 与
与 反应产生
反应产生 促进藻类快速生长,该反应中氧化剂是
促进藻类快速生长,该反应中氧化剂是 ,转移电子的数目为
,转移电子的数目为(3)如果在不同温度、浓度的条件下,
 与
与 溶液的反应,可以生成
溶液的反应,可以生成 或
或 。现将氯气缓缓通入冷
。现将氯气缓缓通入冷 溶液,当溶液中含有的
溶液,当溶液中含有的 与
与 的物质的量为1:1时,
的物质的量为1:1时,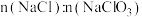 为
为 与氯气的物质的量之比为
与氯气的物质的量之比为若将
 通入含amol
通入含amol 的溶液中,发生上述过程,回答下列问题:
的溶液中,发生上述过程,回答下列问题:(4)
 与
与 的物质的量之和可能为
的物质的量之和可能为 amol,该说法
amol,该说法A.正确 B.错误
(5)反应中转移电子的物质的量可能为___________。
A. amol amol | B. amol amol | C. amol amol | D. amol amol |
亚氯酸钠(
 )为便携式消毒除菌卡的主要活性成分,一种制备
)为便携式消毒除菌卡的主要活性成分,一种制备 粗产品的工艺流程如下图,已知,纯
粗产品的工艺流程如下图,已知,纯 易分解爆炸,一般用空气稀释到10%以下。
易分解爆炸,一般用空气稀释到10%以下。
(6)
 在发生器中发生
在发生器中发生 产率下降,原因是
产率下降,原因是(7)“有效氯含量”的定义是:每克含氯消毒剂的氧化能力(即得电子数)相当于多少克
 的氧化能力(氯元素均被还原至
的氧化能力(氯元素均被还原至 价),则亚氯酸钠
价),则亚氯酸钠 的有效氯含量为
的有效氯含量为
您最近半年使用:0次
名校
解题方法
4 . 某学习小组用MnO2和浓盐酸共热制取氯气,再用氯气与潮湿的消石灰反应制取漂白粉(这是一个放热反应)。
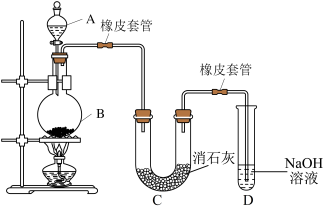
(1)圆底烧瓶内发生反应的化学方程式为_______ ;
(2)漂粉精在空气中起漂白作用的原理是_______ (用化学方程式表示)。
(3)此实验Ca(ClO)2产率太低。经分析发现,主要原因是在U形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是_______ 。
②试判断另一个副反应:_______ (用化学方程式表示)。

(1)圆底烧瓶内发生反应的化学方程式为
(2)漂粉精在空气中起漂白作用的原理是
(3)此实验Ca(ClO)2产率太低。经分析发现,主要原因是在U形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是
②试判断另一个副反应:
您最近半年使用:0次
5 . 工业上以晒盐后的卤水为原料进行提溴,主要流程如下:
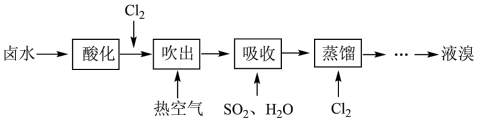
(1)卤水呈碱性,在通入Cl2先需先酸化,原因是___________ 。
(2)向酸化后的卤水中通入Cl2时发生反应的离子方程式为___________ 。
(3)已知吸收反应的化学方程式为:SO2+Br2+2H2O=H2SO4+2HBr
①设立“吸收”步骤的目的是___________ 。
②由该反应可知关于物质氧化性和还原性比较正确的是___________ 。
A.氧化性:Br2>H2SO4 B.还原性:SO2>H2SO4
C.氧化性:Br2>HBr D.还原性:HBr>H2SO4
③有人提出“吸收”步骤也可以用有机溶剂,下列有机溶剂适用的是___________ 。
A.苯 B.四氯化碳 C.植物油 D.酒精
(4)蒸馏时应控制温度不超过100℃,原因是___________ 。
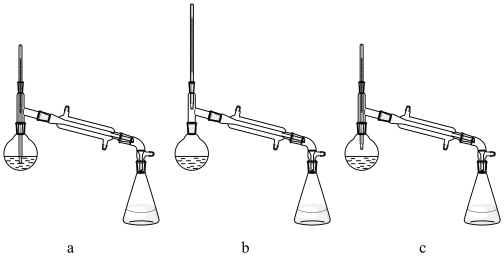
(5)下图的实验室蒸馏操作中,仪器选择及安装都正确的是___________ 。
(6)经该方法处理后,1m3海水最终得到38.4gBr2,若总提取率为60%,则原海水中溴离子的浓度是___________ mmol/L (毫摩尔/L)。

(1)卤水呈碱性,在通入Cl2先需先酸化,原因是
(2)向酸化后的卤水中通入Cl2时发生反应的离子方程式为
(3)已知吸收反应的化学方程式为:SO2+Br2+2H2O=H2SO4+2HBr
①设立“吸收”步骤的目的是
②由该反应可知关于物质氧化性和还原性比较正确的是
A.氧化性:Br2>H2SO4 B.还原性:SO2>H2SO4
C.氧化性:Br2>HBr D.还原性:HBr>H2SO4
③有人提出“吸收”步骤也可以用有机溶剂,下列有机溶剂适用的是
A.苯 B.四氯化碳 C.植物油 D.酒精
(4)蒸馏时应控制温度不超过100℃,原因是
(5)下图的实验室蒸馏操作中,仪器选择及安装都正确的是

(6)经该方法处理后,1m3海水最终得到38.4gBr2,若总提取率为60%,则原海水中溴离子的浓度是
您最近半年使用:0次
名校
6 . 二氯异氰尿酸钠(NaC3N3O3Cl2)是一种高效广谱杀菌消毒剂,它常温下为白色固体,难溶于冷水。工业上合成二氯异氰尿酸钠的方法有多种,其中NaClO法是向NaOH溶液通入Cl2产生高浓度NaClO溶液,然后与氰尿酸(C3H3N3O3)反应制取二氯异氰尿酸钠:2NaClO+C3H3N3O3=NaC3N3O3Cl2+NaOH+H2O。
(1)从下面选择所需装置完成实验,按气流从左至右,导管口连接顺序为______ (填小写字母)。
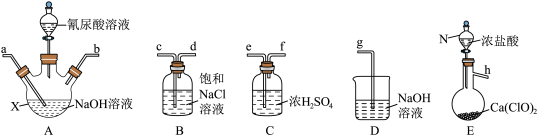
(2)若发现实际操作过程中仪器N中浓盐酸不易流下,可将仪器N换为_________ 。
(3)装置A中制备NaClO溶液完成的现象是___________ ,在加氰尿酸溶液过程仍需不断通入Cl2的理由是___________ 。
(4)有效氯含量是判断产品质量的标准。实验采用碘量法测定产物有效氯的含量,原理为: +H++2H2O=C3H3N3O3+2HClO,HClO+2I-+H+=I2+Cl-+H2O,
+H++2H2O=C3H3N3O3+2HClO,HClO+2I-+H+=I2+Cl-+H2O, ,准确称取1.120g样品,配成250mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;加入0.1000mol/LNa2S2O3溶液20.00mL恰好完全反应。
,准确称取1.120g样品,配成250mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;加入0.1000mol/LNa2S2O3溶液20.00mL恰好完全反应。
①配制样品溶液时,需要用到的玻璃仪器除烧杯、玻璃棒外,还需要___________ 。
②二氯异氰尿酸钠优质品要求有效氯大于60%,通过计算判断该样品是否为优质品________ 。( 该样品的有效氯  )(写出计算过程)
)(写出计算过程)
③若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值______ (填“偏高”或“偏低”)。
(5)高铁酸钾是一种重要的多功能绿色净水剂,暗紫色具有金属光泽的粉末,无臭无味,干燥品在室温下稳定,在强碱溶液中稳定。
①配平K2FeO4与水反应的化学方程式,并用单线桥标出电子转移方向和数目________ 。___K2FeO4+____H2O=___Fe(OH)3胶体+____O2↑+____KOH,被还原的元素是___________ 。
②结合高铁酸钾的性质,说明它是一种多功能绿色净水剂的原因:_________ 。
(1)从下面选择所需装置完成实验,按气流从左至右,导管口连接顺序为

(2)若发现实际操作过程中仪器N中浓盐酸不易流下,可将仪器N换为
(3)装置A中制备NaClO溶液完成的现象是
(4)有效氯含量是判断产品质量的标准。实验采用碘量法测定产物有效氯的含量,原理为:
 +H++2H2O=C3H3N3O3+2HClO,HClO+2I-+H+=I2+Cl-+H2O,
+H++2H2O=C3H3N3O3+2HClO,HClO+2I-+H+=I2+Cl-+H2O, ,准确称取1.120g样品,配成250mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;加入0.1000mol/LNa2S2O3溶液20.00mL恰好完全反应。
,准确称取1.120g样品,配成250mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;加入0.1000mol/LNa2S2O3溶液20.00mL恰好完全反应。①配制样品溶液时,需要用到的玻璃仪器除烧杯、玻璃棒外,还需要
②二氯异氰尿酸钠优质品要求有效氯大于60%,通过计算判断该样品是否为优质品
 )(写出计算过程)
)(写出计算过程)③若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值
(5)高铁酸钾是一种重要的多功能绿色净水剂,暗紫色具有金属光泽的粉末,无臭无味,干燥品在室温下稳定,在强碱溶液中稳定。
①配平K2FeO4与水反应的化学方程式,并用单线桥标出电子转移方向和数目
②结合高铁酸钾的性质,说明它是一种多功能绿色净水剂的原因:
您最近半年使用:0次
名校
7 . 新型冠状病毒肺炎爆发以来,各类杀菌消毒剂逐渐被人们所认识和使用。下列是常见的几种消毒剂:①“84”消毒液(有效成分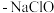 );②
);② (在水中一部分可以电离出正、负离子);③漂白粉;④
(在水中一部分可以电离出正、负离子);③漂白粉;④ ⑤
⑤ ;⑥碘酒;⑦
;⑥碘酒;⑦ 酒精;⑧过氧乙酸
酒精;⑧过氧乙酸 ⑨高铁酸钠
⑨高铁酸钠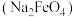 。回答下列问题:
。回答下列问题:
(1)上述杀菌消毒剂___________ (填序号)属于电解质,___________ (填序号)属于非电解质。“84”消毒液中有效成分的电离方程式为___________ 。
(2)巴西奥运会期间,由于工作人员将“84"消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能原因是NaClO与H2O2反应产生O2促进藻类快速生长。该反应说明氧化性:NaClO___________ H2O2(填“>”或“<”)。
(3)若混合使用“洁厕灵”(盐酸是成分之一)与84消毒液会产生氯气。原因是___________ (用离子方程式表示)。
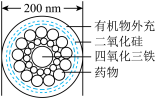
(4)如图是中国科学院上海硅酸盐研究所研发的“纳米药物分子运输车”,可提高肿瘤的治疗效果。以下说法不正确的是___________。
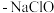 );②
);② (在水中一部分可以电离出正、负离子);③漂白粉;④
(在水中一部分可以电离出正、负离子);③漂白粉;④ ⑤
⑤ ;⑥碘酒;⑦
;⑥碘酒;⑦ 酒精;⑧过氧乙酸
酒精;⑧过氧乙酸 ⑨高铁酸钠
⑨高铁酸钠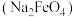 。回答下列问题:
。回答下列问题:(1)上述杀菌消毒剂
(2)巴西奥运会期间,由于工作人员将“84"消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能原因是NaClO与H2O2反应产生O2促进藻类快速生长。该反应说明氧化性:NaClO
(3)若混合使用“洁厕灵”(盐酸是成分之一)与84消毒液会产生氯气。原因是
(4)如图是中国科学院上海硅酸盐研究所研发的“纳米药物分子运输车”,可提高肿瘤的治疗效果。以下说法不正确的是___________。

| A.葡萄糖等大多数含碳化合物属于有机物 |
| B.该“纳米药物分子车"属于混合物 |
| C.该“纳米药物分子车”分散于水后能够透过半透膜 |
| D.该“纳米药物分子车”中的二氧化硅和四氧化三铁属于氧化物 |
您最近半年使用:0次
8 . 某化学兴趣小组欲在实验室探究氯气的性质及模拟工业制取84消毒液,设计了如图装置进行实验。

(1)圆底烧瓶内发生的化学反应方程式为___________ ,分液漏斗上的导管作用为___________ 。
(2)饱和食盐水的作用为___________ 。
(3)甲同学想要 漂白条件,为达到探究目的,装置还需补充完整,请在虚线框中画出你认为合适的常见化学仪器并标注所需试剂。能说明湿润的氯气具有漂白性的实验现象是
漂白条件,为达到探究目的,装置还需补充完整,请在虚线框中画出你认为合适的常见化学仪器并标注所需试剂。能说明湿润的氯气具有漂白性的实验现象是___________ 。
(4)该装置中的多孔球泡作用为___________ 。利用最后的吸收装置可以制取84消毒液,化学方程式为___________ 。
(5)已知在加热条件下会发生反应: ,根据此信息写出此加热条件下
,根据此信息写出此加热条件下 与NaOH溶液反应的方程式
与NaOH溶液反应的方程式___________ 。
84消毒液中含氯成分浓度与pH的关系图:
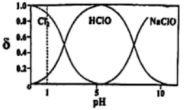
(6)生产84消毒液时需NaOH过量,从图像角度解释原因:___________ ,如果加入盐酸调节溶液pH=1,试写出发生反应的化学方程式___________ 。

(1)圆底烧瓶内发生的化学反应方程式为
(2)饱和食盐水的作用为
(3)甲同学想要
 漂白条件,为达到探究目的,装置还需补充完整,请在虚线框中画出你认为合适的常见化学仪器并标注所需试剂。能说明湿润的氯气具有漂白性的实验现象是
漂白条件,为达到探究目的,装置还需补充完整,请在虚线框中画出你认为合适的常见化学仪器并标注所需试剂。能说明湿润的氯气具有漂白性的实验现象是(4)该装置中的多孔球泡作用为
(5)已知在加热条件下会发生反应:
 ,根据此信息写出此加热条件下
,根据此信息写出此加热条件下 与NaOH溶液反应的方程式
与NaOH溶液反应的方程式84消毒液中含氯成分浓度与pH的关系图:

(6)生产84消毒液时需NaOH过量,从图像角度解释原因:
您最近半年使用:0次
9 . 实验室用浓盐酸、二氧化锰共热制氯气,并用氯气制取氯酸钾、次氯酸钠,并验证氯水的性质。

(1)写出实验室用装置①制备氯气的反应方程式___________ 。
(2)有同学认为①②装置之间应加入一盛有饱和食盐水的洗气瓶,则此洗气瓶的作用是___________ 。
(3)图一中②的试管中盛有15mL 30%的KOH溶液;③的试管中盛有15mL 8%的NaOH溶液,并置于冰水浴中;写出制取次氯酸钠的反应方程式___________ ,比较制取次氯酸钠和氯酸钾的反应条件,试总结两条差异:①___________ ;②___________ 。
(4)④的试管中加有紫色石蕊试液,实验过程中可观察到的现象是___________ ,导致该现象的相应微粒为___________ 。
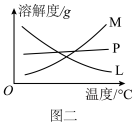
(5)反应完毕冷却后,②的试管中有大量晶体析出,图二中符合该晶体溶解度随温度变化规律的曲线是___________ (选填字母);从②的试管中分离该晶体的操作是___________ (填写实验操作名称)。
(6)含氯消毒剂的消毒效果用有效氯表示,有效氯指的是与浓盐酸反应产生Cl2的质量与原消毒液质量的比值。计算10% NaClO溶液的有效氯___________ (保留三位小数)。
(7)传统工业电解饱和食盐水所得的烧碱中往往混有食盐,若要检验其中混有氯离子,简述实验方法、现象和结论___________ 。

(1)写出实验室用装置①制备氯气的反应方程式
(2)有同学认为①②装置之间应加入一盛有饱和食盐水的洗气瓶,则此洗气瓶的作用是
(3)图一中②的试管中盛有15mL 30%的KOH溶液;③的试管中盛有15mL 8%的NaOH溶液,并置于冰水浴中;写出制取次氯酸钠的反应方程式
(4)④的试管中加有紫色石蕊试液,实验过程中可观察到的现象是
(5)反应完毕冷却后,②的试管中有大量晶体析出,图二中符合该晶体溶解度随温度变化规律的曲线是

(6)含氯消毒剂的消毒效果用有效氯表示,有效氯指的是与浓盐酸反应产生Cl2的质量与原消毒液质量的比值。计算10% NaClO溶液的有效氯
(7)传统工业电解饱和食盐水所得的烧碱中往往混有食盐,若要检验其中混有氯离子,简述实验方法、现象和结论
您最近半年使用:0次
名校
解题方法
10 . 漂白粉等氯系消毒剂与洁厕灵(主要成分为浓盐酸)等酸性洗涤剂相遇,会产生有毒的氯气。
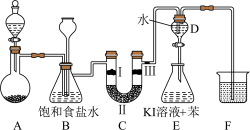
(1)写出A中制备氯气反应的化学方程式:_______ 。
(2)装置B中饱和食盐水的作用是_______ 。同时装置B亦可监测C中是否发生堵塞,请写出发生堵塞时B中的现象:_______ 。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅲ处应依次放入_______ 、_______ (选填序号,下同),Ⅱ处可以放入_______ 。
①干燥的的有色布条②湿润的有色布条③碱石灰④浓硫酸⑤无水氯化钙
(4)装置D、E的目的探究氯气与水和KI溶液的反应。反应一段时间后,装置D中的现象是_______ 。
(5)小组通过查阅资料了解到,氯气与碱溶液在常温下反应,主要产物是 和
和 ,在75℃以上主要产物是
,在75℃以上主要产物是 和
和 。
。
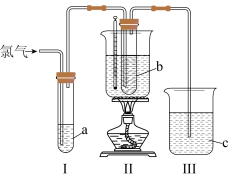
其中,a、c为NaOH溶液,b为浓KOH溶液。检查装置气密性后,添加药品,待装置Ⅱ烧杯中的水温升至75℃后,通入氯气。回答下列问题:
①写出试管a中制备漂白液的化学方程式:_______ 。
②反应结束后,试管b的溶液中除产物 外,还混有的杂质有
外,还混有的杂质有_______ 和_______ 。提纯 的方法是
的方法是_______ 。
③若通入的氯气中混有HCl气体,则对此制备实验的影响是_______ 。

(1)写出A中制备氯气反应的化学方程式:
(2)装置B中饱和食盐水的作用是
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅲ处应依次放入
①干燥的的有色布条②湿润的有色布条③碱石灰④浓硫酸⑤无水氯化钙
(4)装置D、E的目的探究氯气与水和KI溶液的反应。反应一段时间后,装置D中的现象是
(5)小组通过查阅资料了解到,氯气与碱溶液在常温下反应,主要产物是
 和
和 ,在75℃以上主要产物是
,在75℃以上主要产物是 和
和 。
。
其中,a、c为NaOH溶液,b为浓KOH溶液。检查装置气密性后,添加药品,待装置Ⅱ烧杯中的水温升至75℃后,通入氯气。回答下列问题:
①写出试管a中制备漂白液的化学方程式:
②反应结束后,试管b的溶液中除产物
 外,还混有的杂质有
外,还混有的杂质有 的方法是
的方法是③若通入的氯气中混有HCl气体,则对此制备实验的影响是
您最近半年使用:0次



