解题方法
1 . 下列所涉及的离子方程式书写正确的是
| 选项 | 用途或者制备 | 离子方程式 |
| A | 用稀硫酸清洗铁锈 |  |
| B | 大理石与稀盐酸反应制备二氧化碳 | 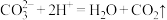 |
| C | 用氢氧化钠溶液吸收氯气 |  |
| D | 氧化铝与氢氧化钠溶液 |  |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
2 . X、Y、Z、W为原子序数依次增大的四种短周期元素。X与Z同族,Z的核电荷数是X的2倍,Y原子K层电子数与M层电子数的乘积等于其L层的电子数,下列说法不正确的是
| A.非金属性:X>Z>Y |
| B.Y、W的单质均可与NaOH溶液反应 |
| C.W的单质具有漂白性 |
D.化合物 中各原子最外层均满足8电子稳定结构 中各原子最外层均满足8电子稳定结构 |
您最近半年使用:0次
3 . 如图所示,反应①为常温下的反应,A、C、D中均含有氯元素,且A中氯元素的化合价介于C和D中氯元素的化合价之间,E在常温下为无色无味的液体,F是淡黄色固体,C为常见的无色气体。请据图回答下列问题:
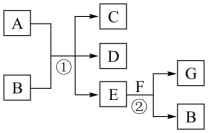
(1)A的化学式为_______ 。
(2)写出反应①的化学方程式:_______ 。
(3)写出反应②的化学方程式:_______ 。
(4)已知A是一种重要的化工原料,在工农业生产和生活中有着重要的应用。A与石灰乳反应制得的漂白粉的有效成分是_______ (填化学式),该物质在空气中久置失效的原因是_______ (用化学方程式表示)。

(1)A的化学式为
(2)写出反应①的化学方程式:
(3)写出反应②的化学方程式:
(4)已知A是一种重要的化工原料,在工农业生产和生活中有着重要的应用。A与石灰乳反应制得的漂白粉的有效成分是
您最近半年使用:0次
4 . 实验室制取A并进一步制取无水FeCl3的实验装置如图所示。
已知:无水FeCl3在空气中易与水发生作用,加热易升华。
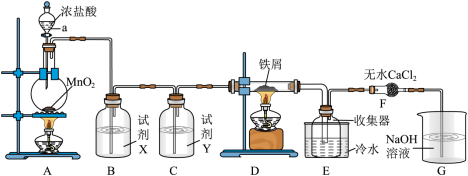
回答下列问题:
(1)仪器a的名称是_______ ,装置A所发生的氧化还原反应中,氧化剂与还原剂的物质的量之比为_______ 。
(2)试剂X是_______ 。
(3)装置F中无水CaCl2的作用是_______
(4)某温度下,将氯气通入G装置中,反应得到NaCl,NaClO和NaClO3的混合溶液,经测定ClO-与ClO 的物质的量之比为4∶1,写出该反应总的离子方程式:
的物质的量之比为4∶1,写出该反应总的离子方程式:_______ 。
已知:无水FeCl3在空气中易与水发生作用,加热易升华。

回答下列问题:
(1)仪器a的名称是
(2)试剂X是
(3)装置F中无水CaCl2的作用是
(4)某温度下,将氯气通入G装置中,反应得到NaCl,NaClO和NaClO3的混合溶液,经测定ClO-与ClO
 的物质的量之比为4∶1,写出该反应总的离子方程式:
的物质的量之比为4∶1,写出该反应总的离子方程式:
您最近半年使用:0次
5 . 利用下列装置制备无水氯化铁。
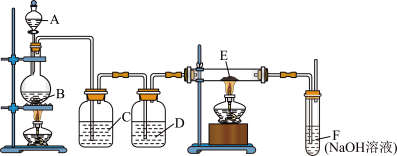
(1)仪器A的名称_______ 。
(2)烧瓶B中利用MnO2与浓盐酸制备氯气的离子方程式为:_______ 。
(3)将8.7gMnO2与含HCl14.6g的浓盐酸共热制Cl2,甲同学认为可制得Cl27.1g,乙同学认为制得Cl2的质量小于7.1g,你认为_______ (填“甲”或“乙”)同学正确,原因是_______ 。
(4)装置C盛有饱和食盐水的作用为_______ 。
(5)装置F的作用是_______ 。写出F中发生反应的化学方程式为:_______ 。
(6)制备无水氯化铁,该实验装置是否存在缺陷_______ (填“是”或“否”),若存在缺陷应怎样改进:_______ 。

(1)仪器A的名称
(2)烧瓶B中利用MnO2与浓盐酸制备氯气的离子方程式为:
(3)将8.7gMnO2与含HCl14.6g的浓盐酸共热制Cl2,甲同学认为可制得Cl27.1g,乙同学认为制得Cl2的质量小于7.1g,你认为
(4)装置C盛有饱和食盐水的作用为
(5)装置F的作用是
(6)制备无水氯化铁,该实验装置是否存在缺陷
您最近半年使用:0次
6 . 如图所示,从A处通入新制备的 ,关闭B阀时,C处的红色布条看不到明显现象;当打开B阀后,C处红色布条逐渐褪色。D瓶中装的是
,关闭B阀时,C处的红色布条看不到明显现象;当打开B阀后,C处红色布条逐渐褪色。D瓶中装的是 ④饱和NaCl溶液
④饱和NaCl溶液
 ,关闭B阀时,C处的红色布条看不到明显现象;当打开B阀后,C处红色布条逐渐褪色。D瓶中装的是
,关闭B阀时,C处的红色布条看不到明显现象;当打开B阀后,C处红色布条逐渐褪色。D瓶中装的是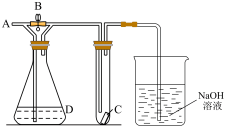
 ④饱和NaCl溶液
④饱和NaCl溶液| A.①③ | B.②④ | C.①② | D.③④ |
您最近半年使用:0次
名校
解题方法
7 . 下列反应的离子方程式正确的是
A.石灰乳与 溶液混合: 溶液混合: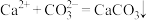 |
B.向 中加入少量 中加入少量 溶液: 溶液: |
C.氯气通入冷的氢氧化钠溶液中: |
D.钠与水的反应: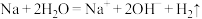 |
您最近半年使用:0次
8 . 下列处理方法错误的是
| A.钢铁厂生产中,炽热的铁水注入模具之前,模具必须进行充分干燥 |
| B.可利用高温下铝粉与氧化铁的反应焊接钢轨 |
| C.金属钠起火时,用泡沫灭火器灭火 |
D.贮氯罐意外泄漏,要组织人员向高处疏散,并喷洒稀 溶液 溶液 |
您最近半年使用:0次
名校
9 . “84”消毒液是生活中常见的含氯消毒剂,呈无色或淡黄色,可由Cl2与NaOH溶液反应制得。回答下列问题:
I.
(1)Cl2与NaOH溶液反应制取“84”消毒液的离子方程式 为___________ 。
(2)“84”消毒液的稀溶液在浸泡餐具过程中,因吸收空气中CO2使消毒杀菌能力增强,产物中有小苏打,请用化学方程式说明原因:___________ 。
II.实验室需使用480mL1.0mol/L的NaOH溶液来制备“84”消毒液。因此首先配制该NaOH溶液。
(3)实验必须用到的仪器有托盘天平、药匙、玻璃棒、烧杯、___________ 和___________ ,需要称量的NaOH固体的质量为___________ g。
(4)在配制氢氧化钠溶液时,有如下操作,正确的操作顺序是___________ (用字母符号 表示)。
A.盖好瓶塞,反复上下颠倒、摇匀
B.改用胶头滴管滴加蒸馏水,使溶液的凹液面恰好与容量瓶瓶颈上的刻度线相切
C.将已恢复至室温的溶液沿玻璃棒注入容量瓶中
D.用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,将洗涤液全部注入容量瓶中,轻轻摇动容量瓶
E.将NaOH固体置于烧杯中准确称量,向烧杯中加入适量蒸馏水,慢慢搅拌,使其全部溶解
F.继续往容量瓶中加蒸馏水,直到液面接近瓶颈上的刻度线1~2cm处
(5)在配制上述溶液的实验中,下列操作会造成结果偏低的有___________ (填标号 )。
a.容量瓶洗净后未干燥就进行实验
b.NaOH溶解后未冷却至室温就立即进行后面的配制操作
c.定容时,仰视容量瓶刻度线
d.没有用蒸馏水洗涤烧杯2~3次
(6)将4gNaOH溶于___________ g水中,可使溶液中H2O与Na+的物质的量之比等于20:1.若测得该溶液的密度为1.1g/cm3,溶液中c(Na+)为___________ mol/L。
I.
(1)Cl2与NaOH溶液反应制取“84”消毒液的
(2)“84”消毒液的稀溶液在浸泡餐具过程中,因吸收空气中CO2使消毒杀菌能力增强,产物中有小苏打,请用化学方程式说明原因:
II.实验室需使用480mL1.0mol/L的NaOH溶液来制备“84”消毒液。因此首先配制该NaOH溶液。
(3)实验必须用到的仪器有托盘天平、药匙、玻璃棒、烧杯、
(4)在配制氢氧化钠溶液时,有如下操作,正确的操作顺序是
A.盖好瓶塞,反复上下颠倒、摇匀
B.改用胶头滴管滴加蒸馏水,使溶液的凹液面恰好与容量瓶瓶颈上的刻度线相切
C.将已恢复至室温的溶液沿玻璃棒注入容量瓶中
D.用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,将洗涤液全部注入容量瓶中,轻轻摇动容量瓶
E.将NaOH固体置于烧杯中准确称量,向烧杯中加入适量蒸馏水,慢慢搅拌,使其全部溶解
F.继续往容量瓶中加蒸馏水,直到液面接近瓶颈上的刻度线1~2cm处
(5)在配制上述溶液的实验中,下列操作会造成结果偏低的有
a.容量瓶洗净后未干燥就进行实验
b.NaOH溶解后未冷却至室温就立即进行后面的配制操作
c.定容时,仰视容量瓶刻度线
d.没有用蒸馏水洗涤烧杯2~3次
(6)将4gNaOH溶于
您最近半年使用:0次
10 . 采用如图装置制取一定量的氯气,并进行氯水的性质实验。
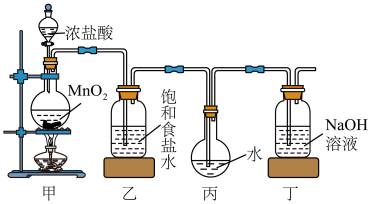
(1)如图装置中,盛装浓盐酸的仪器名称是__________ ,在装入药品前应进行的操作___________ 。
(2)写出甲装置中发生反应的化学反应方程式为___________ 。
(3)写出丁装置中发生反应的离子反应方程式为__________ 。
(4)用制得的氯水滴到蓝色石蕊试纸上的现象为__________ 。
(5)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,写出此反应的化学方程式:__________ 。

(1)如图装置中,盛装浓盐酸的仪器名称是
(2)写出甲装置中发生反应的化学反应方程式为
(3)写出丁装置中发生反应的离子反应方程式为
(4)用制得的氯水滴到蓝色石蕊试纸上的现象为
(5)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,写出此反应的化学方程式:
您最近半年使用:0次



