1 . 按下图制取氯气,并检验氯气是否具有漂白性。下列说法正确的是
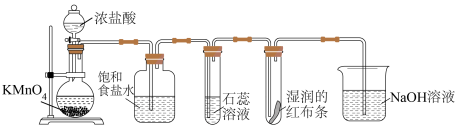
| A.在烧瓶内的反应中,盐酸只表现出还原性 | B.紫色的石蕊溶液先变红,后褪色 |
C.湿润的红布条褪色证明 具有漂白性 具有漂白性 | D.将 溶液改为澄清石灰水,可制备漂白粉 溶液改为澄清石灰水,可制备漂白粉 |
您最近半年使用:0次
2 . Cl2、SO2、CO2均是中学化学常见的气体,减少Cl2、SO2的排放可以防止污染空气,减少CO2的排放,有利于保护环境,实现碳中和。回答下列问题:
(1)化工厂可用浓氨水来检验Cl2是否泄漏,当有少量Cl2泄漏时,可以观察到的现象是________ 。
(2)用热烧碱溶液吸收Cl2反应后的混合溶液,若含NaCl、NaClO和NaClO3物质的量比值为n∶1∶2,则n=________ 。
(3)常温下,可用NaOH溶液作CO2的捕捉剂。若经测定某次捕捉所得溶液中,Na和C两种元素物质的量比值为3:1,则所得溶液中溶质成分为________ (填化学式)。
(4)①除品红外,鉴别SO2、CO2两种气体还可以采用________ (填试剂名称),SO2、Cl2均有漂白性,若将两者1∶1通入品红溶液中,不能使品红褪色,理由是________ (写离子方程式),除去SO2中的HCl可采用________ (填试剂名称)。
②用硫酸酸化的K2Cr2O7溶液处理SO2气体,会析出铬钾矾[KCr(SO4)2·12H2O]晶体。写出该反应的化学方程式:________ 。
(1)化工厂可用浓氨水来检验Cl2是否泄漏,当有少量Cl2泄漏时,可以观察到的现象是
(2)用热烧碱溶液吸收Cl2反应后的混合溶液,若含NaCl、NaClO和NaClO3物质的量比值为n∶1∶2,则n=
(3)常温下,可用NaOH溶液作CO2的捕捉剂。若经测定某次捕捉所得溶液中,Na和C两种元素物质的量比值为3:1,则所得溶液中溶质成分为
(4)①除品红外,鉴别SO2、CO2两种气体还可以采用
②用硫酸酸化的K2Cr2O7溶液处理SO2气体,会析出铬钾矾[KCr(SO4)2·12H2O]晶体。写出该反应的化学方程式:
您最近半年使用:0次
3 . 在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气,进行此实验,所用仪器如图:
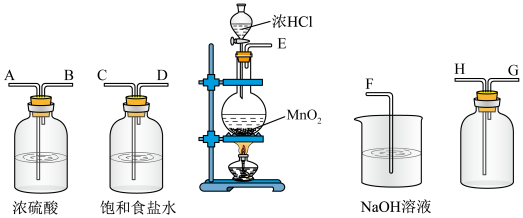
(1)连接上述仪器的正确顺序是___________ 。
 接 ___________,___________接 ___________,___________接___________,___________接
接 ___________,___________接 ___________,___________接___________,___________接 。
。
(2)气体发生装置中进行的反应化学方程式是___________ ;当
 参与反应时,被氧化的
参与反应时,被氧化的 的质量为
的质量为 ___________ ,生成的 在标准状况下的体积约为
在标准状况下的体积约为___________ 。
(3)写出尾气吸收装置中进行的反应的化学方程式___________ 。

(1)连接上述仪器的正确顺序是
 接 ___________,___________接 ___________,___________接___________,___________接
接 ___________,___________接 ___________,___________接___________,___________接 。
。(2)气体发生装置中进行的反应化学方程式是

 参与反应时,被氧化的
参与反应时,被氧化的 的质量为
的质量为  在标准状况下的体积约为
在标准状况下的体积约为(3)写出尾气吸收装置中进行的反应的化学方程式
您最近半年使用:0次
名校
解题方法
4 . 某小组用下列装置制备 并探究其部分性质,下列说法错误的是
并探究其部分性质,下列说法错误的是
 并探究其部分性质,下列说法错误的是
并探究其部分性质,下列说法错误的是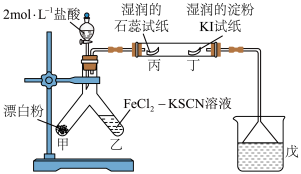
A.漂白粉的主要成分为 和 和 |
B.一段时间后,乙处溶液会变红,丁处湿润的淀粉 试纸会变蓝 试纸会变蓝 |
| C.实验过程中,能观察到丙处湿润的石蕊试纸先变蓝后褪色的现象 |
D.戊处的溶液为 浓溶液,用于吸收尾气中的 浓溶液,用于吸收尾气中的 |
您最近半年使用:0次
2024-03-28更新
|
89次组卷
|
2卷引用:河北省保定市定州市第二中学2023-2024学年高一下学期3月月考化学试题
名校
5 . 氯碱工业涉及Cl2、H2、NaOH、NaClO等物质。设NA为阿伏加德罗常数的值,下列说法错误的是
| A.1 mol NaOH固体中的离子数目为2NA |
| B.1 L1mol/L的NaClO溶液中,ClO-的数目小于NA |
| C.标况下,22.4L的H2和Cl2混合气体,共价键数目为NA |
| D.1 mol Cl2与足量NaOH溶液反应生成NaClO转移电子数为2NA |
您最近半年使用:0次
2024-03-22更新
|
390次组卷
|
2卷引用:河北省石家庄市第二中学2023-2024学年高三上学期期末考试化学试题
解题方法
6 . 如图所示的氯元素的价类二维图。下列叙述不正确的是
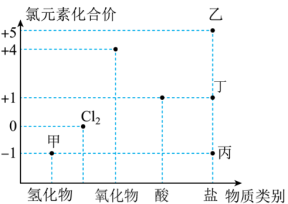

| A.胃酸的主要成分是甲的水溶液 |
B.将 通入一定温度下的 通入一定温度下的 溶液中,生成乙和丙,则 溶液中,生成乙和丙,则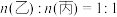 |
| C.“84”消毒液(丁的钠盐)不能与“洁厕灵”(甲的水溶液)混合使用 |
D.如果物质丙和丁是漂白粉的主要成分,其中有效成分是 |
您最近半年使用:0次
7 .  为阿伏加德罗常数的值,下列有关说法正确的是
为阿伏加德罗常数的值,下列有关说法正确的是
 为阿伏加德罗常数的值,下列有关说法正确的是
为阿伏加德罗常数的值,下列有关说法正确的是A. 的 的 溶液中 溶液中 的数目为 的数目为 |
B. 中含有的中子数为 中含有的中子数为 |
C.标准状况下,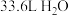 中含有的分子数为 中含有的分子数为 |
D.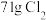 溶于过量氢氧化钠溶液中,所得溶液中 溶于过量氢氧化钠溶液中,所得溶液中 和 和 微粒总数为 微粒总数为 |
您最近半年使用:0次
解题方法
8 . 实验室可以用氯气制备多种物质,某化学小组在实验室制备 、NaClO和
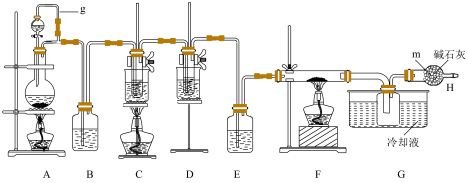
、NaClO和 三种物质。实验装置如下图所示,其中C的试管里盛有15mL 30% KOH溶液,并置于热水浴中;D的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;F中硬质玻璃管中为还原铁粉,FeCl3能吸收空气里的水分而潮解。回答下列问题:
三种物质。实验装置如下图所示,其中C的试管里盛有15mL 30% KOH溶液,并置于热水浴中;D的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;F中硬质玻璃管中为还原铁粉,FeCl3能吸收空气里的水分而潮解。回答下列问题:
(1)装置A中用 和浓盐酸反应制备
和浓盐酸反应制备 的离子方程式为
的离子方程式为_______ 。
(2)装置A中g管的作用是_______ ;装置B中的试剂是_______ ;装置E中的试剂是_______ 。
(3)比较制取 和NaClO的反应条件,二者的差异是:
和NaClO的反应条件,二者的差异是:_______ 。
(4)写出制备NaClO反应的离子方程式_______ 。
(5)写出制备 的化学反应方程式
的化学反应方程式_______ 。
(6)若没有控制好反应温度,C中产物中可能有 、KClO和KCl三种盐生成,反应后
、KClO和KCl三种盐生成,反应后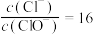 ,则溶液
,则溶液
_______ (填分数比)。
(7)碱石灰的成分是NaOH和CaO的混合物,盛放碱石灰的仪器m的名称是_______ ,其作用是(答出两条)_______ 。
 、NaClO和
、NaClO和 三种物质。实验装置如下图所示,其中C的试管里盛有15mL 30% KOH溶液,并置于热水浴中;D的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;F中硬质玻璃管中为还原铁粉,FeCl3能吸收空气里的水分而潮解。回答下列问题:
三种物质。实验装置如下图所示,其中C的试管里盛有15mL 30% KOH溶液,并置于热水浴中;D的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;F中硬质玻璃管中为还原铁粉,FeCl3能吸收空气里的水分而潮解。回答下列问题:
(1)装置A中用
 和浓盐酸反应制备
和浓盐酸反应制备 的离子方程式为
的离子方程式为(2)装置A中g管的作用是
(3)比较制取
 和NaClO的反应条件,二者的差异是:
和NaClO的反应条件,二者的差异是:(4)写出制备NaClO反应的离子方程式
(5)写出制备
 的化学反应方程式
的化学反应方程式(6)若没有控制好反应温度,C中产物中可能有
 、KClO和KCl三种盐生成,反应后
、KClO和KCl三种盐生成,反应后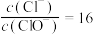 ,则溶液
,则溶液
(7)碱石灰的成分是NaOH和CaO的混合物,盛放碱石灰的仪器m的名称是
您最近半年使用:0次
名校
9 . 某课外活动小组欲验证干燥氯气有无漂白性以及卤素单质氧化性的强弱,根据已有的仪器设计相关实验。请回答下列问题:
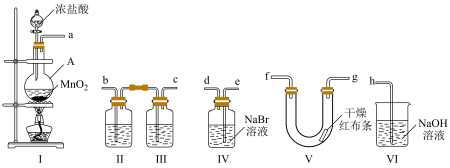
(1)各仪器装置连接的顺序为_______ (填接口字母)
a接___________、___________接___________、___________接___________、___________接h
(2)装置I中仪器A的名称是___________ ,装置I中发生反应的化学方程式为___________ 。
(3)为了除去混有的少量HCl气体,装置Ⅱ应加入的试剂是___________ ,装置Ⅲ的作用是___________ 。
(4)反应结束一段时间后,向装置Ⅳ中加入四氯化碳,震荡静置,四氯化碳在___________ 层(填“上”或“下”),呈现___________ 色验证了卤素单质氧化性的强弱。装置V中现象为___________ 验证了干燥氯气无漂白性。
(5)装置Ⅵ中发生反应的离子方程式为___________ 。

(1)各仪器装置连接的顺序为
a接___________、___________接___________、___________接___________、___________接h
(2)装置I中仪器A的名称是
(3)为了除去混有的少量HCl气体,装置Ⅱ应加入的试剂是
(4)反应结束一段时间后,向装置Ⅳ中加入四氯化碳,震荡静置,四氯化碳在
(5)装置Ⅵ中发生反应的离子方程式为
您最近半年使用:0次
2024-02-26更新
|
68次组卷
|
2卷引用:河北省唐山市2023-2024学年高一上学期1月期末考试化学试题
解题方法
10 . 化学与生产、生活息息相关。下列说法正确的是
| A.在去除锅炉水垢时,通常先用碳酸钠溶液浸泡,再用酸去除 |
B.硫酸工业中, 的催化氧化不采用高压,是因为压强对 的催化氧化不采用高压,是因为压强对 转化率无影响 转化率无影响 |
| C.明矾水解时产生具有吸附性的胶体粒子,可作漂白剂 |
| D.用氯气和氢氧化钠制取消毒液,运用了盐类水解的原理 |
您最近半年使用:0次



