解题方法
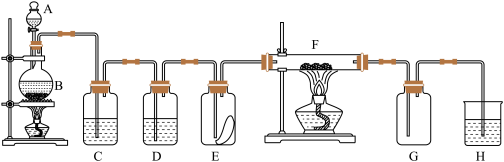
1 . 如图为实验室制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条,F中为红色的铜网,其右端出气管口放有脱脂棉。___________ 。
(2)装置C中盛装的溶液是___________ ,D中试剂的作用是___________ 。
(3)E中红色布条是否褪色?___________ (填“是”或“否”),F中的反应产物为___________ 。
(4)新制氯水呈酸性,分别写出盐酸和次氯酸的电离方程式___________ ,___________ 。
(5)若H中选用NaOH溶液进行尾气处理,则发生的反应是(用离子方程式表示)___________ 。
(2)装置C中盛装的溶液是
(3)E中红色布条是否褪色?
(4)新制氯水呈酸性,分别写出盐酸和次氯酸的电离方程式
(5)若H中选用NaOH溶液进行尾气处理,则发生的反应是(用离子方程式表示)
您最近半年使用:0次
名校
解题方法
2 .  、HCl的混合气体通入足量的NaOH溶液,充分反应后,溶液中除大量
、HCl的混合气体通入足量的NaOH溶液,充分反应后,溶液中除大量 外,还有
外,还有 、
、 、
、 ,且这三种离子的个数比为9∶2∶1,则原混合气体中
,且这三种离子的个数比为9∶2∶1,则原混合气体中 和HCl的个数之比为
和HCl的个数之比为
 、HCl的混合气体通入足量的NaOH溶液,充分反应后,溶液中除大量
、HCl的混合气体通入足量的NaOH溶液,充分反应后,溶液中除大量 外,还有
外,还有 、
、 、
、 ,且这三种离子的个数比为9∶2∶1,则原混合气体中
,且这三种离子的个数比为9∶2∶1,则原混合气体中 和HCl的个数之比为
和HCl的个数之比为| A.5∶2 | B.2∶5 | C.3∶1 | D.1∶3 |
您最近半年使用:0次
名校
3 . 次氯酸钠消毒液广泛应用于不同场景,可以用在酒店、学校及其他公共场所消毒。如图为实验室制备次氯酸钠的装置。

回答下列问题:
(1)装置A中发生反应的化学方程式为___________ 。
(2)装置B中饱和食盐水的作用是___________ 。
(3)实验室还可以用 制取氯气,反应的化学方程式为
制取氯气,反应的化学方程式为 。
。
①用双线桥标出该反应电子转移的方向和数目:___________ 。
②标准状况下若产生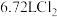 ,则反应过程中被氧化的HCl的物质的量是
,则反应过程中被氧化的HCl的物质的量是___________ ,转移电子的物质的量为___________ 。
(4)三颈烧瓶中生成各物质的物质的量随时间的变化如图所示(已知 与NaOH溶液的反应为放热反应)。
与NaOH溶液的反应为放热反应)。
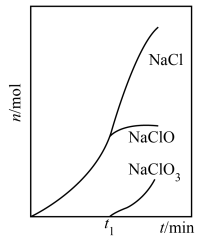
① 前所发生主要反应的化学方程式为
前所发生主要反应的化学方程式为___________ 。
②装置C中进行___________ (填“冰水浴”或“热水浴”)可提高次氯酸钠的产率,如果缺少该装置,可能造成的影响是___________ (用化学方程式表示)。

回答下列问题:
(1)装置A中发生反应的化学方程式为
(2)装置B中饱和食盐水的作用是
(3)实验室还可以用
 制取氯气,反应的化学方程式为
制取氯气,反应的化学方程式为 。
。①用双线桥标出该反应电子转移的方向和数目:
②标准状况下若产生
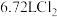 ,则反应过程中被氧化的HCl的物质的量是
,则反应过程中被氧化的HCl的物质的量是(4)三颈烧瓶中生成各物质的物质的量随时间的变化如图所示(已知
 与NaOH溶液的反应为放热反应)。
与NaOH溶液的反应为放热反应)。
①
 前所发生主要反应的化学方程式为
前所发生主要反应的化学方程式为②装置C中进行
您最近半年使用:0次
名校
解题方法
4 . 氯气是一种重要的化工原料,可用于制备盐酸、漂白剂和杀菌消毒剂等。
(1)1774年的舍勒用软锰矿粉末(主要成分是 )和浓盐酸混合加热制备氯气,若
)和浓盐酸混合加热制备氯气,若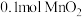 和
和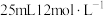 盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量
盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量 溶液,生成
溶液,生成 沉淀物质的量为_____(不考虑盐酸的挥发)
沉淀物质的量为_____(不考虑盐酸的挥发)
(2)氯化铁是一种常见的水处理剂,需要密封保存。无水氯化铁遇潮湿空气极易吸水生成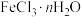 。在实验室中,可以采用下列仪器和药品制取较纯的无水氯化铁固体。
。在实验室中,可以采用下列仪器和药品制取较纯的无水氯化铁固体。

①C装置中的试剂为_____ (填试剂名称),其作用是_____ 。
②D装置的作用是_____ 。用一件仪器装填适当试剂后,也可起到C和D的作用,所装填的试剂为_____ (填干燥剂名称)。
③若D中吸收了标准状况下 L氯气,则需要消耗NaOH的质量为
L氯气,则需要消耗NaOH的质量为_____ 克。
(1)1774年的舍勒用软锰矿粉末(主要成分是
 )和浓盐酸混合加热制备氯气,若
)和浓盐酸混合加热制备氯气,若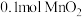 和
和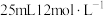 盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量
盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量 溶液,生成
溶液,生成 沉淀物质的量为_____(不考虑盐酸的挥发)
沉淀物质的量为_____(不考虑盐酸的挥发)A.等于 | B.小于 |
C.大于 ,小于 ,小于 | D.以上结论都不正确 |
(2)氯化铁是一种常见的水处理剂,需要密封保存。无水氯化铁遇潮湿空气极易吸水生成
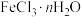 。在实验室中,可以采用下列仪器和药品制取较纯的无水氯化铁固体。
。在实验室中,可以采用下列仪器和药品制取较纯的无水氯化铁固体。
①C装置中的试剂为
②D装置的作用是
③若D中吸收了标准状况下
 L氯气,则需要消耗NaOH的质量为
L氯气,则需要消耗NaOH的质量为
您最近半年使用:0次
2023-11-23更新
|
89次组卷
|
2卷引用:河北省石家庄市第十八中学2023-2024学年高一上学期期中考试化学试题
解题方法
5 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备 和NaClO,已知:氯气和碱反应在室温下生成氯化物和次氯酸盐,温度升高时主要产物是氯化物和氯酸盐,氯气和碱的反应释放热量。
和NaClO,已知:氯气和碱反应在室温下生成氯化物和次氯酸盐,温度升高时主要产物是氯化物和氯酸盐,氯气和碱的反应释放热量。

回答下列问题:
(1)a中制取氯气的化学方程式为_______ 。
(2)d中化学反应的离子方程式是_______ ,采用冰水浴冷却的目的是_______ 。
(3)e的作用是_______ 。
(4)反应结束后,取出c中试管,经冷却结晶、_______ 、_______ 、干燥,得到 晶体。(填写操作名称)
晶体。(填写操作名称)
(5)反应结束后,d试管中溶液具有消毒、漂白作用,向d中通入或加入下列物质,能使其消毒、漂白效果明显增强的有_______。
 和NaClO,已知:氯气和碱反应在室温下生成氯化物和次氯酸盐,温度升高时主要产物是氯化物和氯酸盐,氯气和碱的反应释放热量。
和NaClO,已知:氯气和碱反应在室温下生成氯化物和次氯酸盐,温度升高时主要产物是氯化物和氯酸盐,氯气和碱的反应释放热量。
回答下列问题:
(1)a中制取氯气的化学方程式为
(2)d中化学反应的离子方程式是
(3)e的作用是
(4)反应结束后,取出c中试管,经冷却结晶、
 晶体。(填写操作名称)
晶体。(填写操作名称)(5)反应结束后,d试管中溶液具有消毒、漂白作用,向d中通入或加入下列物质,能使其消毒、漂白效果明显增强的有_______。
A. | B.饱和食盐水 | C. | D.NaOH溶液 |
您最近半年使用:0次
2023-11-15更新
|
95次组卷
|
2卷引用:河北省高碑店市崇德实验中学2023-2024学年高一上学期期中考试化学试题
名校
6 . NaCl是一种化工原料,可以制备多种物质,如图所示。
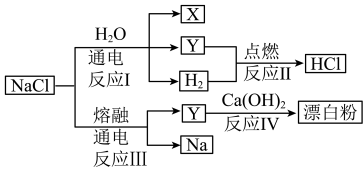
下列说法错误的是

下列说法错误的是
A.反应I的化学方程式为NaCl+2H2O NaOH+H2↑+Cl2↑ NaOH+H2↑+Cl2↑ |
| B.反应I、II、III、IV均为氧化还原反应 |
| C.X的溶液可用于吸收含Y的尾气 |
| D.漂白粉的有效成分为Ca(ClO)2 |
您最近半年使用:0次
2023-11-10更新
|
190次组卷
|
3卷引用:河北省定州市2023-2024学年高二上学期11月期中考试化学试题
7 . 某化学兴趣小组同学利用如图所示装置制取氯气。
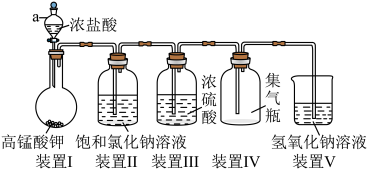
回答下列问题:
(1)连接好装置,再________ ,然后添加药品。
(2)装置I中发生反应的离子方程式为________ ,a的仪器名称为_______ 。
(3)装置III中浓硫酸的作用为_______ 。
(4)密度:Cl2_________ (填“>”、“<”或“=”)空气,判断的理由为________ 。
(5)装置V中发生反应的化学方程式为_________ (不考虑空气对反应的影响),该反应中,每消耗7.1gCl2,消耗NaOH的质量为________ g。

回答下列问题:
(1)连接好装置,再
(2)装置I中发生反应的离子方程式为
(3)装置III中浓硫酸的作用为
(4)密度:Cl2
(5)装置V中发生反应的化学方程式为
您最近半年使用:0次
解题方法
8 . 将氯气缓慢通过内有湿润的红纸条的广口瓶(如图所示),下列说法错误的是
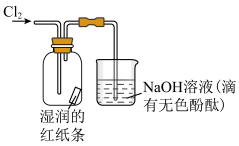

| A.烧杯中的溶液可换成饱和氯化钠溶液进行尾气处理 |
| B.一段时间后,可观察到湿润的红纸条褪色 |
| C.氯气是一种黄绿色的有毒气体 |
| D.烧杯中可能发生反应的化学方程式为3Cl2+6NaOH=5NaCl+NaClO3+3H2O |
您最近半年使用:0次
名校
解题方法
9 . 将一定量的氯气通入0.50 mol的氢氧化钠浓溶液中,加热少许时间后,溶液中形成NaCl、NaClO、 共存体系(不考虑氯气和水的反应)。下列说法正确的是
共存体系(不考虑氯气和水的反应)。下列说法正确的是
 共存体系(不考虑氯气和水的反应)。下列说法正确的是
共存体系(不考虑氯气和水的反应)。下列说法正确的是| A.若反应中转移的电子为n mol,则0.25<n<0.5 |
B.溶液中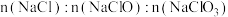 可能为4∶3∶1 可能为4∶3∶1 |
| C.与NaOH反应的氯气为0.5 mol |
D.当溶液中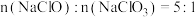 时,反应中氧化剂与还原剂的物质的量之比为5∶3 时,反应中氧化剂与还原剂的物质的量之比为5∶3 |
您最近半年使用:0次
2023-10-11更新
|
815次组卷
|
5卷引用:河北省秦皇岛市第一中学2023-2024学年高一上学期期中考试化学试题
名校
10 . 用NA表示阿伏伽德罗常数,下列说法中正确的有
A.若Cl2与足量NaOH的溶液反应生成 0.1 mol,则生成的 0.1 mol,则生成的 数目为0.2NA 数目为0.2NA |
| B.常温常压下,17 g NH3的体积约为22.4L |
| C.1 mol/L的CaCl2溶液中含Cl-的数目为2NA |
| D.在50g质量分数为46%的乙醇水溶液中,含氢原子总数为6NA |
您最近半年使用:0次
2023-10-09更新
|
75次组卷
|
2卷引用:河北省石家庄市第十八中学2023-2024学年高一上学期期中考试化学试题



