解题方法
1 . 将Cl2通入70℃的氢氧化钠水溶液中,发生以下反应(未配平):
 ,反应完成后测得溶液中NaClO与NaClO3的物质的量浓度之比为5:2,则该溶液中NaClO与NaCl的物质的量之比为
,反应完成后测得溶液中NaClO与NaClO3的物质的量浓度之比为5:2,则该溶液中NaClO与NaCl的物质的量之比为
 ,反应完成后测得溶液中NaClO与NaClO3的物质的量浓度之比为5:2,则该溶液中NaClO与NaCl的物质的量之比为
,反应完成后测得溶液中NaClO与NaClO3的物质的量浓度之比为5:2,则该溶液中NaClO与NaCl的物质的量之比为| A.5:2 | B.2:5 | C.5:16 | D.1:3 |
您最近半年使用:0次
解题方法
2 . 向盛有氯气的集气瓶中,注入约五分之一容器体积的下列液体并轻轻振荡,观察到的现象记录如图所示。判断瓶中注入的液体是
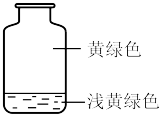

| A.AgNO3溶液 | B.NaOH溶液 | C.水 | D.FeCl2溶液 |
您最近半年使用:0次
解题方法
3 . 某化学兴趣小组用浓盐酸与MnO2制备并收集纯净的氯气,回答下列问题。
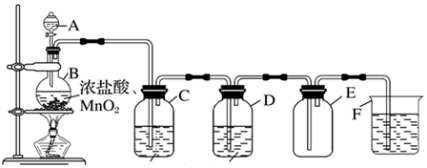
(1)仪器A名称_______ ,利用该装置制氯气的化学方程式为_______ 。
(2)C中溶液的试剂是_______ ,D的作用是______ 。
(3)装置F的作用______ ,涉及的主要离子反应方程式_______ 。

(1)仪器A名称
(2)C中溶液的试剂是
(3)装置F的作用
您最近半年使用:0次
4 . 按要求填空:
(1)将80克NaOH溶解于水中,配成5L溶液,则NaOH的物质的量浓度是
(2)在同温同压下,等质量铝投入足量盐酸和NaOH溶液中,产生气体的体积之比为
(3)某些化学反应可以表示为A+B→C+D+H2O,若A、C、D均含有氯元素,且A的化合价介于C与D之间,写出该反应的离子方程式:
(4)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为
(5)某+3价阳离子(M3+)含有24个电子,它的质量数为56,该离子核内中子数为
您最近半年使用:0次
解题方法
5 . ClO2作为一种广泛的消毒剂,它密度比空气大,易溶于水而难溶于有机溶剂,实验室用NaClO2与干燥的Cl2反应制得ClO2和NaCl。下图是实验室用于制备和收集一定量纯净的ClO2的装置(某些夹持装置和垫持用品省略)。其中E中盛有液体(用于除去 中的未反应的Cl2,氧气几乎不溶于饱和食盐水)。
中的未反应的Cl2,氧气几乎不溶于饱和食盐水)。
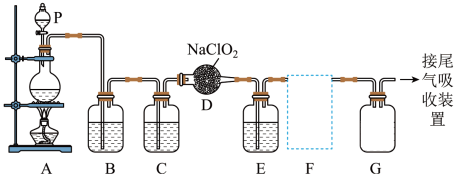
(1)仪器P的名称是___________ 。
(2)请写出装置A中烧瓶内发生反应的化学方程式:___________ ,每转移4NA个电子时,产生Cl2分子的物质的量为___________ 。
(3)B的作用___________ ,C装置中所盛试剂是___________ 。
(4)F为ClO2收集装置,应选用的装置是___________ (填序号),其中与装置E导管相连的导管口是___________ (填接口字母)。

(5)装置D中发生反应的化学方程式为___________ 。
(6)Cl2与NaOH反应可以得到以NaClO为有效成分的漂白液,漂白液与洁厕灵(主要成分为HCl)同时使用会产生Cl2,请用离子方程式表示该反应___________ 。
 中的未反应的Cl2,氧气几乎不溶于饱和食盐水)。
中的未反应的Cl2,氧气几乎不溶于饱和食盐水)。
(1)仪器P的名称是
(2)请写出装置A中烧瓶内发生反应的化学方程式:
(3)B的作用
(4)F为ClO2收集装置,应选用的装置是

(5)装置D中发生反应的化学方程式为
(6)Cl2与NaOH反应可以得到以NaClO为有效成分的漂白液,漂白液与洁厕灵(主要成分为HCl)同时使用会产生Cl2,请用离子方程式表示该反应
您最近半年使用:0次
名校
6 . 化学是一门以实验为基础的学科,下列实验方案操作正确且能够达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 除去 中的少量的 中的少量的 | 将混合气体通过盛有碱石灰的干燥管 |
| B | 制备 胶体 胶体 | 向饱和 溶液中逐滴加入 溶液中逐滴加入 溶液,继续煮沸后停止加热 溶液,继续煮沸后停止加热 |
| C | 制备 | 向铁粉中通入氯气并点燃 |
| D | 除去 中混有的少量 中混有的少量 | 将混合物加热分解至恒重 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-02-24更新
|
75次组卷
|
2卷引用:云南省昭通市第一中学教研联盟2023-2024学年高一上学期期末质量检测化学(B卷)试题
名校
解题方法
7 . 下列离子方程式书写正确的是
A.铁粉与硝酸银溶液反应: |
B.碳酸氢钠溶液与氢氧化钾反应: |
C. 与水反应: 与水反应: |
D.向 粉中加入 粉中加入 溶液: 溶液: |
您最近半年使用:0次
2024-02-24更新
|
53次组卷
|
2卷引用:云南省昭通市第一中学教研联盟2023-2024学年高一上学期期末质量检测化学(B卷)试题
名校
解题方法
8 . 下列化学反应的离子方程式正确的是
| A.用醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O |
B.氯气溶于水:Cl2+H2O 2H++Cl-+ClO- 2H++Cl-+ClO- |
| C.钠投入硫酸铜溶液:2Na+Cu2+=2Na++Cu |
| D.石灰乳制漂白粉:Ca(OH)2+Cl2=Ca2++ClO-+Cl-+H2O |
您最近半年使用:0次
名校
解题方法
9 . 下列反应的离子反应方程式正确的是
A.向NaHCO3溶液中加入少量Ca(OH)2溶液:HCO +OH-+Ca2+=CaCO3↓+H2O +OH-+Ca2+=CaCO3↓+H2O |
| B.氯气通入冷的氢氧化钠溶液中:2Cl2+2OH-=3Cl-+ClO-+H2O |
| C.用“示踪原子法”来判断反应历程:5H218O2+2KMnO4+3H2SO4=418O2↑+K2SO4+2MnSO218O2+8H2O |
| D.用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+=Cu2++2Fe2+ |
您最近半年使用:0次
10 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备KClO3和NaClO,探究其氧化还原性质。

已知:CCl4难溶于水且密度比水大,I2在CCl4中显紫色;氯气与碱反应时温度不同产物不同。
请回答下列问题:
(1)写出装置①制取氯气的化学方程式___________________________________ 。
(2)其中盐酸的性质是__________________ ,仪器A的名称是______________ ,其中氧化剂与还原剂物质的量之比为_______________ 。
(3)装置②中的试剂为______________________ 。
(4)装置③中反应的化学方程式为____________________________ ,反应结束后,取出③中试管,经冷却结晶,过滤,少量(冷)水洗涤,干燥,得到 晶体。
晶体。
(5)装置④中反应的离子方程式为____________________________________ 。
(6)⑤中可选用试剂 (填标号)。
(7)取少量 和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入
和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入 振荡,静置后
振荡,静置后 层显紫色,可知该条件下
层显紫色,可知该条件下 的氧化能力比NaClO
的氧化能力比NaClO___________ (填“强”或“弱”)。

已知:CCl4难溶于水且密度比水大,I2在CCl4中显紫色;氯气与碱反应时温度不同产物不同。
请回答下列问题:
(1)写出装置①制取氯气的化学方程式
(2)其中盐酸的性质是
(3)装置②中的试剂为
(4)装置③中反应的化学方程式为
 晶体。
晶体。(5)装置④中反应的离子方程式为
(6)⑤中可选用试剂 (填标号)。
| A.Na2S | B.NaCl | C.澄清石灰水 | D.H2SO4 |
 和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入
和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入 振荡,静置后
振荡,静置后 层显紫色,可知该条件下
层显紫色,可知该条件下 的氧化能力比NaClO
的氧化能力比NaClO
您最近半年使用:0次



