解题方法
1 . 已知实验室常用 粉末和浓盐酸制取
粉末和浓盐酸制取 ,请回答下列问题:
,请回答下列问题:
(1)反应的化学方程式为: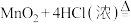
___________  。
。
(2)图1为 的发生装置,仪器
的发生装置,仪器 中盛放的试剂为
中盛放的试剂为___________ 。 的收集及尾气处理装置。
的收集及尾气处理装置。___________ (填“红棕色”或“黄绿色”)。
②该气体收集方法为___________ (填“向上”或“向下”)排空气法。
③烧杯中 溶液的作用是
溶液的作用是___________ 。
(4)将 中含有
中含有 气体通过
气体通过___________ 除去。
(5)若获得干燥的 ,用
,用___________ (填“浓硫酸”或“碱石灰”)做干燥剂。
 粉末和浓盐酸制取
粉末和浓盐酸制取 ,请回答下列问题:
,请回答下列问题:(1)反应的化学方程式为:
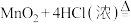
 。
。(2)图1为
 的发生装置,仪器
的发生装置,仪器 中盛放的试剂为
中盛放的试剂为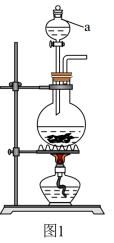
 的收集及尾气处理装置。
的收集及尾气处理装置。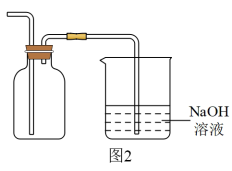
②该气体收集方法为
③烧杯中
 溶液的作用是
溶液的作用是(4)将
 中含有
中含有 气体通过
气体通过(5)若获得干燥的
 ,用
,用
您最近半年使用:0次
名校
解题方法
2 . 下列离子方程式与所给事实不相符的是
A. 制备84消毒液(主要成分是NaClO): 制备84消毒液(主要成分是NaClO): |
B.食醋去除水垢中的 : :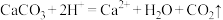 |
C.利用覆铜板制作印刷电路板: |
D.小苏打治疗胃酸过多: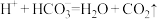 |
您最近半年使用:0次
名校
解题方法
3 . 用NA表示阿伏加德罗常数的值,下列叙述正确的是
A. 比 比 多2NA个质子 多2NA个质子 |
B.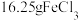 水解形成的 水解形成的 胶体粒子数为0.1NA 胶体粒子数为0.1NA |
C. 与足量的 与足量的 溶液反应转移的电子数为NA 溶液反应转移的电子数为NA |
D.pH=1的 溶液中含有0.1NA个H+ 溶液中含有0.1NA个H+ |
您最近半年使用:0次
名校
解题方法
4 . 已知氯气与强碱溶液反应时,产物受温度的影响。实验室中利用如图装置(部分装置省略)制备 和NaClO,并探究其氧化还原性质。
和NaClO,并探究其氧化还原性质。
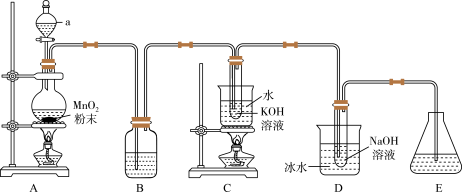
回答下列问题:
(1)仪器a的名称是___________ 。
(2)装置A制备氯气的离子方程式为___________ 。装置B中的试剂为___________ 。
(3)装置C中发生反应的化学方程式___________ 。
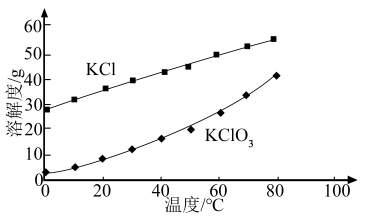
(4) 、KCl的溶解度曲线如下图所示,反应结束取出C中试管内制得的
、KCl的溶解度曲线如下图所示,反应结束取出C中试管内制得的 热饱和溶液,经
热饱和溶液,经___________ ,___________ ,洗涤,干燥,得到 晶体。
晶体。
(5)推测装置D使用冰水的原因___________ 。
(6)在40℃条件下,将一定量的 通入一定量的NaOH溶液中,NaOH恰好反应完全,得到的产物中含有NaCl、NaClO和
通入一定量的NaOH溶液中,NaOH恰好反应完全,得到的产物中含有NaCl、NaClO和 ,已知
,已知 和
和 的物质的量之比为11:1,则此过程中氧化剂和还原剂的物质的量之比为
的物质的量之比为11:1,则此过程中氧化剂和还原剂的物质的量之比为___________ 。
(7)探究 和NaClO的氧化能力
和NaClO的氧化能力
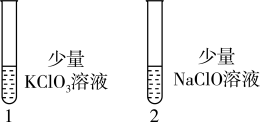
操作:向1号( )和2号(NaClO)试管中,滴加中性KI溶液。
)和2号(NaClO)试管中,滴加中性KI溶液。
现象:1号试管溶液颜色不变,2号试管溶液变为棕色。
结论:该条件下氧化能力
___________ NaClO。(填“大于”或“小于”)。
 和NaClO,并探究其氧化还原性质。
和NaClO,并探究其氧化还原性质。
回答下列问题:
(1)仪器a的名称是
(2)装置A制备氯气的离子方程式为
(3)装置C中发生反应的化学方程式
(4)
 、KCl的溶解度曲线如下图所示,反应结束取出C中试管内制得的
、KCl的溶解度曲线如下图所示,反应结束取出C中试管内制得的 热饱和溶液,经
热饱和溶液,经 晶体。
晶体。
(5)推测装置D使用冰水的原因
(6)在40℃条件下,将一定量的
 通入一定量的NaOH溶液中,NaOH恰好反应完全,得到的产物中含有NaCl、NaClO和
通入一定量的NaOH溶液中,NaOH恰好反应完全,得到的产物中含有NaCl、NaClO和 ,已知
,已知 和
和 的物质的量之比为11:1,则此过程中氧化剂和还原剂的物质的量之比为
的物质的量之比为11:1,则此过程中氧化剂和还原剂的物质的量之比为(7)探究
 和NaClO的氧化能力
和NaClO的氧化能力
操作:向1号(
 )和2号(NaClO)试管中,滴加中性KI溶液。
)和2号(NaClO)试管中,滴加中性KI溶液。现象:1号试管溶液颜色不变,2号试管溶液变为棕色。
结论:该条件下氧化能力

您最近半年使用:0次
5 . 下列图示实验(部分夹持装置省略)能达到目的的是
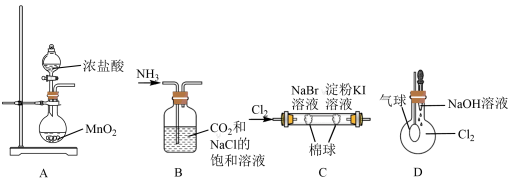

| A.图1:制取氯气 |
| B.图2:用于制备NaHCO3 |
| C.图3:证明非金属性: Cl2>Br2> I2 |
| D.图4:探究Cl2能否溶于水或与NaOH反应 |
您最近半年使用:0次
6 . 现有下列物质(括号内为对应物质的主要成分):a.熔融NaOH;b.医用酒精;c.蔗糖晶体;d.加碘盐(NaCl和KIO3);e.“84”消毒液(NaClO);f.小苏打(NaHCO3);g.洁厕灵(HCl),回答下列问题:
(1)上述状态下的物质中,属于电解质且能导电的是_______ (填字母,下同);d和f均为厨房中的常用物质,可用于区分两者的物质是________ 。
(2)生活中若将“84”消毒液和洁厕灵混合易产生黄绿色有毒气体,写出该反应的离子方程式:________ 。
(3)碘酸钾(KIO3)可作为食盐中的补碘剂。一种制备KIO3的方法是将I2与KOH溶液共热,生成KIO3、H2O和另—种化合物,写出该反应的化学方程式:___________ ;该反应中被氧化的Ⅰ原子与被还原的Ⅰ原子的个数之比为___________ 。
(4)二氧化氯泡腾片(有效成分为NaClO2和NaHSO4)也是一种用途广泛的消毒用品,将1片(规格为1g/片)二氧化氯泡腾片溶于1L水中,得到ClO2溶液(假设ClO2全部溶于水且反应后溶液体积仍为1L)。补全生成ClO2的化学方程式:_____ ,__NaClO2+__NaHSO4=___ClO2+___NaCl+__Na2SO4+____H2O;若每片泡腾片中NaClO2的质量分数≥17%为合格品,上述所得ClO2溶液的物质的量浓度为0.002mol/L,则所用泡腾片____ (填“属于”或“不属于”)合格品。
(1)上述状态下的物质中,属于电解质且能导电的是
(2)生活中若将“84”消毒液和洁厕灵混合易产生黄绿色有毒气体,写出该反应的离子方程式:
(3)碘酸钾(KIO3)可作为食盐中的补碘剂。一种制备KIO3的方法是将I2与KOH溶液共热,生成KIO3、H2O和另—种化合物,写出该反应的化学方程式:
(4)二氧化氯泡腾片(有效成分为NaClO2和NaHSO4)也是一种用途广泛的消毒用品,将1片(规格为1g/片)二氧化氯泡腾片溶于1L水中,得到ClO2溶液(假设ClO2全部溶于水且反应后溶液体积仍为1L)。补全生成ClO2的化学方程式:
您最近半年使用:0次
7 . 化学与生产、生活和科学技术的发展有着密切的联系。下列说法中错误的是
| A.二氧化氯(ClO2)、臭氧可替代氯气成为新的自来水消毒剂 |
| B.工业上用Na2O和H2O反应制取烧碱 |
| C.生铁和钢是含碳量不同的两种铁碳合金,一般生铁的含碳量高于钢 |
| D.“84”消毒液和“洁厕灵”不能混合使用 |
您最近半年使用:0次
名校
8 . 下表是元素周期表的一部分,针对表中的①~⑨9种元素,填写下列空白:
(1)写出元素符号和名称:
①_____ ,②_____ ,⑧_____ ,⑨_____ 。
(2)写出下列反应的化学方程式:
⑦的单质跟④的氢氧化物溶液反应_____ 。
⑤的氧化物跟④的氢氧化物溶液反应:_____ 。
④的单质在③的单质中燃烧:_____ 。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 四 | ⑨ |
①
(2)写出下列反应的化学方程式:
⑦的单质跟④的氢氧化物溶液反应
⑤的氧化物跟④的氢氧化物溶液反应:
④的单质在③的单质中燃烧:
您最近半年使用:0次
名校
解题方法
9 . 已知:将 通入适量
通入适量 溶液中,反应会放热,当温度升高后会发生如下反应:
溶液中,反应会放热,当温度升高后会发生如下反应: 。则
。则 通入
通入 溶液的产物中可能有
溶液的产物中可能有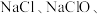
 中的两种或三种,且
中的两种或三种,且 的值与温度高低有关。当参与反应的
的值与温度高低有关。当参与反应的 时,下列说法错误的是
时,下列说法错误的是
 通入适量
通入适量 溶液中,反应会放热,当温度升高后会发生如下反应:
溶液中,反应会放热,当温度升高后会发生如下反应: 。则
。则 通入
通入 溶液的产物中可能有
溶液的产物中可能有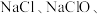
 中的两种或三种,且
中的两种或三种,且 的值与温度高低有关。当参与反应的
的值与温度高低有关。当参与反应的 时,下列说法错误的是
时,下列说法错误的是A.参加反应的 物质的量为 物质的量为 |
B.改变温度,反应中转移电子的物质的量可能为 |
C.某温度下,反应后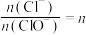 ,则溶液中 ,则溶液中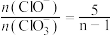 |
D.某温度下,反应后溶液中: |
您最近半年使用:0次
10 . 一氧化二氯( )是高效安全的杀菌消毒剂,某兴趣小组用下图所示装置制备并收集
)是高效安全的杀菌消毒剂,某兴趣小组用下图所示装置制备并收集 ,反应的原理如下:
,反应的原理如下: 。
。
已知: 的部分性质如表所示
的部分性质如表所示

请回答下列问题:
(1)装置A中仪器a的名称为___________ ,装置A中发生反应的化学方程式为___________ 。
(2)装置B中盛装的试剂的名称为___________ 。
(3)装置E采用冰水混合物冷却的目的是___________ 。
(4)装置F中无水 的作用是
的作用是___________ 。
(5)装置G中发生反应的离子方程式为___________ 。
(6)与传统消毒剂 比较,
比较, 消毒效率是
消毒效率是 的
的___________ 倍(产物视为 ,消毒效率以单位质量得到的电子数表示,结果精确到0.01)。
,消毒效率以单位质量得到的电子数表示,结果精确到0.01)。
 )是高效安全的杀菌消毒剂,某兴趣小组用下图所示装置制备并收集
)是高效安全的杀菌消毒剂,某兴趣小组用下图所示装置制备并收集 ,反应的原理如下:
,反应的原理如下: 。
。已知:
 的部分性质如表所示
的部分性质如表所示| 物理性质 | 化学性质 |
常温下, 是棕黄色、有刺激性气味的气体;熔点:-120.6℃;沸点2.0℃ 是棕黄色、有刺激性气味的气体;熔点:-120.6℃;沸点2.0℃ |  易溶于水,同时与水反应生成 易溶于水,同时与水反应生成 |

请回答下列问题:
(1)装置A中仪器a的名称为
(2)装置B中盛装的试剂的名称为
(3)装置E采用冰水混合物冷却的目的是
(4)装置F中无水
 的作用是
的作用是(5)装置G中发生反应的离子方程式为
(6)与传统消毒剂
 比较,
比较, 消毒效率是
消毒效率是 的
的 ,消毒效率以单位质量得到的电子数表示,结果精确到0.01)。
,消毒效率以单位质量得到的电子数表示,结果精确到0.01)。
您最近半年使用:0次



