1 . 下列离子方程式正确的是
A.过氧化钠和稀盐酸反应: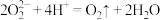 |
B.将 通入含 通入含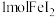 的溶液中: 的溶液中: |
C.向饱和碳酸钠溶液中通入足量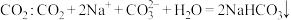 |
D.工业上制备漂白粉的离子方程式: |
您最近半年使用:0次
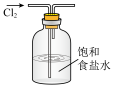
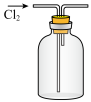
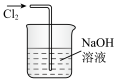
2 . 实验室制取氯气时,下列设计不能达到相应实验目的的是
|
|
|
|
| A.制取 | B.除氯化氢 | C.收集 | D.尾气吸收 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
3 . 用NA表示阿伏加德罗常数,下列说法错误的是
A.将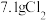 通入足量氢氧化钠溶液中,转移电子数为 通入足量氢氧化钠溶液中,转移电子数为 |
B.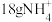 所含的电子数目为 所含的电子数目为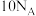 |
C.含0.2mol FeCl3的氯化铁饱和溶液滴入沸水充分反应形成的 胶体粒子数小于0.2NA 胶体粒子数小于0.2NA |
D. 在空气中完全燃烧生成MgO和Mg3N2的混合物,转移的电子数为 在空气中完全燃烧生成MgO和Mg3N2的混合物,转移的电子数为 |
您最近半年使用:0次
4 . 下列现象不能用“相似相溶”规律解释的是
| A.甲烷难溶于水 | B.氯气易溶于NaOH溶液 |
| C.溴易溶于CCl4 | D.酒精易溶于水 |
您最近半年使用:0次
解题方法
5 . 已知:将 通入适量的浓
通入适量的浓 溶液中,反应会放热,当温度升高后会发生如下反应:
溶液中,反应会放热,当温度升高后会发生如下反应: 。则
。则 通入浓
通入浓 溶液的产物中可能有
溶液的产物中可能有 、
、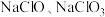 中的两种或三种,且
中的两种或三种,且 的值与温度高低有关。当参与反应的
的值与温度高低有关。当参与反应的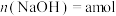 时,下列说法错误的是
时,下列说法错误的是
 通入适量的浓
通入适量的浓 溶液中,反应会放热,当温度升高后会发生如下反应:
溶液中,反应会放热,当温度升高后会发生如下反应: 。则
。则 通入浓
通入浓 溶液的产物中可能有
溶液的产物中可能有 、
、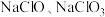 中的两种或三种,且
中的两种或三种,且 的值与温度高低有关。当参与反应的
的值与温度高低有关。当参与反应的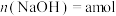 时,下列说法错误的是
时,下列说法错误的是A.与碱的反应中, 既是氧化剂又是还原剂 既是氧化剂又是还原剂 |
B.参加反应的 物质的量为 物质的量为 |
C.若某温度下,反应后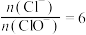 ,则溶液中 ,则溶液中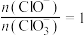 |
D.改变温度,反应中转移电子的物质的量可能为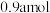 |
您最近半年使用:0次
6 . 下列离子方程式错误的是
A.向稀硫酸中滴加 溶液产生白色沉淀: 溶液产生白色沉淀: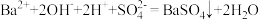 |
B.将 通入冷的石灰乳中制备漂白粉: 通入冷的石灰乳中制备漂白粉: |
C.用稀盐酸清洗水垢中的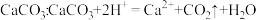 |
D.向 溶液中加入 溶液中加入 |
您最近半年使用:0次
7 . 实验室用浓盐酸和 制
制 ,并以干燥的
,并以干燥的 为原料制备无水
为原料制备无水 。已知
。已知 易升华,易吸收水分而潮解。装置如下图所示。
易升华,易吸收水分而潮解。装置如下图所示。_______ 。
(2)装置B、C中应盛放的试剂名称分别为_______ 、_______ 。
(3)从A装置导出的气体若不经过B、C装置而直接进入D管,将对实验产生的不良后果是_______ 。
(4)实验时,先点燃A处的酒精灯,让 充满装置,再点燃D处酒精灯,写出D中反应的化学方程式:
充满装置,再点燃D处酒精灯,写出D中反应的化学方程式:_______ 。
(5)F装置所起的作用是_______ 和防止空气中的水蒸气进入E中。
(6)生产消毒液是将氯气通入NaOH溶液中,发生反应的化学方程式为_______ 。
(7)取少量消毒液滴加酸性 溶液,现象是出现白色沉淀,说明消毒液中有
溶液,现象是出现白色沉淀,说明消毒液中有_______ (填离子符号),消毒液稀释后喷洒在空气中,可以生成有漂白性的物质,请写出此过程的化学方程式:_______ 。
 制
制 ,并以干燥的
,并以干燥的 为原料制备无水
为原料制备无水 。已知
。已知 易升华,易吸收水分而潮解。装置如下图所示。
易升华,易吸收水分而潮解。装置如下图所示。
(2)装置B、C中应盛放的试剂名称分别为
(3)从A装置导出的气体若不经过B、C装置而直接进入D管,将对实验产生的不良后果是
(4)实验时,先点燃A处的酒精灯,让
 充满装置,再点燃D处酒精灯,写出D中反应的化学方程式:
充满装置,再点燃D处酒精灯,写出D中反应的化学方程式:(5)F装置所起的作用是
(6)生产消毒液是将氯气通入NaOH溶液中,发生反应的化学方程式为
(7)取少量消毒液滴加酸性
 溶液,现象是出现白色沉淀,说明消毒液中有
溶液,现象是出现白色沉淀,说明消毒液中有
您最近半年使用:0次
解题方法
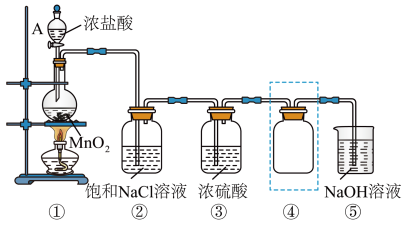
8 . 实验室制备并收集干燥氯气的实验装置如下所示,完成下列问题:______ 。
(2)装置①制备 的化学方程式是
的化学方程式是__________________ 。
(3)装置②中饱和NaCl溶液的作用是__________________ 。
(4)将图中气体收集装置④补充完整:__________________ 。
(5)装置⑤中反应的离子方程式是__________________ 。
(6)为推断 溶于水的产物并验证其光照分解的产物,利用数字传感器监测光照过程中某氯水的pH、氯水中氯离子的浓度、装置中氧气的体积分数这三者随时间的变化,实验结果如下图所示:
溶于水的产物并验证其光照分解的产物,利用数字传感器监测光照过程中某氯水的pH、氯水中氯离子的浓度、装置中氧气的体积分数这三者随时间的变化,实验结果如下图所示: 溶于水的化学反应方程式是
溶于水的化学反应方程式是__________________ 。
②表示氯水中氯离子浓度变化的图是______ (填图a或图b)。
(2)装置①制备
 的化学方程式是
的化学方程式是(3)装置②中饱和NaCl溶液的作用是
(4)将图中气体收集装置④补充完整:
(5)装置⑤中反应的离子方程式是
(6)为推断
 溶于水的产物并验证其光照分解的产物,利用数字传感器监测光照过程中某氯水的pH、氯水中氯离子的浓度、装置中氧气的体积分数这三者随时间的变化,实验结果如下图所示:
溶于水的产物并验证其光照分解的产物,利用数字传感器监测光照过程中某氯水的pH、氯水中氯离子的浓度、装置中氧气的体积分数这三者随时间的变化,实验结果如下图所示: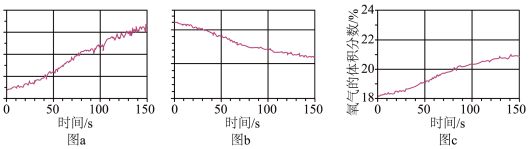
 溶于水的化学反应方程式是
溶于水的化学反应方程式是②表示氯水中氯离子浓度变化的图是
您最近半年使用:0次
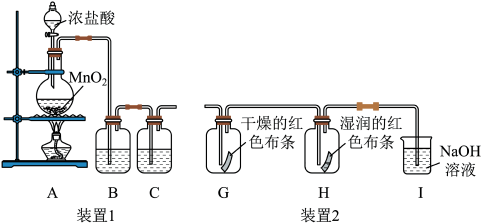
9 . 氯气是一种重要的化工原料,能与有机物和无机物发生反应生成多种氯化物。现用如图装置制取氯气并进行一系列的实验探究。
(1)装置1用来制备纯净、干燥的氯气。
①制备氯气的化学方程式:___________ 。
②B中溶液为___________ ,作用是___________ ,C中液体为___________ ,B和C的位置能否颠倒?___________ (填“能”或“不能”)。
(2)将装置1与装置2连接起来探究氯气是否具有漂白性。
①装置G和H中分别观察到的现象是___________ 。
② 溶液的作用是
溶液的作用是___________ ,写出相应反应的化学方程式:___________ 。工业上常用廉价的石灰乳吸收氯气制得漂白粉,漂白粉的有效成分是___________ (填化学式)。
(3)氯水具有多种成分(分子和离子):
①氯水呈浅黄绿色,是因为有___________ (写化学式)。
②将紫色石蕊溶液滴入新制氯水中,溶液显___________ 色,起作用的微粒是___________ ,一段时间后,溶液的颜色褪去,颜色褪去过程中起作用的微粒是___________ (写化学式)。
(1)装置1用来制备纯净、干燥的氯气。
①制备氯气的化学方程式:
②B中溶液为
(2)将装置1与装置2连接起来探究氯气是否具有漂白性。
①装置G和H中分别观察到的现象是
②
 溶液的作用是
溶液的作用是(3)氯水具有多种成分(分子和离子):
①氯水呈浅黄绿色,是因为有
②将紫色石蕊溶液滴入新制氯水中,溶液显
您最近半年使用:0次
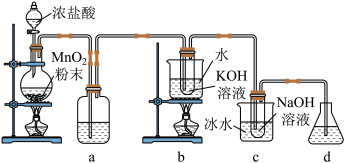
10 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备KClO3和NaClO,探究其氧化还原性质。
(1)盛放浓盐酸的仪器名称是___________ ,a的作用为___________ 。
(2)d中可选用试剂___________(填字母)。
(3)浓盐酸与二氧化锰反应的离子方程式是___________ 。
(4)b中采用的加热方式是___________ ,化学反应的离子方程式是___________ 。
(5)c中采用冰水浴冷却的目的是___________ 。
(6)取少量KClO3和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入CCl4振荡,静置后CCl4层显___________ 色。可知该条件下KClO3的氧化能力___________ (填“大于”或“小于”)NaClO。
(1)盛放浓盐酸的仪器名称是
(2)d中可选用试剂___________(填字母)。
| A.Na2S | B.NaCl | C.Ca(OH)2 | D.H2SO4 |
(3)浓盐酸与二氧化锰反应的离子方程式是
(4)b中采用的加热方式是
(5)c中采用冰水浴冷却的目的是
(6)取少量KClO3和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入CCl4振荡,静置后CCl4层显
您最近半年使用:0次