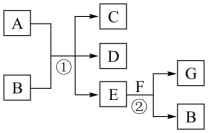
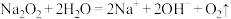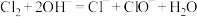1 . 如图所示,反应①为常温下的反应,A、C、D中均含有氯元素,且A中氯元素的化合价介于C和D中氯元素的化合价之间,E在常温下为无色无味的液体,F是淡黄色固体,C为常见的无色气体。请据图回答下列问题:
(1)A的化学式为_______ 。
(2)写出反应①的化学方程式:_______ 。
(3)写出反应②的化学方程式:_______ 。
(4)已知A是一种重要的化工原料,在工农业生产和生活中有着重要的应用。A与石灰乳反应制得的漂白粉的有效成分是_______ (填化学式),该物质在空气中久置失效的原因是_______ (用化学方程式表示)。

(1)A的化学式为
(2)写出反应①的化学方程式:
(3)写出反应②的化学方程式:
(4)已知A是一种重要的化工原料,在工农业生产和生活中有着重要的应用。A与石灰乳反应制得的漂白粉的有效成分是
您最近半年使用:0次
2 . 实验室制取A并进一步制取无水FeCl3的实验装置如图所示。
已知:无水FeCl3在空气中易与水发生作用,加热易升华。
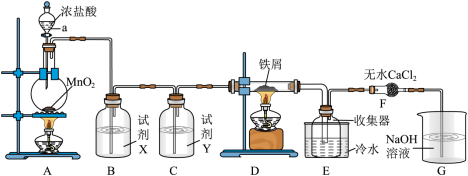
回答下列问题:
(1)仪器a的名称是_______ ,装置A所发生的氧化还原反应中,氧化剂与还原剂的物质的量之比为_______ 。
(2)试剂X是_______ 。
(3)装置F中无水CaCl2的作用是_______
(4)某温度下,将氯气通入G装置中,反应得到NaCl,NaClO和NaClO3的混合溶液,经测定ClO-与ClO 的物质的量之比为4∶1,写出该反应总的离子方程式:
的物质的量之比为4∶1,写出该反应总的离子方程式:_______ 。
已知:无水FeCl3在空气中易与水发生作用,加热易升华。

回答下列问题:
(1)仪器a的名称是
(2)试剂X是
(3)装置F中无水CaCl2的作用是
(4)某温度下,将氯气通入G装置中,反应得到NaCl,NaClO和NaClO3的混合溶液,经测定ClO-与ClO
 的物质的量之比为4∶1,写出该反应总的离子方程式:
的物质的量之比为4∶1,写出该反应总的离子方程式:
您最近半年使用:0次
3 . 按要求填空:
(1)将80克NaOH溶解于水中,配成5L溶液,则NaOH的物质的量浓度是
(2)在同温同压下,等质量铝投入足量盐酸和NaOH溶液中,产生气体的体积之比为
(3)某些化学反应可以表示为A+B→C+D+H2O,若A、C、D均含有氯元素,且A的化合价介于C与D之间,写出该反应的离子方程式:
(4)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为
(5)某+3价阳离子(M3+)含有24个电子,它的质量数为56,该离子核内中子数为
您最近半年使用:0次
名校
4 . 下列离子方程式书写正确的是
| A.硝酸溶液溶解氧化亚铁:FeO+2H+=Fe2++H2O |
| B.用醋酸溶液去除铁锈:Fe2O3+6H+=2Fe3++3H2O |
| C.氯气通入石灰乳中反应:2OH-+Cl2=Cl-+ClO-+H2O |
D.向Ba(OH)2溶液中滴加少量NaHCO3溶液:HCO +OH-+Ba2+=BaCO3↓+H2O +OH-+Ba2+=BaCO3↓+H2O |
您最近半年使用:0次
名校
解题方法
5 . 某小组用下列装置制备 并探究其部分性质,下列说法错误的是
并探究其部分性质,下列说法错误的是
 并探究其部分性质,下列说法错误的是
并探究其部分性质,下列说法错误的是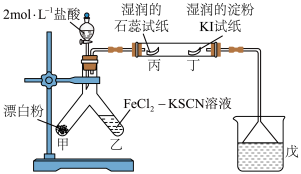
A.漂白粉的主要成分为 和 和 |
B.一段时间后,乙处溶液会变红,丁处湿润的淀粉 试纸会变蓝 试纸会变蓝 |
| C.实验过程中,能观察到丙处湿润的石蕊试纸先变蓝后褪色的现象 |
D.戊处的溶液为 浓溶液,用于吸收尾气中的 浓溶液,用于吸收尾气中的 |
您最近半年使用:0次
2024-03-28更新
|
89次组卷
|
2卷引用:河北省保定市定州市第二中学2023-2024学年高一下学期3月月考化学试题
解题方法
6 . 对浓盐酸与高锰酸钾反应产生的气体进行如下图所示的探究实验,下列分析正确的是
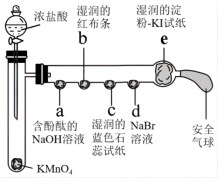

| A.a处酚酞褪色,说明了氯气有漂白性 |
| B.b处湿润的红布条褪色,说明氯气有漂白性 |
| C.c湿润的蓝色石蕊试纸先变红后褪色,说明氯气与水生成了酸性物质和漂白性物质 |
D.d处溶液变成橙黄色、e处试纸变成蓝色,说明氧化性: |
您最近半年使用:0次
7 . 84消毒液适用于家庭、医院、饭店及其他公共场所的物体表面消毒。某小组针对84消毒液的性质展开探究。
实验一:探究84消毒液的氧化性
资料显示:洁厕灵(含盐酸)和84消毒液不能混合使用,否则易产生有毒气体。
他们利用如图所示装置探究上述资料的真实性。
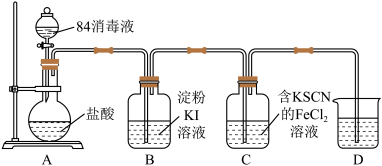
(1)盛装84消毒液的仪器名称是
(2)D装置中应盛装
(3)若B装置中出现
(4)若实验中观察到C装置中溶液先变红色后变黄色,则红色变黄色的原因可能是
实验二:探究84消毒液的漂白性
(5)一定体积和浓度的84消毒液的漂白效率与温度的关系如图所示:
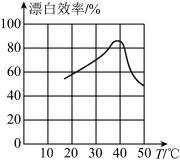
温度高于40℃时,漂白效率急剧减弱的原因可能是
(6)为了探究84消毒液的漂白效率与pH的关系,设计如下实验:
3%的84消毒液 |
|
| 5%品红溶液 | 蒸馏水 | 实验现象 | |
① | 0 | 0 | 2mL | 5滴 | 0 | 不褪色 |
② | 0 | 2mL | 0 | 5滴 | 0 | 不褪色 |
③ | 10mL | 0 | 0 | 5滴 | 5mL | 较快褪色 |
④ | 10mL | 2mL | 0 | 5滴 | 3mL | 缓慢褪色 |
⑤ | 10mL | 0 | 2mL | 5滴 | 3mL | 很快褪色 |
由上述实验可得出的结论是
您最近半年使用:0次
解题方法
8 . 实验室中常用二氧化锰与浓盐酸共热制取氯气。某化学兴趣小组为制取较为纯净、干燥的氯气,设计了如图实验装置。
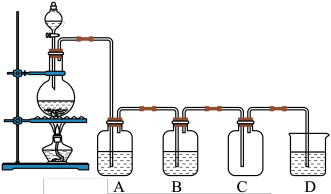
请回答下列问题:
(1)Cl2是_______ 的气体;(填“黄绿色”或“无色”),Cl2气体收集方法为_______ ;(A.向上排空气法B.向下排空气法);实验室制取Cl2的离子方程式为_______ 。
(2)A中盛放的是_______ ,其作用为_______ 。
(3)B中盛放的是_______ ,其作用为_______ 。
(4)D中盛放的是_______ ,其作用为_______ ,相关反应的化学方程式为:_______

请回答下列问题:
(1)Cl2是
(2)A中盛放的是
(3)B中盛放的是
(4)D中盛放的是
您最近半年使用:0次
解题方法
9 . 氮及其化合物在生产、生活中广泛应用。
Ⅰ.氮元素化合价-物质类别关系图如图所示。

(1)图中A可以是__________ (写化学式)。写出一个能够生成B的化学方程式__________ 。
(2)实验室中,检验溶液中是否含有 的操作方法是
的操作方法是__________ 。
(3)水体中硝酸盐含量过高对环境不利,通过电催化法可以将水体中的硝酸盐进行合理转化。写出在中性介质中硝酸盐转化为氮气的阴极电极反应式__________ 。
Ⅱ.下图为实验室模拟尿素法制备水合肼( )的流程图:
)的流程图:
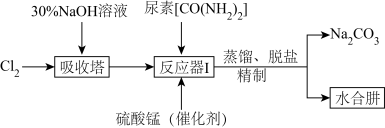
已知:① 易溶于水,具有强还原性,易被氧化成
易溶于水,具有强还原性,易被氧化成 。
。
②一定条件下,碱性NaClO溶液与尿素溶液反应生成 。
。
回答下列问题:
(4)“吸收塔”内发生反应的离子方程式为__________ 。
(5)写出“反应器Ⅰ”中生成水合肼反应的化学方程式为__________ 。
(6)“反应器Ⅰ”要控制NaClO溶液的用量,其主要目的是__________ 。
Ⅰ.氮元素化合价-物质类别关系图如图所示。

(1)图中A可以是
(2)实验室中,检验溶液中是否含有
 的操作方法是
的操作方法是(3)水体中硝酸盐含量过高对环境不利,通过电催化法可以将水体中的硝酸盐进行合理转化。写出在中性介质中硝酸盐转化为氮气的阴极电极反应式
Ⅱ.下图为实验室模拟尿素法制备水合肼(
 )的流程图:
)的流程图:
已知:①
 易溶于水,具有强还原性,易被氧化成
易溶于水,具有强还原性,易被氧化成 。
。②一定条件下,碱性NaClO溶液与尿素溶液反应生成
 。
。回答下列问题:
(4)“吸收塔”内发生反应的离子方程式为
(5)写出“反应器Ⅰ”中生成水合肼反应的化学方程式为
(6)“反应器Ⅰ”要控制NaClO溶液的用量,其主要目的是
您最近半年使用:0次


 置于水中:
置于水中: