解题方法
1 . 下列关于氯气及含氯化合物的叙述中正确的是
| A.可以用向下排空气法收集少量的氯气 |
| B.氯气可以溶于水,但是不能与水发生化学反应 |
| C.在加热的条件下,过量的铁与氯气反应生成氯化铁 |
| D.氯气与氢氧化钠溶液反应时只做氧化剂 |
您最近半年使用:0次
2 . 在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气,进行此实验,所用仪器如图:
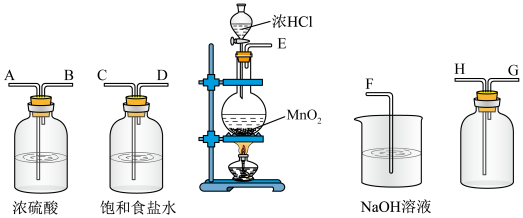
(1)连接上述仪器的正确顺序是___________ 。
 接 ___________,___________接 ___________,___________接___________,___________接
接 ___________,___________接 ___________,___________接___________,___________接 。
。
(2)气体发生装置中进行的反应化学方程式是___________ ;当
 参与反应时,被氧化的
参与反应时,被氧化的 的质量为
的质量为 ___________ ,生成的 在标准状况下的体积约为
在标准状况下的体积约为___________ 。
(3)写出尾气吸收装置中进行的反应的化学方程式___________ 。

(1)连接上述仪器的正确顺序是
 接 ___________,___________接 ___________,___________接___________,___________接
接 ___________,___________接 ___________,___________接___________,___________接 。
。(2)气体发生装置中进行的反应化学方程式是

 参与反应时,被氧化的
参与反应时,被氧化的 的质量为
的质量为  在标准状况下的体积约为
在标准状况下的体积约为(3)写出尾气吸收装置中进行的反应的化学方程式
您最近半年使用:0次
解题方法
3 . 实验室为制备和收集少量干燥、纯净的氯气,选用如图所示仪器及药品:
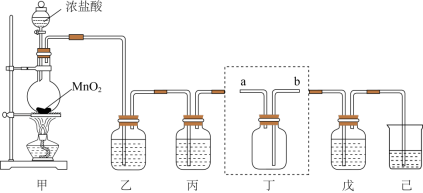
(1)盛装浓盐酸的仪器的名称为___________ 。
(2)写出甲装置中制取氯气的离子方程式___________ 。
(3)装置丁用来收集纯净且干燥的氯气,进气口为___________ (填a或b);装置乙装的试剂是___________ 。(填名称)
(4)将氯气通入装置己中制备“84”漂白液,离子方程式为___________ ,有同学认为装置己还有一个作用,该作用为___________ ,发挥该作用进___________ (填“能”或“不能”)用澄清石灰水代替。
(5)另按如下图所示,在A处通入未经干燥的氯气,若B处的弹簧夹关闭,C处的干燥红布条看不到明显现象;若B处弹簧夹打开,C处的干燥红布条逐渐褪色。

则D瓶中盛放的溶液可能是___________。

(1)盛装浓盐酸的仪器的名称为
(2)写出甲装置中制取氯气的离子方程式
(3)装置丁用来收集纯净且干燥的氯气,进气口为
(4)将氯气通入装置己中制备“84”漂白液,离子方程式为
(5)另按如下图所示,在A处通入未经干燥的氯气,若B处的弹簧夹关闭,C处的干燥红布条看不到明显现象;若B处弹簧夹打开,C处的干燥红布条逐渐褪色。

则D瓶中盛放的溶液可能是___________。
| A.饱和NaCl溶液 | B.NaOH溶液 | C.蒸馏水 | D.浓硫酸 |
您最近半年使用:0次
解题方法
4 . 向盛有氯气的集气瓶中,注入约五分之一容器体积的下列液体并轻轻振荡,观察到的现象记录如图所示。判断瓶中注入的液体是
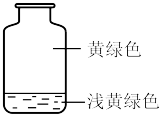

| A.AgNO3溶液 | B.NaOH溶液 | C.水 | D.FeCl2溶液 |
您最近半年使用:0次
名校
5 . 已知X、Y、Z、W均为元素周期表中的短周期元素,它们具有如下特征:
请使用化学用语回答下列问题:
(1)写出Y的两种气体单质的化学式为_______ ,这两种单质的关系是互为_______ ,W的原子结构示意图_______ 。
(2)按从大到小顺序排列X、Y、Z、W的简单离子半径_______ 。
(3)元素Y、Z形成的化合物能与水反应生成Y的气体单质,生成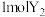 时该反应转移的电子数为
时该反应转移的电子数为_______ ,该化合物阴阳离子个数比为_______ 。元素X、Y形成的化合物也能反应生成Y的气体单质,写出该反应的化学方程式_______ , 该化合物中含有离子数目为
该化合物中含有离子数目为_______ 。
(4)与Z元素同周期的一种金属元素U和一种非金属元素V,它们的最高价氧化物的水化物两两之间可以反应,Z的最高价氧化物的水化物可以检验溶液中是否含有U的离子,写出检验时的实验现象:_______ ,非金属元素V的单质在常温常压下是气体,写出V的单质与Z的最高价氧化物的水化物溶液反应的离子方程式:_______ 。
| 元素 | 特征 |
| X | 在元素周期表中,原子半径最小 |
| Y | 常温下,有 、 、 型两种气体单质存在 型两种气体单质存在 |
| Z | 其原子内层电子数与最外层电子数之比为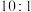 |
| W | 最高化合价为+6价 |
(1)写出Y的两种气体单质的化学式为
(2)按从大到小顺序排列X、Y、Z、W的简单离子半径
(3)元素Y、Z形成的化合物能与水反应生成Y的气体单质,生成
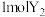 时该反应转移的电子数为
时该反应转移的电子数为 该化合物中含有离子数目为
该化合物中含有离子数目为(4)与Z元素同周期的一种金属元素U和一种非金属元素V,它们的最高价氧化物的水化物两两之间可以反应,Z的最高价氧化物的水化物可以检验溶液中是否含有U的离子,写出检验时的实验现象:
您最近半年使用:0次
6 . 已知氯气与碱反应时,产物受温度影响。实验室中利用如图装置(部分装置省略)制备KClO3和NaClO,并探究其Cl2的氧化还原性质。

回答下列问题:
(1)A装置中a的作用是________ 。
(2)装置A产生氯气的化学方程式为________________ ,此反应中氧化剂与还原剂的个数比为________ ,当得到7.1gCl2时,被氧化的HCl的质量是________ 。
(3)装置B中的试剂为________ ;作用是________________ 。
(4)装置E选用试剂________ (填标号)。
A.NaCl溶液 B.NaOH溶液 C.稀硫酸
(5)装置D反应的离子方程式为________________ 。

回答下列问题:
(1)A装置中a的作用是
(2)装置A产生氯气的化学方程式为
(3)装置B中的试剂为
(4)装置E选用试剂
A.NaCl溶液 B.NaOH溶液 C.稀硫酸
(5)装置D反应的离子方程式为
您最近半年使用:0次
7 . 下列说法不正确 的是
A. 为白色固体,易被空气氧化 为白色固体,易被空气氧化 |
B.工业上常用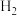 和 和 直接化合的方法生产氯化氢以制得盐酸 直接化合的方法生产氯化氢以制得盐酸 |
C.实验室常用 溶液吸收多余的 溶液吸收多余的 以避免污染 以避免污染 |
D.将废铁屑加入 溶液中,可用于除去工业废气中的 溶液中,可用于除去工业废气中的 |
您最近半年使用:0次
名校
解题方法
8 . 下列实验装置或操作能达到实验目的的是
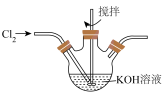 | 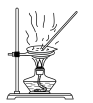 |
| A.制备KClO溶液 | B.由CuCl2溶液制取无水CuCl2 |
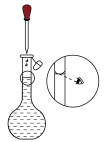 | 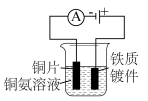 |
| C.配制0.1mol/L的NaCl溶液 | D.铁件上镀铜 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
9 . 某校化学实验兴趣小组为探究卤素单质性质进行了以下实验:
I.为验证卤族元素性质的递变规律,某同学设计了如图所示装置。A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉-KI试纸、沾有NaOH溶液的棉花。

(1)A处反应的离子方程式:___________ ,B处的实验现象为___________ ,C处沾有NaOH溶液的棉花的作用为___________ ;
(2)该实验___________ 验证非金属性Cl>Br>I(填“能”或“不能”),理由是___________ ;
II.已知Cl2可以将Fe2+氧化成Fe3+,为探究Br2能否将Fe2+氧化成Fe3+,某同学甲做了以下实验:在足量的稀氯化亚铁溶液中,加入1~2滴溴水,振荡后观察到溶液呈黄色。
(3)乙同学认为不能据此现象认为Br2氧化性比Fe3+强,理由是___________ ;
(4)丙同学选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了氧化性:Br2>Fe3+。请在表中写出丙同学可能选用的试剂及实验中观察到的现象(供选用的试剂:a.酚酞试液、b.CCl4、c.无水酒精、d.KSCN溶液)。
(5)向FeBr2溶液中通入少量Cl2,发生反应的离子方程式为___________ 。
I.为验证卤族元素性质的递变规律,某同学设计了如图所示装置。A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉-KI试纸、沾有NaOH溶液的棉花。

(1)A处反应的离子方程式:
(2)该实验
II.已知Cl2可以将Fe2+氧化成Fe3+,为探究Br2能否将Fe2+氧化成Fe3+,某同学甲做了以下实验:在足量的稀氯化亚铁溶液中,加入1~2滴溴水,振荡后观察到溶液呈黄色。
(3)乙同学认为不能据此现象认为Br2氧化性比Fe3+强,理由是
(4)丙同学选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了氧化性:Br2>Fe3+。请在表中写出丙同学可能选用的试剂及实验中观察到的现象(供选用的试剂:a.酚酞试液、b.CCl4、c.无水酒精、d.KSCN溶液)。
| 选用试剂(填序号) | 实验现象 | |
| 方案1 | ||
| 方案2 |
(5)向FeBr2溶液中通入少量Cl2,发生反应的离子方程式为
您最近半年使用:0次
解题方法
10 . 84消毒液是常用消毒剂,主要成分为 ,某化学小组在实验室制备84消毒液并探究其相关性质。回答下列问题:
,某化学小组在实验室制备84消毒液并探究其相关性质。回答下列问题:
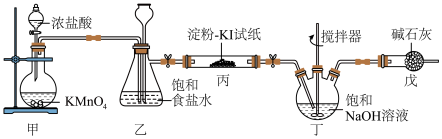
(1)装置甲中盛放浓盐酸的仪器名称是_______ 。
(2)配平方程式:_______ 。
_______MnO +_______Cl-+ _______= _______Mn2++_______Cl2↑+_______
+_______Cl-+ _______= _______Mn2++_______Cl2↑+_______
(3)装置丙中现象_______ 所发生反应的化学方程_______ 。
(4)装置丁制备 的反应中,氧化产物和还原产物的物质的量之比为1∶1,若要制取
的反应中,氧化产物和还原产物的物质的量之比为1∶1,若要制取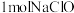 ,理论上反应中转移电子数为
,理论上反应中转移电子数为___ 。
(5)装置戊的作用是_______ 装置乙饱和食盐水作用_______ 。
 ,某化学小组在实验室制备84消毒液并探究其相关性质。回答下列问题:
,某化学小组在实验室制备84消毒液并探究其相关性质。回答下列问题:
(1)装置甲中盛放浓盐酸的仪器名称是
(2)配平方程式:
_______MnO
 +_______Cl-+ _______= _______Mn2++_______Cl2↑+_______
+_______Cl-+ _______= _______Mn2++_______Cl2↑+_______(3)装置丙中现象
(4)装置丁制备
 的反应中,氧化产物和还原产物的物质的量之比为1∶1,若要制取
的反应中,氧化产物和还原产物的物质的量之比为1∶1,若要制取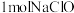 ,理论上反应中转移电子数为
,理论上反应中转移电子数为(5)装置戊的作用是
您最近半年使用:0次



