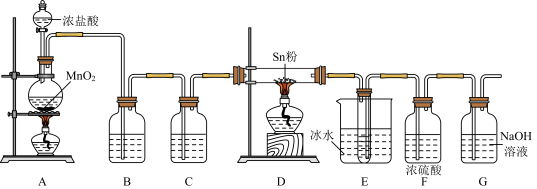
1 . 四氯化锡(SnCl4)常用作分析试剂、有机合成脱水剂等。设计如下装置制备SnCl4.
②装置D中发生反应:Sn+2Cl2 SnCl4.
SnCl4.
回答下列问题:
(1)装置A中反应的化学方程式为______ ,若反应中消耗1molMnO2,则生成Cl2的体积为______ L(标准状况下)。
(2)实验前,应进行的操作是______ 。
(3)装置B、C所盛装的试剂分别是______ 、______ (填字母),装置F的作用是______ 。
a.饱和食盐水 b.浓硫酸 c.饱和碳酸氢钠溶液 d.碱石灰 e.无水硫酸铜 f.无水氯化钙
(4)装置E中使用冰水浴的目的是______ 。
(5)常温下,装置G中发生反应的离子方程式为______ 。
②装置D中发生反应:Sn+2Cl2
 SnCl4.
SnCl4.回答下列问题:
(1)装置A中反应的化学方程式为
(2)实验前,应进行的操作是
(3)装置B、C所盛装的试剂分别是
a.饱和食盐水 b.浓硫酸 c.饱和碳酸氢钠溶液 d.碱石灰 e.无水硫酸铜 f.无水氯化钙
(4)装置E中使用冰水浴的目的是
(5)常温下,装置G中发生反应的离子方程式为
您最近半年使用:0次
2024-04-13更新
|
150次组卷
|
2卷引用:2024届西藏自治区拉萨市高三上学期第一次模拟考试理综试题
名校
2 . 下列化学方程式不正确 的是
A.Cl2通入氢氧化钠溶液: |
B.H2SO3溶液中滴入氯化钙: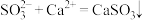 |
C.将少量SO2气体通入NaClO溶液中: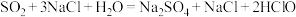 |
D.氧化铝溶于氢氧化钠: |
您最近半年使用:0次
名校
解题方法
3 . 有关Cl2的性质,下列说法不正确的是
| A.Cl2有毒但可用于自来水消毒 |
| B.能与Ca(OH)2溶液反应生成两种正盐 |
| C.过量的Fe在氯气中燃烧生成FeCl3 |
| D.将氯气和二氧化硫分别通入到紫色石蕊溶液中现象相同 |
您最近半年使用:0次
4 . 化学与社会、生活密切相关。下列说法不正确 的是
| A.液氨汽化时要吸收大量的热,可用作制冷剂 | B.葡萄酒添加微量SO2可杀菌、保鲜 |
| C.氯气可用于制漂白粉 | D.水晶、玛瑙都属于硅酸盐工业产品 |
您最近半年使用:0次
解题方法
5 . 将Cl2通入70℃的氢氧化钠水溶液中,发生以下反应(未配平):
 ,反应完成后测得溶液中NaClO与NaClO3的物质的量浓度之比为5:2,则该溶液中NaClO与NaCl的物质的量之比为
,反应完成后测得溶液中NaClO与NaClO3的物质的量浓度之比为5:2,则该溶液中NaClO与NaCl的物质的量之比为
 ,反应完成后测得溶液中NaClO与NaClO3的物质的量浓度之比为5:2,则该溶液中NaClO与NaCl的物质的量之比为
,反应完成后测得溶液中NaClO与NaClO3的物质的量浓度之比为5:2,则该溶液中NaClO与NaCl的物质的量之比为| A.5:2 | B.2:5 | C.5:16 | D.1:3 |
您最近半年使用:0次
名校
解题方法
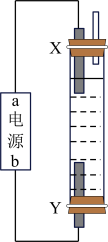
6 . 利用氢一氧燃料电池可以充当电源电解饱和食盐水制备84消毒液(如图)。则X是_____ (填电极名称),Y极电极反应式为_____ 。
您最近半年使用:0次
7 . 下列有关物质的用途错误的是
A.工业上用 与石灰乳反应制备漂白粉 与石灰乳反应制备漂白粉 |
B. 可作呼吸面罩的供氧剂 可作呼吸面罩的供氧剂 |
| C.食盐可用作防腐剂 |
D. 固体可作粉刷墙壁的红色涂料 固体可作粉刷墙壁的红色涂料 |
您最近半年使用:0次
8 . 某研究性学习小组欲利用下列装置制取少量次氯酸钠,并进一步探究市场所售的84消毒液成分性质。
①中利用反应MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O制取氯气。
MnCl2+Cl2↑+2H2O制取氯气。
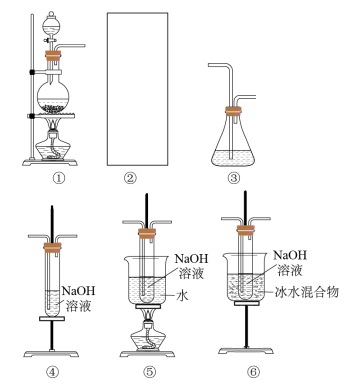
相关资料:已知制备84消毒液的反应属于放热反应,温度稍高时便发生副反应:3Cl2+6NaOH=NaClO3+5NaCl+3H2O。
(1)请在上图装置A、B、C中选择一个合适的装置放在②处制消毒液:___________ 。
(2)请写出②中制备消毒液的离子方程式___________ 。
(3)请用双线桥法标出下方副反应化学方程式的电子转移方向和数目:___________ 3Cl2+6NaOH=NaClO3+5NaCl+3H2O
(4)当收集了约448mL Cl2(标准状况下)时,反应消耗的HCl的物质的量为___________ mol。
(5)研究小组中部分同学想继续探究市场所售的84消毒液成分与性质,分别做了以下实验: 需将表格填写完整
需将表格填写完整
①中利用反应MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O制取氯气。
MnCl2+Cl2↑+2H2O制取氯气。
相关资料:已知制备84消毒液的反应属于放热反应,温度稍高时便发生副反应:3Cl2+6NaOH=NaClO3+5NaCl+3H2O。
(1)请在上图装置A、B、C中选择一个合适的装置放在②处制消毒液:
(2)请写出②中制备消毒液的离子方程式
(3)请用双线桥法标出下方副反应化学方程式的电子转移方向和数目:
(4)当收集了约448mL Cl2(标准状况下)时,反应消耗的HCl的物质的量为
(5)研究小组中部分同学想继续探究市场所售的84消毒液成分与性质,分别做了以下实验:
 需将表格填写完整
需将表格填写完整
| 实验操作 | 预期现象 | 实际现象 | 结论及解释 |
| 1.向少量84消毒液中滴入酚酞试液 | 变红 | 先变红,后慢慢褪色 | ① |
| 2.向少量84消毒液中加入FeCl3溶液 | 有红褐色沉淀产生 | 有红褐色沉淀产生,同时有气泡生成 | 产生了Fe(OH)3沉淀,同时可能产生了CO2气体 |
| 3.向少量84消毒液中加入AgNO3溶液,最后加入稀硝酸 | 有白色沉淀产生 | 有白色沉淀产生,加入稀硝酸,沉淀部分溶解,且有气泡产生 | ② |
您最近半年使用:0次
9 . Cl2、SO2、CO2均是中学化学常见的气体,减少Cl2、SO2的排放可以防止污染空气,减少CO2的排放,有利于保护环境,实现碳中和。回答下列问题:
(1)化工厂可用浓氨水来检验Cl2是否泄漏,当有少量Cl2泄漏时,可以观察到的现象是________ 。
(2)用热烧碱溶液吸收Cl2反应后的混合溶液,若含NaCl、NaClO和NaClO3物质的量比值为n∶1∶2,则n=________ 。
(3)常温下,可用NaOH溶液作CO2的捕捉剂。若经测定某次捕捉所得溶液中,Na和C两种元素物质的量比值为3:1,则所得溶液中溶质成分为________ (填化学式)。
(4)①除品红外,鉴别SO2、CO2两种气体还可以采用________ (填试剂名称),SO2、Cl2均有漂白性,若将两者1∶1通入品红溶液中,不能使品红褪色,理由是________ (写离子方程式),除去SO2中的HCl可采用________ (填试剂名称)。
②用硫酸酸化的K2Cr2O7溶液处理SO2气体,会析出铬钾矾[KCr(SO4)2·12H2O]晶体。写出该反应的化学方程式:________ 。
(1)化工厂可用浓氨水来检验Cl2是否泄漏,当有少量Cl2泄漏时,可以观察到的现象是
(2)用热烧碱溶液吸收Cl2反应后的混合溶液,若含NaCl、NaClO和NaClO3物质的量比值为n∶1∶2,则n=
(3)常温下,可用NaOH溶液作CO2的捕捉剂。若经测定某次捕捉所得溶液中,Na和C两种元素物质的量比值为3:1,则所得溶液中溶质成分为
(4)①除品红外,鉴别SO2、CO2两种气体还可以采用
②用硫酸酸化的K2Cr2O7溶液处理SO2气体,会析出铬钾矾[KCr(SO4)2·12H2O]晶体。写出该反应的化学方程式:
您最近半年使用:0次
10 . 下列离子方程式书写正确的是
A.碳酸氢钠溶液与稀盐酸混合:CO +2H+=CO2↑+H2O +2H+=CO2↑+H2O |
| B.氢氧化铝治疗胃酸过多:Al(OH)3+3H+=Al3++3H2O |
C.向CaCO3悬浊液中通入足量CO2:CO +CO2+H2O=2HCO +CO2+H2O=2HCO |
| D.氯气通入冷的石灰乳制漂白粉:Cl2+2OH-=Cl-+ClO-+H2O |
您最近半年使用:0次



