1 . 在指定条件下,下列选项所示的物质间转化能实现的是
A.Al2O3(s) Al(OH)3(s) Al(OH)3(s) | B.Cl2(g)  NaClO(aq) NaClO(aq) |
C.FeCl3(aq)  Fe(s) Fe(s) | D.BaCl2(aq)  BaCO3(s) BaCO3(s) |
您最近半年使用:0次
解题方法
2 . 下列反应的离子方程式正确的是
| A.向FeCl3溶液中通入H2S气体:2Fe3++H2S=2Fe2++S↓+2H+ |
B.向AlCl3溶液中滴加过量氨水:Al+4NH3·H2O= +4 +4 +2H2O +2H2O |
| C.将Cl2通入冷的石灰乳中制漂白粉:2OH-+Cl2=Cl-+ClO-+H2O |
D.向Ba(OH)2溶液中滴加H2SO4溶液至沉淀完全:Ba2++ +H++OH-=BaSO4↓+H2O +H++OH-=BaSO4↓+H2O |
您最近半年使用:0次
解题方法
3 . 实验室模拟工业漂白液脱除废水中氨氮 的流程如下:
的流程如下:
粗盐水 精制盐水
精制盐水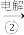 Cl2
Cl2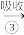 漂白液
漂白液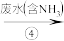 NaCl
NaCl
下列分析正确的是
 的流程如下:
的流程如下:粗盐水
 精制盐水
精制盐水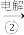 Cl2
Cl2 漂白液
漂白液 NaCl
NaCl下列分析正确的是
A.漂白液的有效成分是 |
| B.①中蒸发浓缩粗盐水,不用加入其它试剂,即可得到纯氯化钠 |
C.③中制备漂白液的反应: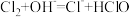 |
| D.②、③、④中均发生了氧化还原反应 |
您最近半年使用:0次
4 . 下列有关物质的工业制备反应正确的是
A.制烧碱:  |
B.炼铁:  |
C.制漂粉精: 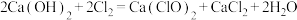 |
D.制乙烯: 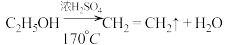 |
您最近半年使用:0次
解题方法
5 . 下列所涉及的离子方程式书写正确的是
| 选项 | 用途或者制备 | 离子方程式 |
| A | 用稀硫酸清洗铁锈 |  |
| B | 大理石与稀盐酸反应制备二氧化碳 | 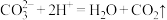 |
| C | 用氢氧化钠溶液吸收氯气 |  |
| D | 氧化铝与氢氧化钠溶液 |  |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
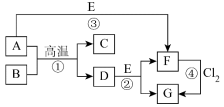
6 . 部分元素的单质及其化合物(或其溶液)的转化关系如图。已知A是生活中使用广泛的金属单质,常温下B是无色无味的液体,E是胃酸的主要成分。
(1)写出下列物质的化学式:E___________ ;G___________ 。
(2)反应①的化学方程式为___________ ;反应②的离子方程式为___________ 。
(3)F溶液常温下呈浅绿色,该溶液中金属阳离子为___________ (填离子符号),反应④中氧化剂和还原剂的物质的量之比为___________ 。
(4)Cl2通入到石灰乳中可以制成一种常用的消毒剂,其有效成分为___________ (填化学式)。
(1)写出下列物质的化学式:E
(2)反应①的化学方程式为
(3)F溶液常温下呈浅绿色,该溶液中金属阳离子为
(4)Cl2通入到石灰乳中可以制成一种常用的消毒剂,其有效成分为
您最近半年使用:0次
解题方法
7 . 向KOH溶液中通入11.2 L(标准状况)氯气恰好完全反应,生成三种含氯盐:0.7 mol KCl、0.2 mol KClO和X。则X是
| A.0.15 mol KClO4 | B.0.1 mol KClO3 | C.0.2 mol KClO2 | D.0.3 mol KClO2 |
您最近半年使用:0次
名校
8 . 下列物质的用途或者制备中所涉及到的离子方程式书写正确的是
| 选项 | 用途或者制备 | 离子方程式 |
| A | 往饱和碳酸钠溶液中通入CO2 |  +CO2+H2O=2 +CO2+H2O=2 |
| B | 实验室用大理石与稀盐酸反应制备二氧化碳 |  +2H+=H2O+CO2↑ +2H+=H2O+CO2↑ |
| C | 用氢氧化钠溶液吸收氯气 | Cl2+2OH-=Cl-+ClO-+H2O |
| D | 用氯化铁溶液刻蚀铜板 | Fe3++Cu=Fe2++Cu2+ |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
9 . 下列离子方程式书写正确的是
| A.稀硫酸与氢氧化钡溶液的反应:OH-+H+=H2O |
| B.铁和稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
| C.氯气与氢氧化钠溶液反应:Cl2+2OH-=Cl-+ClO-+H2O |
| D.铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag |
您最近半年使用:0次
10 . 下列生产生活中涉及的反应方程式正确的是
| A.用TiCl4制备TiCl4+(x+2)H2O=TiO2·xH2O↓+4HCl |
B.用食醋和淀粉-KI溶液检验加碘盐中的IO ,IO ,IO +5I-+6H+=3I2+3H2O +5I-+6H+=3I2+3H2O |
C.工业制硫酸时黄铁矿在足量氧气中煅烧:4FeS+15O2 8SO3+2Fe2O3 8SO3+2Fe2O3 |
| D.Cl2通入石灰乳中制漂白粉:Cl2+2OH-=Cl-+ClO-+H2O |
您最近半年使用:0次



