解题方法
1 . 氯气是一种重要的化工原料,大量用于制造盐酸、漂白剂、农药、染料和药品等。
(1)1774年,瑞典化学家舍勒将浓盐酸与软锰矿(主要成分为 )混合加热,发现了氯气。下图为实验室制取Cl2的装置,请回答:
)混合加热,发现了氯气。下图为实验室制取Cl2的装置,请回答:
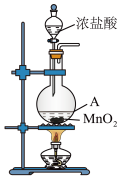
盛放浓盐酸的仪器名称是_______ 。
(2)下图所示制取氯气的净化、收集、尾气处理的装置能达到实验目的的是_______ 。(填序号)
(3)已知:常温下用 和市售浓盐酸(11.9
和市售浓盐酸(11.9 )反应制取Cl2难以进行。但若用漂白粉(有效成分
)反应制取Cl2难以进行。但若用漂白粉(有效成分 )、高锰酸钾等与浓盐酸反应,常温下很容易制取Cl2。
)、高锰酸钾等与浓盐酸反应,常温下很容易制取Cl2。
①已知,如图装置A是氯气的发生装置。加入适量的浓盐酸充分反应有黄绿色气体生成,写出发生反应的化学方程式,并用单线桥标明电子转移的方向和数目 :_______ 。

②装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅲ处应放入的是_______ (填序号)。
a.干燥的有色布条 b.湿润的有色布条 c.湿润的淀粉 试纸
试纸
装置C的Ⅱ处的试剂是_______ (填序号)。
a.碱石灰(氢氧化钠和氧化钙的固体混合物) b.无水氯化钙 c.浓硫酸
③装置D中一般不用 澄清石灰水吸收多余的氯气。理由是_______ 。
(4)84消毒液是一种常见的含氯消毒剂,其有效成分为次氯酸钠。
资料:84消毒液中含氯微粒主要有 、
、 、
、 ;相同浓度时,
;相同浓度时, 的氧化性强于
的氧化性强于 ;
; 是反映水溶液中所有物质表现出来的氧化—还原性,
是反映水溶液中所有物质表现出来的氧化—还原性, 值越大,氧化性越强。
值越大,氧化性越强。
某兴趣小组同学研究84消毒液的漂白性,实验如下。
I.向2 84消毒液中加入2
84消毒液中加入2 水后,放入红色纸片,观察到纸片慢慢褪色。
水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.向2 84消毒液中加入2
84消毒液中加入2 白醋后,放入红色纸片,观察到纸片迅速褪色。
白醋后,放入红色纸片,观察到纸片迅速褪色。
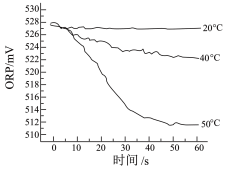
Ⅲ.测得84消毒液在不同温度时 随时间的变化曲线如
随时间的变化曲线如图 。
①已知白醋显酸性,不具有漂白性。实验I、Ⅱ现象不同的原因是_______ 。
②由实验Ⅲ可得出的结论是_______ 。
(1)1774年,瑞典化学家舍勒将浓盐酸与软锰矿(主要成分为
 )混合加热,发现了氯气。下图为实验室制取Cl2的装置,请回答:
)混合加热,发现了氯气。下图为实验室制取Cl2的装置,请回答:
盛放浓盐酸的仪器名称是
(2)下图所示制取氯气的净化、收集、尾气处理的装置能达到实验目的的是
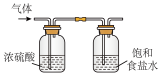 | 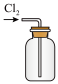 |  |
| A.净化Cl2 | B.收集Cl2 | C.尾气处理 |
(3)已知:常温下用
 和市售浓盐酸(11.9
和市售浓盐酸(11.9 )反应制取Cl2难以进行。但若用漂白粉(有效成分
)反应制取Cl2难以进行。但若用漂白粉(有效成分 )、高锰酸钾等与浓盐酸反应,常温下很容易制取Cl2。
)、高锰酸钾等与浓盐酸反应,常温下很容易制取Cl2。①已知,如图装置A是氯气的发生装置。加入适量的浓盐酸充分反应有黄绿色气体生成,写出发生反应的化学方程式,并用

②装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅲ处应放入的是
a.干燥的有色布条 b.湿润的有色布条 c.湿润的淀粉
 试纸
试纸装置C的Ⅱ处的试剂是
a.碱石灰(氢氧化钠和氧化钙的固体混合物) b.无水氯化钙 c.浓硫酸
③装置D中一般
(4)84消毒液是一种常见的含氯消毒剂,其有效成分为次氯酸钠。
资料:84消毒液中含氯微粒主要有
 、
、 、
、 ;相同浓度时,
;相同浓度时, 的氧化性强于
的氧化性强于 ;
; 是反映水溶液中所有物质表现出来的氧化—还原性,
是反映水溶液中所有物质表现出来的氧化—还原性, 值越大,氧化性越强。
值越大,氧化性越强。某兴趣小组同学研究84消毒液的漂白性,实验如下。
I.向2
 84消毒液中加入2
84消毒液中加入2 水后,放入红色纸片,观察到纸片慢慢褪色。
水后,放入红色纸片,观察到纸片慢慢褪色。Ⅱ.向2
 84消毒液中加入2
84消毒液中加入2 白醋后,放入红色纸片,观察到纸片迅速褪色。
白醋后,放入红色纸片,观察到纸片迅速褪色。Ⅲ.测得84消毒液在不同温度时
 随时间的变化曲线如
随时间的变化曲线如
①已知白醋显酸性,不具有漂白性。实验I、Ⅱ现象不同的原因是
②由实验Ⅲ可得出的结论是
您最近半年使用:0次
2 . 如图为实验室制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条 ,F中为红色的铜网 ,其右端出气管口放有脱脂棉。
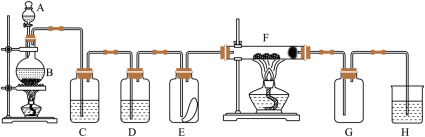
(1)仪器A的名称是_______ ,烧瓶中反应的化学方程式是_______ 。
(2)装置C中的物质是_______ 。装置D的作用是_______ 。
(3)E中红色布条是否褪色(填“是”或“否”)_______ ,F中反应的化学方程式为_______ 。
(4)H处溶液为NaOH溶液,其作用是_______ 。试写出H处所发生反应的离子反应方程式_______ 。

(1)仪器A的名称是
(2)装置C中的物质是
(3)E中红色布条是否褪色(填“是”或“否”)
(4)H处溶液为NaOH溶液,其作用是
您最近半年使用:0次
3 . 某同学在培养皿上做如下实验(如图所示),a、b、c、d是浸有相关溶液的滤纸。向 晶体上滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
晶体上滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
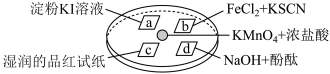
下列对实验现象的“解释或结论”描述,不正确的是
 晶体上滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
晶体上滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
下列对实验现象的“解释或结论”描述,不正确的是
选项 | 实验现象 | 解释或结论 |
A | a处试纸变蓝 | 还原性: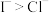 |
B | b处试纸变红 |  |
C | c处试纸褪色 |  与 与 反应生成了具有漂白性的物质 反应生成了具有漂白性的物质 |
D | d处红色褪去 |  和 和 反应使溶液呈中性 反应使溶液呈中性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
4 . 下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | 牙膏中常加入含氟物质预防龋齿 | 氟磷灰石的溶解度小于羟基磷灰石 |
B | 气态氢化物稳定性: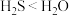 | 分子间作用力: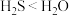 |
C | 电解食盐水制备氯气和氢氧化钠 | 氯气和氢氧化钠溶液反应制备漂白液 |
D | 饱和 溶液导电性比饱和 溶液导电性比饱和 溶液强 溶液强 |  溶液碱性强于 溶液碱性强于 溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
5 . 下列说法中,正确的个数是
①0℃,101kPa含有1mol硫原子的SO2与SO3的混合物,其体积小于22.4L
②不能用澄清石灰水鉴别CO2和SO2
③常温下,铝可溶于过量浓硝酸,也可溶于过量NaOH溶液
④向SiO2固体中滴加NaOH溶液或氢氟酸,固体均溶解,说明SiO2是两性氧化物
⑤工业上通常使用电解熔融氯化铝的方式制备金属铝
⑥可用澄清石灰水吸收反应产生的Cl2制备漂白粉
①0℃,101kPa含有1mol硫原子的SO2与SO3的混合物,其体积小于22.4L
②不能用澄清石灰水鉴别CO2和SO2
③常温下,铝可溶于过量浓硝酸,也可溶于过量NaOH溶液
④向SiO2固体中滴加NaOH溶液或氢氟酸,固体均溶解,说明SiO2是两性氧化物
⑤工业上通常使用电解熔融氯化铝的方式制备金属铝
⑥可用澄清石灰水吸收反应产生的Cl2制备漂白粉
| A.2个 | B.3个 | C.4个 | D.5个 |
您最近半年使用:0次
2024-04-03更新
|
223次组卷
|
2卷引用:江苏省无锡市第一中学2023-2024学年高一下学期3月月考化学试题
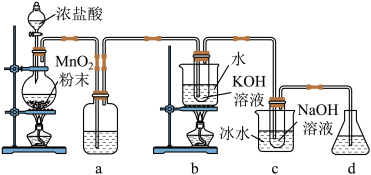
6 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中用下图装置(部分装置省略)制备氯气,并利用其与碱反应时的温度控制制备KClO3和NaClO。
回答下列问题:
(1)盛放浓盐酸的仪器名称是___________ ,a中的试剂为___________ ,d的作用是___________ 。
(2)制备氯气的化学方程式是___________ 。(双线桥表示电子的转移方向和数目)
(3)反应结束后,取出b中试管,经___________ ,过滤,洗涤干燥,得到KClO3晶体。
(4)c中制备NaClO的离子方程式是___________ ;温度过高会生成KClO3。当n(NaClO)=n(KClO3)时,该反应中n(Cl2):n(NaCl)=___________
(5)取少量KClO3和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入CCl4振荡,静置后CCl4显紫红色。可知该条件下NaClO的氧化能力___________ KClO3 (填“大于”或“小于”)。
(6)反应结束后多余的氯气也可以制成氯水使用。下图是用强光照射密闭广口瓶中新制氯水时,用数字化传感器采集的图像,下列纵坐标代表的物理量与图像相符的是___________ 。
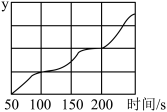
a.瓶中氯气的体积分数 b.瓶中氧气的体积分数
c.溶液的导电能力 d.溶液的漂白能力

回答下列问题:
(1)盛放浓盐酸的仪器名称是
(2)制备氯气的化学方程式是
(3)反应结束后,取出b中试管,经
(4)c中制备NaClO的离子方程式是
(5)取少量KClO3和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入CCl4振荡,静置后CCl4显紫红色。可知该条件下NaClO的氧化能力
(6)反应结束后多余的氯气也可以制成氯水使用。下图是用强光照射密闭广口瓶中新制氯水时,用数字化传感器采集的图像,下列纵坐标代表的物理量与图像相符的是

a.瓶中氯气的体积分数 b.瓶中氧气的体积分数
c.溶液的导电能力 d.溶液的漂白能力
您最近半年使用:0次
解题方法
7 . 无水ZnCl2常用作有机合成的脱水剂、缩合剂和催化剂。无水ZnCl2易吸水潮解。某化学兴趣小组的同学设计如下实验方案制备无水ZnCl2,并测定其纯度,实验装置如图所示:
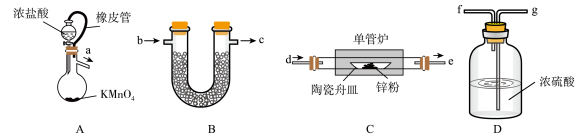
(1)装置A中反应的离子方程式为______ ;装置A中橡皮管的作用为______ 。
(2)按气流从左到右的方向,装置合理的连接顺序为a→______→______d→e→______(填接口小写字母)。______
(3)装置B中药品的作用为______ 。
(4)氯化锌纯度的测定:将ag试样配成100mL溶液。取20.00mL,加入磷酸三钠消除干扰离子后,滴入两滴半二甲酚橙作指示剂,用bmol/LEDTA(Na2H2Y)标准溶液滴定Zn2+,反应的离子方程式为Zn2++H2Y2-=ZnY2-+H+,达到终点时,消耗EDTA溶液的平均体积为5.00mL。
①配制100mLZnCl2溶液需用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管、______ 。
②该氯化锌试样中氯化锌的质量分数为______ (用含a、b的代数式表示)。

(1)装置A中反应的离子方程式为
(2)按气流从左到右的方向,装置合理的连接顺序为a→______→______d→e→______(填接口小写字母)。
(3)装置B中药品的作用为
(4)氯化锌纯度的测定:将ag试样配成100mL溶液。取20.00mL,加入磷酸三钠消除干扰离子后,滴入两滴半二甲酚橙作指示剂,用bmol/LEDTA(Na2H2Y)标准溶液滴定Zn2+,反应的离子方程式为Zn2++H2Y2-=ZnY2-+H+,达到终点时,消耗EDTA溶液的平均体积为5.00mL。
①配制100mLZnCl2溶液需用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管、
②该氯化锌试样中氯化锌的质量分数为
您最近半年使用:0次
名校
解题方法
8 . 如图是一种测试某气体化学性质的装置,图中b为开关,如先打开b,在a处通入湿润的氯气,c中干燥的红色布条颜色褪去;当关闭b时,c中干燥的红色布条颜色无变化,则d瓶中盛有的溶液可以是
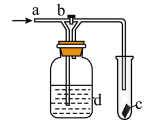
①浓H2SO4 ②饱和NaCl溶液 ③浓NaOH溶液 ④石灰乳

①浓H2SO4 ②饱和NaCl溶液 ③浓NaOH溶液 ④石灰乳
| A.①② | B.②③ | C.②④ | D.①③④ |
您最近半年使用:0次
解题方法
9 . 写出下列物质的反应方程式
(1)过氧化钠与水的反应______ 。
(2)氯气与水的反应______ 。
(3)氯气与氢氧化钙的反应______ 。
(4)碳酸氢钠受热分解之后的反应______ 。
(5)氧化铝与盐酸的反应______ 。
(6)氯气和铁的反应______ 。
(7)钠与水的反应______ 。
(8)硫酸亚铁与氢氧化钠的反应______ 。
(9)铁与水蒸气的反应______ 。
(10)氢氧化亚铁氧气与水的反应______ 。
(1)过氧化钠与水的反应
(2)氯气与水的反应
(3)氯气与氢氧化钙的反应
(4)碳酸氢钠受热分解之后的反应
(5)氧化铝与盐酸的反应
(6)氯气和铁的反应
(7)钠与水的反应
(8)硫酸亚铁与氢氧化钠的反应
(9)铁与水蒸气的反应
(10)氢氧化亚铁氧气与水的反应
您最近半年使用:0次
10 . 实验室用浓盐酸和 制
制 ,并以干燥的
,并以干燥的 为原料制备无水
为原料制备无水 。已知
。已知 易升华,易吸收水分而潮解。装置如下图所示。
易升华,易吸收水分而潮解。装置如下图所示。

(1)装置A中发生的化学方程式为__________ ,装置B、C中应盛放的试剂名称为__________ 。
(2)从A装置导出的气体若不经过B、C装置而直接进入D管,将对实验产生的不良后果是__________ 。
(3)实验时,先点燃__________ 处的酒精灯,其目的是__________ ,写出D中反应的化学方程式:__________ 。
(4)F装置所起的作用是__________ 和防止空气中的水蒸气进入E中。
(5)生产84消毒液是将氯气通入NaOH溶液中,发生反应的离子方程式为__________ 。
(6)84消毒液稀释后喷洒在空气中,可以生成有漂白性的物质,请写出此过程的化学方程式:__________ 。
 制
制 ,并以干燥的
,并以干燥的 为原料制备无水
为原料制备无水 。已知
。已知 易升华,易吸收水分而潮解。装置如下图所示。
易升华,易吸收水分而潮解。装置如下图所示。
(1)装置A中发生的化学方程式为
(2)从A装置导出的气体若不经过B、C装置而直接进入D管,将对实验产生的不良后果是
(3)实验时,先点燃
(4)F装置所起的作用是
(5)生产84消毒液是将氯气通入NaOH溶液中,发生反应的离子方程式为
(6)84消毒液稀释后喷洒在空气中,可以生成有漂白性的物质,请写出此过程的化学方程式:
您最近半年使用:0次



