名校
解题方法
1 .  是原子序数依次增大的短周期主族元素,X与Z同主族,Z的最高正价与最低负价之和为4,Y在同周期中半径最大,下列说法正确的是
是原子序数依次增大的短周期主族元素,X与Z同主族,Z的最高正价与最低负价之和为4,Y在同周期中半径最大,下列说法正确的是
 是原子序数依次增大的短周期主族元素,X与Z同主族,Z的最高正价与最低负价之和为4,Y在同周期中半径最大,下列说法正确的是
是原子序数依次增大的短周期主族元素,X与Z同主族,Z的最高正价与最低负价之和为4,Y在同周期中半径最大,下列说法正确的是A.简单氢化物沸点: | B.最高价氧化物对应的水化物的酸性: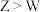 |
| C.X与Y形成的化合物中只有离子键 | D.W的单质可用于制备漂白液 |
您最近半年使用:0次
名校
解题方法
2 . 将一定量的氯气通入30ml浓度为10mol/L的氢氧化钠浓溶液中,加热少许时间后恰好完全反应,形成了 、
、 、
、 共存体系,下列判断不正确的是
共存体系,下列判断不正确的是
 、
、 、
、 共存体系,下列判断不正确的是
共存体系,下列判断不正确的是A.当溶液中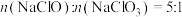 时,反应的离子方程式为 时,反应的离子方程式为 |
B.与 反应的氯气为3.36L 反应的氯气为3.36L |
C. 可能为8∶3∶1 可能为8∶3∶1 |
D.溶液中氯离子的物质的量取值范围是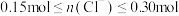 |
您最近半年使用:0次
名校
3 .  是一种常用的试剂。下列探究其用途的装置或操作能达到相应实验目的的是
是一种常用的试剂。下列探究其用途的装置或操作能达到相应实验目的的是

 是一种常用的试剂。下列探究其用途的装置或操作能达到相应实验目的的是
是一种常用的试剂。下列探究其用途的装置或操作能达到相应实验目的的是
A.用操作甲鉴别 溶液和 溶液和 溶液 溶液 |
B.用装置乙除去 气体中的 气体中的 |
C.用装置丙吸收多余的 |
D.用操作丁制备少量 固体 固体 |
您最近半年使用:0次
4 . 高铁酸钾(K2FeO4)是一种环保、高效、多功能饮用水处理剂,制备流程如图所示:
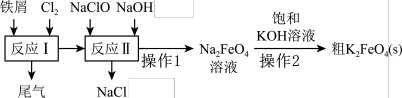
下列叙述不正确的是

下列叙述不正确的是
| A.反应I产生的尾气可通入澄清石灰水中吸收 |
| B.反应I生成的FeCl3,在碱性条件下会被NaClO氧化成Na2FeO4 |
| C.反应II中每消耗3个ClO-转移6个电子 |
| D.Na2FeO4转化成K2FeO4的反应是氧化还原反应 |
您最近半年使用:0次
名校
解题方法
5 . 为除去括号内的杂质,所选用的试剂或方法错误的是
| A.Cl2(水蒸气):将混合气体通过盛有碱石灰的球形干燥管 |
| B.Na2CO3固体粉末(NaHCO3):加热到固体质量不再减轻为止 |
| C.NaHCO3溶液(Na2CO3):向溶液中加入适量CaCl2溶液,过滤 |
| D.Cl2(HCl):将混合气体通过饱和食盐水 |
您最近半年使用:0次
名校
解题方法
6 . 如图所示,若关闭阀门Ⅰ,打开阀门Ⅱ,让一种含氯气的气体经过甲瓶后,通入乙瓶,布条不褪色;若关闭阀门Ⅱ,打开阀门Ⅰ,再通入这种气体,布条褪色。甲瓶中所盛的试剂可能是


| A.蒸馏水 | B.浓硫酸 | C.氢氧化钡溶液 | D.饱和氯化钾溶液 |
您最近半年使用:0次
名校
解题方法
7 . 下列反应的相关方程式书写不正确的是
A.氯气通入冷的石灰乳中制取漂白粉: |
B.钠与水反应: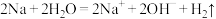 |
C.将 通入 通入 溶液中: 溶液中: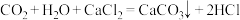 |
D.氢氧化铁胶体的制备: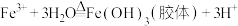 |
您最近半年使用:0次
8 . 已知:常温下可发生反应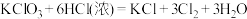 。利用如下图装置进行Cl2的制备及其化学性质的探究。下列说法正确的是
。利用如下图装置进行Cl2的制备及其化学性质的探究。下列说法正确的是
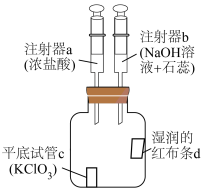
 。利用如下图装置进行Cl2的制备及其化学性质的探究。下列说法正确的是
。利用如下图装置进行Cl2的制备及其化学性质的探究。下列说法正确的是
A.c中产生 后,d褪色的原因是次氯酸具有漂白性 后,d褪色的原因是次氯酸具有漂白性 |
B.性质实验结束后,加入b中溶液除去多余的 溶液由蓝色变为紫色 溶液由蓝色变为紫色 |
| C.拉动a或b的活塞,可检查装置气密性 |
| D.c中反应的氧化剂与还原剂的物质的量比为1:6 |
您最近半年使用:0次
9 . 以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的步骤如下:
步骤1:将电石渣与水混合,形成浆料。
步骤2:控制电石渣过量,75℃时向浆料中通入Cl2,该过程生成Ca(ClO)2,Ca(ClO)2进一步转化为Ca(ClO3)2,少量Ca(ClO)2分解为CaCl2和O2。氯化过程中Cl2转化为Ca(ClO3)2的总反应方程式为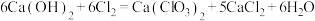 。充分反应后过滤。
。充分反应后过滤。
步骤3:向滤液中加入稍过量KCl固体,蒸发浓缩、冷却至25℃结晶,得KClO3。
下列说法正确的是
步骤1:将电石渣与水混合,形成浆料。
步骤2:控制电石渣过量,75℃时向浆料中通入Cl2,该过程生成Ca(ClO)2,Ca(ClO)2进一步转化为Ca(ClO3)2,少量Ca(ClO)2分解为CaCl2和O2。氯化过程中Cl2转化为Ca(ClO3)2的总反应方程式为
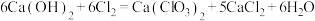 。充分反应后过滤。
。充分反应后过滤。步骤3:向滤液中加入稍过量KCl固体,蒸发浓缩、冷却至25℃结晶,得KClO3。
下列说法正确的是
A.控制通入 的速率,可以提高 的速率,可以提高 的利用率 的利用率 |
B.25℃时, 的溶解度比 的溶解度比 的溶解度大 的溶解度大 |
C.步骤2中,过滤所得滤液中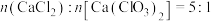 |
D.生成 的化学方程式为 的化学方程式为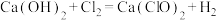 |
您最近半年使用:0次
2023-12-24更新
|
105次组卷
|
2卷引用:江苏省徐州市沛县四校联考2023-2024学年高一上学期12月月考化学试题
名校
10 . 下列离子方程式正确的是
A.氧化亚铁溶于浓盐酸中: |
B.氯气通入石灰乳制漂白粉: |
C.氢氧化铁溶于氢碘酸中: |
D. 与 与 溶液反应至溶液呈中性: 溶液反应至溶液呈中性: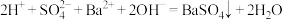 |
您最近半年使用:0次



