解题方法
1 . 84消毒液是常用消毒剂,主要成分为 ,某化学小组在实验室制备84消毒液并探究其相关性质。回答下列问题:
,某化学小组在实验室制备84消毒液并探究其相关性质。回答下列问题:
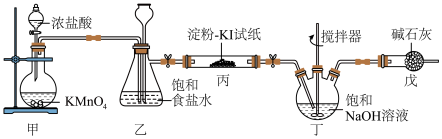
(1)装置甲中盛放浓盐酸的仪器名称是_______ 。
(2)配平方程式:_______ 。
_______MnO +_______Cl-+ _______= _______Mn2++_______Cl2↑+_______
+_______Cl-+ _______= _______Mn2++_______Cl2↑+_______
(3)装置丙中现象_______ 所发生反应的化学方程_______ 。
(4)装置丁制备 的反应中,氧化产物和还原产物的物质的量之比为1∶1,若要制取
的反应中,氧化产物和还原产物的物质的量之比为1∶1,若要制取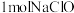 ,理论上反应中转移电子数为
,理论上反应中转移电子数为___ 。
(5)装置戊的作用是_______ 装置乙饱和食盐水作用_______ 。
 ,某化学小组在实验室制备84消毒液并探究其相关性质。回答下列问题:
,某化学小组在实验室制备84消毒液并探究其相关性质。回答下列问题:
(1)装置甲中盛放浓盐酸的仪器名称是
(2)配平方程式:
_______MnO
 +_______Cl-+ _______= _______Mn2++_______Cl2↑+_______
+_______Cl-+ _______= _______Mn2++_______Cl2↑+_______(3)装置丙中现象
(4)装置丁制备
 的反应中,氧化产物和还原产物的物质的量之比为1∶1,若要制取
的反应中,氧化产物和还原产物的物质的量之比为1∶1,若要制取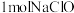 ,理论上反应中转移电子数为
,理论上反应中转移电子数为(5)装置戊的作用是
您最近半年使用:0次
解题方法
2 . 下列反应的离子方程式正确的是
A.氯气尾气处理的原理: |
B.少量 通入 通入 溶液中: 溶液中: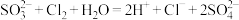 |
C.向红色 溶液中加入过量铁粉至溶液红色褪去: 溶液中加入过量铁粉至溶液红色褪去: |
| D.向含氯化亚铁的氯化铁溶液中通入适量氯气除杂质Fe2+:2Fe2++Cl2=2Fe3++2Clˉ |
您最近半年使用:0次
3 . 氯气是一种重要的化工原料,可用于生产塑料、合成纤维和染料等。实验室某实验小组现用下图装置来制取氯气并对氯气的某些性质和用途进行探究(K为开关,夹持装置已省略)。请回答下列问题:
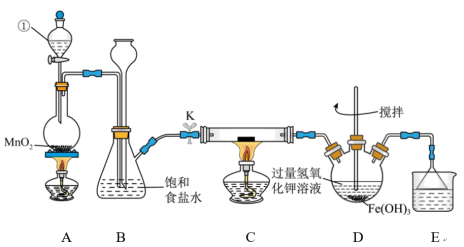
(1)仪器①的名称为__________ 。
(2)检验装置A、B的气密性:将仪器①的活塞和开关K关闭,从长颈漏斗处加水至液面高于锥形瓶中的液面,若________ ,则说明装置气密性良好。
(3)装置A中发生反应的化学方程式为__________ 。
(4)装置E中的试剂是___________ ,作用是___________ 。
(5)装置C中为湿润的KI-淀粉试纸,通入 后试纸变蓝,则该反应的离子方程式为
后试纸变蓝,则该反应的离子方程式为_________ ;该小组为了研究干燥的氯气与金属钠之间的反应,欲在装置C中直接放置一块纯净的金属钠进行实验,该方案存在不妥之处,请你指出不妥之处并改正:__________ 。

(1)仪器①的名称为
(2)检验装置A、B的气密性:将仪器①的活塞和开关K关闭,从长颈漏斗处加水至液面高于锥形瓶中的液面,若
(3)装置A中发生反应的化学方程式为
(4)装置E中的试剂是
(5)装置C中为湿润的KI-淀粉试纸,通入
 后试纸变蓝,则该反应的离子方程式为
后试纸变蓝,则该反应的离子方程式为
您最近半年使用:0次
名校
4 . 回答下列问题
(1)过氧化钠与二氧化碳反应的化学方程式_____________ ,并用单线桥标出电子转移的方向和数目__________________ 。
(2)漂白粉的有效成分是______ (填化学式),制取漂白粉的化学方程式__________________ 。
(3)漂白粉长时间暴露在空气中就会失去效用,失效原因是(写出2个化学方程式)__________________ ;__________________ 。
(4)实验室用 制氯气的离子方程式
制氯气的离子方程式_______________ 。
(5)将钠投入到 溶液中,写出化学方程式
溶液中,写出化学方程式______________ 。
(6)除去碳酸钠中混有的碳酸氢钠应加入______ (填化学式)溶液,涉及到的反应的离子方程式为__________________ 。
(7)厨房里常用小苏打做糕点的发泡剂,写出其受热分解的化学方程式_________________ 。
(1)过氧化钠与二氧化碳反应的化学方程式
(2)漂白粉的有效成分是
(3)漂白粉长时间暴露在空气中就会失去效用,失效原因是(写出2个化学方程式)
(4)实验室用
 制氯气的离子方程式
制氯气的离子方程式(5)将钠投入到
 溶液中,写出化学方程式
溶液中,写出化学方程式(6)除去碳酸钠中混有的碳酸氢钠应加入
(7)厨房里常用小苏打做糕点的发泡剂,写出其受热分解的化学方程式
您最近半年使用:0次
解题方法
5 . 次氯酸钠是家用消毒剂的有效成分。实验室制备次氯酸钠的装置如图所示。
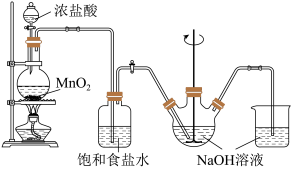
(1)在圆底烧瓶里加入二氧化锰后,通过___________ (填仪器名称)向烧瓶中加入适量的浓盐酸并加热。发生反应的离子方程式为___________ 。
(2)实验室还可用高锰酸钾快速地制取氯气,反应的化学方程式如下:
 。
。
①用双线桥标出该反应中电子转移的方向和数目___________ 。
②若产生标准状况下4.48L ,则反应过程中被氧化的HCl的物质的量是
,则反应过程中被氧化的HCl的物质的量是___________ mol,转移电子的物质的量为___________ mol。
(3)曾有报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分是稀盐酸)与消毒液(主要成分是NaClO)而发生氯气中毒事件。请从氧化还原反应的角度分析原因:___________ 。

(1)在圆底烧瓶里加入二氧化锰后,通过
(2)实验室还可用高锰酸钾快速地制取氯气,反应的化学方程式如下:
 。
。①用双线桥标出该反应中电子转移的方向和数目
②若产生标准状况下4.48L
 ,则反应过程中被氧化的HCl的物质的量是
,则反应过程中被氧化的HCl的物质的量是(3)曾有报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分是稀盐酸)与消毒液(主要成分是NaClO)而发生氯气中毒事件。请从氧化还原反应的角度分析原因:
您最近半年使用:0次
6 . 实验室常用二氧化锰和浓盐酸共热的方法制取氯气。根据要求回答下列问题。
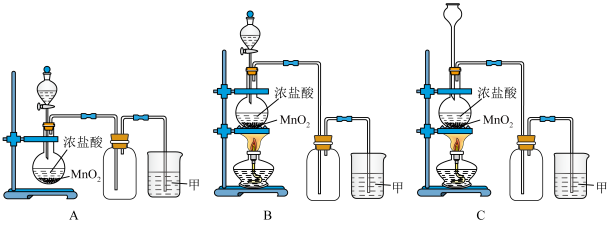
(1)A、B、C三套装置中,应选用的装置是___________ (选填“A”、“B”、“C”)。
(2)写出制取氯气的化学方程式___________ 。
(3)为了防止氯气污染环境,图中溶液甲中发生的化学反应方程式___________ 。
(4)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,在空气中漂白粉长期存放会变质而失效的原理是___________ (用化学方程式说明)
(5)实验室也可用 固体和浓盐酸反应制取氯气,反应方程式:
固体和浓盐酸反应制取氯气,反应方程式: 。请用双线桥标出电子转移的方向和数目:
。请用双线桥标出电子转移的方向和数目:___________ 。若反应中有5mol电子转移,被氧化HCl的的物质的量为___________ 。

(1)A、B、C三套装置中,应选用的装置是
(2)写出制取氯气的化学方程式
(3)为了防止氯气污染环境,图中溶液甲中发生的化学反应方程式
(4)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,在空气中漂白粉长期存放会变质而失效的原理是
(5)实验室也可用
 固体和浓盐酸反应制取氯气,反应方程式:
固体和浓盐酸反应制取氯气,反应方程式: 。请用双线桥标出电子转移的方向和数目:
。请用双线桥标出电子转移的方向和数目:
您最近半年使用:0次
解题方法
7 . 氯气是一种重要的化工原料,大量用于制造盐酸、漂白剂、农药、染料和药品等。
(1)1774年,瑞典化学家舍勒将浓盐酸与软锰矿(主要成分为 )混合加热,发现了氯气。下图为实验室制取Cl2的装置,请回答:
)混合加热,发现了氯气。下图为实验室制取Cl2的装置,请回答:
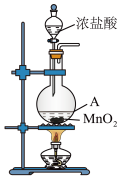
盛放浓盐酸的仪器名称是_______ 。
(2)下图所示制取氯气的净化、收集、尾气处理的装置能达到实验目的的是_______ 。(填序号)
(3)已知:常温下用 和市售浓盐酸(11.9
和市售浓盐酸(11.9 )反应制取Cl2难以进行。但若用漂白粉(有效成分
)反应制取Cl2难以进行。但若用漂白粉(有效成分 )、高锰酸钾等与浓盐酸反应,常温下很容易制取Cl2。
)、高锰酸钾等与浓盐酸反应,常温下很容易制取Cl2。
①已知,如图装置A是氯气的发生装置。加入适量的浓盐酸充分反应有黄绿色气体生成,写出发生反应的化学方程式,并用单线桥标明电子转移的方向和数目 :_______ 。

②装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅲ处应放入的是_______ (填序号)。
a.干燥的有色布条 b.湿润的有色布条 c.湿润的淀粉 试纸
试纸
装置C的Ⅱ处的试剂是_______ (填序号)。
a.碱石灰(氢氧化钠和氧化钙的固体混合物) b.无水氯化钙 c.浓硫酸
③装置D中一般不用 澄清石灰水吸收多余的氯气。理由是_______ 。
(4)84消毒液是一种常见的含氯消毒剂,其有效成分为次氯酸钠。
资料:84消毒液中含氯微粒主要有 、
、 、
、 ;相同浓度时,
;相同浓度时, 的氧化性强于
的氧化性强于 ;
; 是反映水溶液中所有物质表现出来的氧化—还原性,
是反映水溶液中所有物质表现出来的氧化—还原性, 值越大,氧化性越强。
值越大,氧化性越强。
某兴趣小组同学研究84消毒液的漂白性,实验如下。
I.向2 84消毒液中加入2
84消毒液中加入2 水后,放入红色纸片,观察到纸片慢慢褪色。
水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.向2 84消毒液中加入2
84消毒液中加入2 白醋后,放入红色纸片,观察到纸片迅速褪色。
白醋后,放入红色纸片,观察到纸片迅速褪色。
Ⅲ.测得84消毒液在不同温度时 随时间的变化曲线如
随时间的变化曲线如图 。
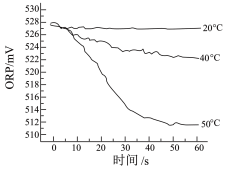
①已知白醋显酸性,不具有漂白性。实验I、Ⅱ现象不同的原因是_______ 。
②由实验Ⅲ可得出的结论是_______ 。
(1)1774年,瑞典化学家舍勒将浓盐酸与软锰矿(主要成分为
 )混合加热,发现了氯气。下图为实验室制取Cl2的装置,请回答:
)混合加热,发现了氯气。下图为实验室制取Cl2的装置,请回答:
盛放浓盐酸的仪器名称是
(2)下图所示制取氯气的净化、收集、尾气处理的装置能达到实验目的的是
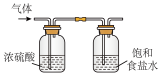 | 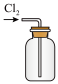 |  |
| A.净化Cl2 | B.收集Cl2 | C.尾气处理 |
(3)已知:常温下用
 和市售浓盐酸(11.9
和市售浓盐酸(11.9 )反应制取Cl2难以进行。但若用漂白粉(有效成分
)反应制取Cl2难以进行。但若用漂白粉(有效成分 )、高锰酸钾等与浓盐酸反应,常温下很容易制取Cl2。
)、高锰酸钾等与浓盐酸反应,常温下很容易制取Cl2。①已知,如图装置A是氯气的发生装置。加入适量的浓盐酸充分反应有黄绿色气体生成,写出发生反应的化学方程式,并用

②装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅲ处应放入的是
a.干燥的有色布条 b.湿润的有色布条 c.湿润的淀粉
 试纸
试纸装置C的Ⅱ处的试剂是
a.碱石灰(氢氧化钠和氧化钙的固体混合物) b.无水氯化钙 c.浓硫酸
③装置D中一般
(4)84消毒液是一种常见的含氯消毒剂,其有效成分为次氯酸钠。
资料:84消毒液中含氯微粒主要有
 、
、 、
、 ;相同浓度时,
;相同浓度时, 的氧化性强于
的氧化性强于 ;
; 是反映水溶液中所有物质表现出来的氧化—还原性,
是反映水溶液中所有物质表现出来的氧化—还原性, 值越大,氧化性越强。
值越大,氧化性越强。某兴趣小组同学研究84消毒液的漂白性,实验如下。
I.向2
 84消毒液中加入2
84消毒液中加入2 水后,放入红色纸片,观察到纸片慢慢褪色。
水后,放入红色纸片,观察到纸片慢慢褪色。Ⅱ.向2
 84消毒液中加入2
84消毒液中加入2 白醋后,放入红色纸片,观察到纸片迅速褪色。
白醋后,放入红色纸片,观察到纸片迅速褪色。Ⅲ.测得84消毒液在不同温度时
 随时间的变化曲线如
随时间的变化曲线如
①已知白醋显酸性,不具有漂白性。实验I、Ⅱ现象不同的原因是
②由实验Ⅲ可得出的结论是
您最近半年使用:0次
8 . 如图为实验室制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条 ,F中为红色的铜网 ,其右端出气管口放有脱脂棉。
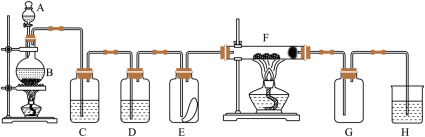
(1)仪器A的名称是_______ ,烧瓶中反应的化学方程式是_______ 。
(2)装置C中的物质是_______ 。装置D的作用是_______ 。
(3)E中红色布条是否褪色(填“是”或“否”)_______ ,F中反应的化学方程式为_______ 。
(4)H处溶液为NaOH溶液,其作用是_______ 。试写出H处所发生反应的离子反应方程式_______ 。

(1)仪器A的名称是
(2)装置C中的物质是
(3)E中红色布条是否褪色(填“是”或“否”)
(4)H处溶液为NaOH溶液,其作用是
您最近半年使用:0次
9 . 某同学在培养皿上做如下实验(如图所示),a、b、c、d是浸有相关溶液的滤纸。向 晶体上滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
晶体上滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
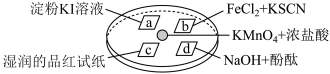
下列对实验现象的“解释或结论”描述,不正确的是
 晶体上滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
晶体上滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
下列对实验现象的“解释或结论”描述,不正确的是
选项 | 实验现象 | 解释或结论 |
A | a处试纸变蓝 | 还原性: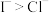 |
B | b处试纸变红 |  |
C | c处试纸褪色 |  与 与 反应生成了具有漂白性的物质 反应生成了具有漂白性的物质 |
D | d处红色褪去 |  和 和 反应使溶液呈中性 反应使溶液呈中性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
10 . 下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | 牙膏中常加入含氟物质预防龋齿 | 氟磷灰石的溶解度小于羟基磷灰石 |
B | 气态氢化物稳定性: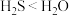 | 分子间作用力: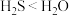 |
C | 电解食盐水制备氯气和氢氧化钠 | 氯气和氢氧化钠溶液反应制备漂白液 |
D | 饱和 溶液导电性比饱和 溶液导电性比饱和 溶液强 溶液强 |  溶液碱性强于 溶液碱性强于 溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



