1 . 二氧化氯 是一种高效消毒灭菌剂。但稳定性较差,可将其用吸收法和电解法两种方法得到较稳定的
是一种高效消毒灭菌剂。但稳定性较差,可将其用吸收法和电解法两种方法得到较稳定的 加以保存。其工艺流程示意图如下图所示:
加以保存。其工艺流程示意图如下图所示:
ⅰ.纯 易分解爆炸,一般用稀有气体或空气稀释到
易分解爆炸,一般用稀有气体或空气稀释到 以下。
以下。
ⅱ.长期放置或高于 时
时 易分解生成
易分解生成 和
和 。
。
(1)步骤1中,生成 的离子方程式是
的离子方程式是_______ ,通入空气的作用是_______ 。
(2)方法1中,反应的离子方程式是_______ ,利用方法1制 时,温度不能超过
时,温度不能超过 ,可能的原因是
,可能的原因是_______ 。
(3)方法2中,利用下图所示装置制备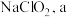 电极(左侧电极)处发生的电极反应式为
电极(左侧电极)处发生的电极反应式为______ ,b电极(右侧电极)处发生的电极反应式为_____ 。溶液中的溶质浓度:f处____ d处(填“>”、“<”或“=”)。 的溶解度曲线如下图所示,步骤3中从
的溶解度曲线如下图所示,步骤3中从 溶液中获得
溶液中获得 的操作是
的操作是_______ 。 使用时,加入稀盐酸即可迅速得到
使用时,加入稀盐酸即可迅速得到 ,写出反应的离子方程式:
,写出反应的离子方程式:_______ 。若加入盐酸浓度过大,则气体产物中 含量会增大,原因是
含量会增大,原因是_______ 。
 是一种高效消毒灭菌剂。但稳定性较差,可将其用吸收法和电解法两种方法得到较稳定的
是一种高效消毒灭菌剂。但稳定性较差,可将其用吸收法和电解法两种方法得到较稳定的 加以保存。其工艺流程示意图如下图所示:
加以保存。其工艺流程示意图如下图所示:
ⅰ.纯
 易分解爆炸,一般用稀有气体或空气稀释到
易分解爆炸,一般用稀有气体或空气稀释到 以下。
以下。ⅱ.长期放置或高于
 时
时 易分解生成
易分解生成 和
和 。
。(1)步骤1中,生成
 的离子方程式是
的离子方程式是(2)方法1中,反应的离子方程式是
 时,温度不能超过
时,温度不能超过 ,可能的原因是
,可能的原因是(3)方法2中,利用下图所示装置制备
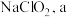 电极(左侧电极)处发生的电极反应式为
电极(左侧电极)处发生的电极反应式为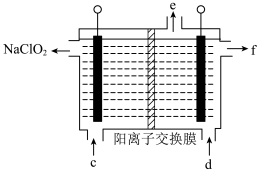
 的溶解度曲线如下图所示,步骤3中从
的溶解度曲线如下图所示,步骤3中从 溶液中获得
溶液中获得 的操作是
的操作是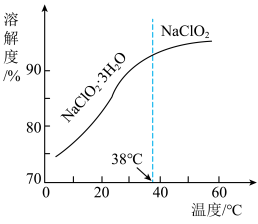
 使用时,加入稀盐酸即可迅速得到
使用时,加入稀盐酸即可迅速得到 ,写出反应的离子方程式:
,写出反应的离子方程式: 含量会增大,原因是
含量会增大,原因是
您最近一年使用:0次
2 . 下列三个化学反应焓变、平衡常数与温度的关系分别如下表所示。下列说法正确的是
| 化学反应 | 平衡常数 | 温度 | |
 | 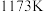 | ||
①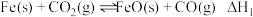 |  | 1.47 | 2.15 |
②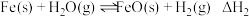 |  | 2.38 | 1.67 |
③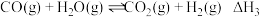 |  | a | b |
| A.反应②是吸热反应 |
| B.反应③达平衡后,升高温度平衡正向移动 |
C.相同温度下,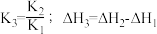 |
D.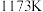 时,若反应①起始 时,若反应①起始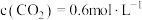 ,平衡时 ,平衡时 约为 约为 |
您最近一年使用:0次
解题方法
3 . 用过量铁片与稀硫酸反应制备氢气,下列方法能增大反应速率而不影响氢气生成量的是
| A.稀硫酸改为浓硫酸 | B.加入 固体 固体 |
C.滴加少量 溶液 溶液 | D.加入 固体 固体 |
您最近一年使用:0次
解题方法
4 . 对下列事实的解释不正确 的是
| 选项 | 事实 | 解释 |
| A | 稳定性: | H-F键键能大于H-I键键能。 |
| B | 键角: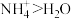 | 中心原子均采取 杂化,孤电子对有较大的斥力 杂化,孤电子对有较大的斥力 |
| C | 熔点:石英>干冰 | 石英是共价晶体,干冰是分子晶体;共价键比分子间作用力强 |
| D | 金属活动性: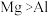 | 第一电离能: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
5 . 下列解释事实的化学用语不正确 的是
A. 溶液遇闪锌矿 溶液遇闪锌矿 生成铜蓝 生成铜蓝 |
B.铜与浓硝酸反应有红棕色气体生成: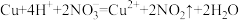 |
C.用过量氨水吸收烟气中的少量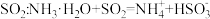 |
D.84消毒液不能与洁厕灵混用: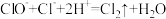 |
您最近一年使用:0次
解题方法
6 . 下列化学用语或图示表达不正确 的是
A. 的VSEPR模型: 的VSEPR模型: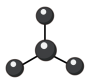 |
B.反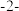 丁烯的分子结构模型: 丁烯的分子结构模型: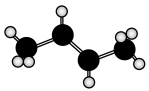 |
C.丙酮的结构简式: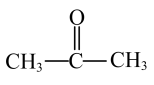 |
D.乙烯分子中的 键: 键: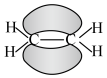 |
您最近一年使用:0次
7 . 生活中的一些现象常常涉及化学知识。下列分析中不正确 的是
| A.咀嚼米饭时,越嚼越甜,因为淀粉水解生成了麦芽糖 |
| B.向食盐浓溶液中加入鸡蛋清溶液,有白色沉淀析出,因为食盐能使蛋白质变性 |
| C.铁锅用水清洗后,出现铁锈,因为潮湿环境中铁锅会发生电化学腐蚀 |
| D.过氧化钠可用作漂白剂,是因为其具有强氧化性 |
您最近一年使用:0次
8 . 下列化学用语不正确 的是
A.氮分子的电子式:  |
B.基态 原子的价电子轨道表示式: 原子的价电子轨道表示式: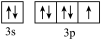 |
C.基态 的价电子排布式: 的价电子排布式: |
D. 分子的空间结构模型: 分子的空间结构模型: |
您最近一年使用:0次
9 . 氮化硼晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如图所示。
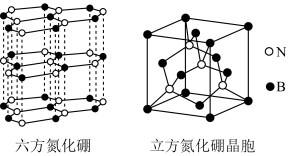
| A.六方氮化硼与立方氮化硼互为同素异形体 |
B.立方相氮化硼含有 键和 键和 键,所以硬度大 键,所以硬度大 |
C.六方、立方相氮化硼晶体的化学式均为BN,硼原子的杂化类型分别为 、 、 |
| D.两种晶体中既有极性键又有非极性键 |
您最近一年使用:0次
10 . 氧化还原反应可拆分为氧化和还原两个“半反应”,某小组同学从“半反应”的角度探究反应规律。
(1)已知: 的转化在酸性条件下才能发生。
的转化在酸性条件下才能发生。
①该转化的还原半反应是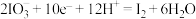 ,则相应的氧化半反应是
,则相应的氧化半反应是___________ 。
②分析上述还原半反应可知:增大 可促进
可促进 得到电子,使其
得到电子,使其___________ 性增强,进而与 发生反应。
发生反应。
(2)探究 与浓盐酸能否发生反应。
与浓盐酸能否发生反应。
①有同学认为 与浓盐酸不能发生反应产生氢气,其依据是
与浓盐酸不能发生反应产生氢气,其依据是___________ 。
用如下装置进行实验【硫酸与浓盐酸中 接近】。
接近】。
②甲实验的目的是___________ 。
③a.丙中气球变鼓是因为生成了___________ 气体(填化学式)。
b.经检测,丙中反应后溶液中存在 。从物质性质角度分析丙中反应能够发生的原因:
。从物质性质角度分析丙中反应能够发生的原因:___________ 。
(3)探究以下原电池的工作原理。
实验结果:产生电流,左侧 电极表面有
电极表面有 析出。
析出。
①该装置中左侧  电极作
电极作___________ (填“正”或“负”)极。
②写出该装置右侧 烧杯中的电极反应式___________ 。
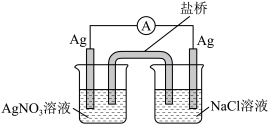
对该原电池的电极反应和总反应的反应类型进行分析,发现两极上分别发生氧化和还原反应,而总反应不一定是氧化还原反应。
③结合上述实验思考,仅由以下实验用品能否设计成原电池__________ 。
 片、
片、 浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
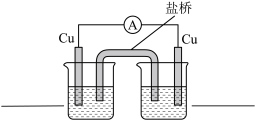
a.若能,在右装置图中填写烧杯中的试剂,并标出电子的移动方向 。
b.若不能,说明原因。
(1)已知:
 的转化在酸性条件下才能发生。
的转化在酸性条件下才能发生。①该转化的还原半反应是
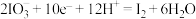 ,则相应的氧化半反应是
,则相应的氧化半反应是②分析上述还原半反应可知:增大
 可促进
可促进 得到电子,使其
得到电子,使其 发生反应。
发生反应。(2)探究
 与浓盐酸能否发生反应。
与浓盐酸能否发生反应。①有同学认为
 与浓盐酸不能发生反应产生氢气,其依据是
与浓盐酸不能发生反应产生氢气,其依据是用如下装置进行实验【硫酸与浓盐酸中
 接近】。
接近】。| 装置 | 序号 | 试管内药品 | 现象 |
 | 甲 | 浓盐酸 | 24小时后仍无明显变化 |
| 乙 |  粉+硫酸 粉+硫酸 | 24小时后仍无明显变化 | |
| 丙 |  粉+浓盐酸 粉+浓盐酸 | 24小时后气球变鼓 |
③a.丙中气球变鼓是因为生成了
b.经检测,丙中反应后溶液中存在
 。从物质性质角度分析丙中反应能够发生的原因:
。从物质性质角度分析丙中反应能够发生的原因:(3)探究以下原电池的工作原理。
实验结果:产生电流,左侧
 电极表面有
电极表面有 析出。
析出。①该装置中
 电极作
电极作②写出该装置

对该原电池的电极反应和总反应的反应类型进行分析,发现两极上分别发生氧化和还原反应,而总反应不一定是氧化还原反应。
③结合上述实验思考,仅由以下实验用品能否设计成原电池
 片、
片、 浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
a.若能,在右装置图中填写烧杯中的试剂,
b.若不能,说明原因。
您最近一年使用:0次



