1 . 将 通入含amolNaOH的溶液中,反应会放热,温度升高后发生反应:
通入含amolNaOH的溶液中,反应会放热,温度升高后发生反应: 。当
。当 完全反应时,下列说法正确的是
完全反应时,下列说法正确的是
 通入含amolNaOH的溶液中,反应会放热,温度升高后发生反应:
通入含amolNaOH的溶液中,反应会放热,温度升高后发生反应: 。当
。当 完全反应时,下列说法正确的是
完全反应时,下列说法正确的是A.反应中作氧化剂的 有 有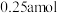 |
B.若反应后溶液中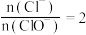 ,则 ,则 |
C. 与 与 的物质的量之和可能为 的物质的量之和可能为 |
D.反应中转移电子的物质的量可能为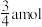 |
您最近一年使用:0次
名校
解题方法
2 . 下图是实验室制备氯气并进行一系列相关实验的装置(夹持仪器已略,无加热仪器)。

(1)实验室利用 装置制备氯气的离子方程式为
装置制备氯气的离子方程式为_______ 。
(2)装置B中饱和食盐水的作用是_______ ,装置B还起到_______ 作用。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放湿润的有色布条、_______ 、_______ 。(填写名称)
(4)设计装置D、E的目的是比较氯、溴、碘三种单质的氧化性的相对强弱。当向D中缓缓通入氯气,控制氯气的通入量,当分液漏斗中的溶液显橙黄色时,关闭A中分液漏斗,停止通氯气,打开E中分液漏斗,_______ 。(写出验证溴强于碘的剩余操作及现象)
(5)你认为在实验中装置F中可以使用的试剂为_______(填字母)。
(6)已知有效氯含量的实质就是指单位质量的含氯化合物中所含氯的氧化能力相当于多少纯净氯气的氧化能力。氯气的有效氯为 ,二氧化氯气体能代替氯气消毒自来水,则
,二氧化氯气体能代替氯气消毒自来水,则 的有效氯是
的有效氯是 的
的_______ 倍。(保留两位小数)

(1)实验室利用
 装置制备氯气的离子方程式为
装置制备氯气的离子方程式为(2)装置B中饱和食盐水的作用是
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放湿润的有色布条、
(4)设计装置D、E的目的是比较氯、溴、碘三种单质的氧化性的相对强弱。当向D中缓缓通入氯气,控制氯气的通入量,当分液漏斗中的溶液显橙黄色时,关闭A中分液漏斗,停止通氯气,打开E中分液漏斗,
(5)你认为在实验中装置F中可以使用的试剂为_______(填字母)。
| A.氢氧化钠溶液 | B.澄清石灰水 | C.硫酸钠溶液 | D.氯化亚铁溶液 |
 ,二氧化氯气体能代替氯气消毒自来水,则
,二氧化氯气体能代替氯气消毒自来水,则 的有效氯是
的有效氯是 的
的
您最近一年使用:0次
2023-01-19更新
|
231次组卷
|
2卷引用:河南省信阳高级中学2022-2023学年高一上学期期末考试化学试题
名校
解题方法
3 . NA为阿伏加德罗常数的值。下列说法错误的是
A.1mol 与足量水反应,转移电子数为NA 与足量水反应,转移电子数为NA |
B.1mol 溶于足量NaOH溶液中,转移电子数为NA 溶于足量NaOH溶液中,转移电子数为NA |
C.足量Fe与1mol 充分反应,转移的电子数为2NA 充分反应,转移的电子数为2NA |
| D.1molAl与含2molHCl的盐酸充分反应,转移电子数为3NA |
您最近一年使用:0次
2022-02-18更新
|
108次组卷
|
2卷引用:河南省潢川第一中学2022-2023学年高一上学期期末考试化学试题
解题方法
4 . 下列物质应用中,对应的离子反应方程式书写错误的是
| A.将溴水加入KI溶液:Br2+2I—=2Br—+I2 |
| B.用盐酸溶解磁性氧化铁:Fe3O4+8H+=3Fe3++4H2O |
| C.用NaOH溶液吸收多余的氯气:2OH—+Cl2=Cl—+ClO—+H2O |
D.用可溶性强碱溶液除去铝表面的氧化膜:Al2O3+2OH—=2 +H2O +H2O |
您最近一年使用:0次
2022-01-24更新
|
132次组卷
|
2卷引用:河南省信阳市华中师大息县附中2022-2023学年高一下学期开学考试化学试题



