名校
解题方法
1 . 氮及其化合物在生产生活中有着广泛的应用,但同时随意排放氮的化合物也会造成环境污染问题。
I.某研究性学习小组设计用如图所示实验装置(夹持仪器省略)制取干燥的氨气并验证NH3具有还原性,请回答下列问题:

(1)实验室制备氨气有多种方法,现欲NH4Cl用与熟石灰反应制取NH3,则甲中的气体发生装置为______ 。(从Ⅱ中选用)
(2)装置丙用于收集NH3,应将导管_____ (填“a”或“b”)延长至集气瓶底部。
Ⅱ.由氨气为原料的合成硝酸工业中有含NO、NO2等氮氧化物的尾气排出,有多种方法解决污染环境。
(3)臭氧脱硝法:O3氧化NO结合水洗,可产生HNO3,该反应的化学方程式为______ 。
(4)氨气催化吸收法处理尾气法:已知6mol氨气恰好能将含NO和NO2共7mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比______ 。
Ⅲ.NO和NO2等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(5)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应为
NO+NO2+2OH-=2NO +H2O
+H2O
2NO2+2OH-=NO +NO
+NO +H2O
+H2O
①下列措施能提高尾气中NO和NO2去除率的有______ (填字母)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是______ (填化学式);吸收后排放的尾气中含量较高的氮氧化物是______ (填化学式)。
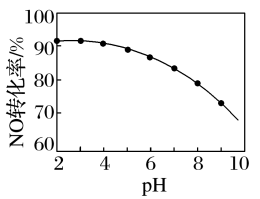
(6)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为NO 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
①在酸性NaClO溶液中,HClO氧化NO生成Cl-和NO ,其离子方程式为
,其离子方程式为______ 。
②NaClO溶液的初始pH越小,NO转化率越高。其原因是______ 。
I.某研究性学习小组设计用如图所示实验装置(夹持仪器省略)制取干燥的氨气并验证NH3具有还原性,请回答下列问题:

(1)实验室制备氨气有多种方法,现欲NH4Cl用与熟石灰反应制取NH3,则甲中的气体发生装置为
(2)装置丙用于收集NH3,应将导管
Ⅱ.由氨气为原料的合成硝酸工业中有含NO、NO2等氮氧化物的尾气排出,有多种方法解决污染环境。
(3)臭氧脱硝法:O3氧化NO结合水洗,可产生HNO3,该反应的化学方程式为
(4)氨气催化吸收法处理尾气法:已知6mol氨气恰好能将含NO和NO2共7mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比
Ⅲ.NO和NO2等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(5)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应为
NO+NO2+2OH-=2NO
 +H2O
+H2O2NO2+2OH-=NO
 +NO
+NO +H2O
+H2O①下列措施能提高尾气中NO和NO2去除率的有
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是
(6)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为NO
 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
①在酸性NaClO溶液中,HClO氧化NO生成Cl-和NO
 ,其离子方程式为
,其离子方程式为②NaClO溶液的初始pH越小,NO转化率越高。其原因是
您最近一年使用:0次
2023-03-09更新
|
606次组卷
|
3卷引用:江西省吉安市井冈山宁冈中学2022-2023学年高一下学期5月期中考试化学试题
2 . 氨气是一种重要的工业原料,可以制备如下图所示的一系列物质(部分产物未标出)

(1)线路Ⅰ为硝酸的制备
写出反应①的化学方程式________ ;反应②中氧化剂与还原剂的物质的量之比为_______ ,工业尾气中的氮氧化物常采用碱液法吸收,若NO与NO2按物质的量之比1:1被足量NaOH溶液完全吸收后只得到一种钠盐,该钠盐的化学式是_______ 。
(2)路线为Ⅱ纯碱的制备
写出反应③的化学方程式________ ,最终得到的纯碱中可能含有NaCl,检验是否存在NaCl的实验方案是________
(3)路线Ⅲ为尿素的制备
写出合成尿素的化学方程式________
(4)实验室中需要少量氨气,写出制备氨气的化学方程式________

(1)线路Ⅰ为硝酸的制备
写出反应①的化学方程式
(2)路线为Ⅱ纯碱的制备
写出反应③的化学方程式
(3)路线Ⅲ为尿素的制备
写出合成尿素的化学方程式
(4)实验室中需要少量氨气,写出制备氨气的化学方程式
您最近一年使用:0次
2019-03-03更新
|
521次组卷
|
6卷引用:广东省广州市第六十五中学2022-2023学年高一下学期期中考试化学试题
广东省广州市第六十五中学2022-2023学年高一下学期期中考试化学试题广东省广州市第六十五中学2022-2023学年高一下学期期中考试化学试题【市级联考】山东省滨州市2018-2019学年高一上学期期末考试化学试题(已下线)第17讲 氨的转化与生成-【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)云南省石屏县第一中学2022-2023学年高一下学期期末考试化学试题云南省泸西县第一中学2022-2023学年高一下学期期末考试化学试题
名校
3 . 工业上硝酸的制备和自然界中硝酸的生成既有相同之处,又有区别。路线①②③是工业生产硝酸的主要途径,路线Ⅰ、Ⅱ、Ⅲ是雷电高能固氮过程中硝酸的生成途径。
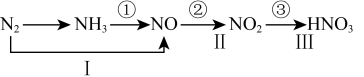
(1)写出N2的一种用途_____________________ 。
(2)工业合成NH3的化学方程式为______________________ 。
(3)写出工业制硝酸第③步反应化学方程式_____________________ 。
(4)硝酸是一种强氧化性、腐蚀性的强酸,其还原产物因硝酸浓度的不同而有变化,从总体上说,硝酸浓度越高,平均每分子硝酸得到的电子数越少,浓硝酸的还原产物主要为NO2,稀硝酸的还原产物主要为NO。 实验室中,常用Cu与浓HNO3反应制取NO2,用Cu与稀HNO3反应制取NO。
(ⅰ)请写出实验室中用Cu与浓HNO3反应制取NO2的化学方程式:____________ 。该反应中发生氧化反应的物质是_______ ,1 mol氧化剂_________ (填“得到”或“失去”)_______ mol电子。
(ⅱ)64.0 g Cu与适量的浓HNO3反应,铜全部溶解后,共收集到标准状况下22.4 L的气体(NO2和NO的混合气体),反应中消耗HNO3的物质的量是( )
(ⅲ)实际上硝酸不仅可被还原为NO2或NO,浓度更稀时硝酸还可以被还原为N2O、N2、NH4NO3等。请将3种物质:FeSO4、Fe(NO3)3和Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式。
HNO3+______ 
______ + ______ + N2O↑ + H2O
并配平其对应的离子方程式:__ Fe2++__ NO3-+__ H+ =__ Fe3++__ N2O↑+__ H2O

(1)写出N2的一种用途
(2)工业合成NH3的化学方程式为
(3)写出工业制硝酸第③步反应化学方程式
(4)硝酸是一种强氧化性、腐蚀性的强酸,其还原产物因硝酸浓度的不同而有变化,从总体上说,硝酸浓度越高,平均每分子硝酸得到的电子数越少,浓硝酸的还原产物主要为NO2,稀硝酸的还原产物主要为NO。 实验室中,常用Cu与浓HNO3反应制取NO2,用Cu与稀HNO3反应制取NO。
(ⅰ)请写出实验室中用Cu与浓HNO3反应制取NO2的化学方程式:
(ⅱ)64.0 g Cu与适量的浓HNO3反应,铜全部溶解后,共收集到标准状况下22.4 L的气体(NO2和NO的混合气体),反应中消耗HNO3的物质的量是
(ⅲ)实际上硝酸不仅可被还原为NO2或NO,浓度更稀时硝酸还可以被还原为N2O、N2、NH4NO3等。请将3种物质:FeSO4、Fe(NO3)3和Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式。
HNO3+

并配平其对应的离子方程式:
您最近一年使用:0次
2016-12-09更新
|
575次组卷
|
2卷引用:2014-2015福建省南安第一中学高一下学期期中考试化学试卷
4 . “价一类”二维图是元素化合物知识结构化的良好工具,如图是氮元素的“价一类”二维图。回答下列问题:

(1)C的化学式为___________ 。
(2)若物质B为 ,其气态呈
,其气态呈___________ 色,不能用排水法收集B气体的原因是___________ 。
(3)物质A的电子式为___________ ;A是重要的化工原料,可以合成C,写出工业上以A为原料制取C的第一步反应的化学方程式:___________ 。
(4)实验室中,检验D溶液中含有 的实验操作和现象是
的实验操作和现象是___________ 。
(5)铜和足量的C的稀溶液反应,反应中C表现的性质为___________(填字母)。

(1)C的化学式为
(2)若物质B为
 ,其气态呈
,其气态呈(3)物质A的电子式为
(4)实验室中,检验D溶液中含有
 的实验操作和现象是
的实验操作和现象是(5)铜和足量的C的稀溶液反应,反应中C表现的性质为___________(填字母)。
| A.只有还原性 | B.还原性和酸性 | C.只有氧化性 | D.氧化性和酸性 |
您最近一年使用:0次
5 . “价—类”二维图是元素化合物知识结构化的良好工具,如图是氮元素的“价—类”二维图。回答下列问题:

(1)N2的电子式为______ 。
(2)若物质B为NO2,实验室制备NO2不能用排水法收集的原因是______ 。
(3)A是重要的化工原料,可以合成C,写出工业上以A为原料制取C的第一步反应的化学方程式:______ 。
(4)实验室中,检验D溶液中含有阳离子的实验操作和现象是______ 。
(5)铜和足量的C的稀溶液反应,当生成11.2L(标准状况)气体时,转移电子的物质的量为______ mol;反应中C表现的性质为______ (填字母)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(6)把盛有48mL由NO和NO2组成的混合气体的容器倒置于水中(保持同温同压),待液面稳定后,容器内气体的体积变为24mL,则原混合气中NO的体积是______ mL。

(1)N2的电子式为
(2)若物质B为NO2,实验室制备NO2不能用排水法收集的原因是
(3)A是重要的化工原料,可以合成C,写出工业上以A为原料制取C的第一步反应的化学方程式:
(4)实验室中,检验D溶液中含有阳离子的实验操作和现象是
(5)铜和足量的C的稀溶液反应,当生成11.2L(标准状况)气体时,转移电子的物质的量为
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(6)把盛有48mL由NO和NO2组成的混合气体的容器倒置于水中(保持同温同压),待液面稳定后,容器内气体的体积变为24mL,则原混合气中NO的体积是
您最近一年使用:0次



