1 . 下图是某元素的价类二维图,G为正盐,通常条件下Z是无色溶液,C的相对分子质量比D大16,各物质转化关系如图所示。下列说法不正确的是

| A.B可能是硫酸,也可能是硝酸 |
| B.F与过量Cl2反应有白烟生成 |
| C.B和F在一定条件下能反应生成盐 |
| D.F在一定条件下可直接与Y反应生成D |
您最近半年使用:0次
名校
解题方法
2 . 在给定条件下,下列选项中所示的物质间转化均能实现的是
A.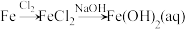 |
B. |
C. |
D.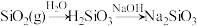 |
您最近半年使用:0次
解题方法
3 . NH3是一种重要的化工产品,也是重要的化工原料。某化学兴趣小组在实验室制备NH3并完成相关性质实验。
Ⅰ.实验室制取NH3通常有两种方法:①选择药品氢氧化钙与氯化铵固体;②选择药品NaOH固体与浓氨水。___________ (填“甲”或“乙”)发生反应的化学方程式为___________ ,检验NH3已收集满的方法是___________ 。
(2)下列能用作NH3尾气吸收装置的是___________ (填序号)。
已知:Cu和Cu2O均为红色固体,Cu2O+2H+=Cu2++Cu+H2O。
①若溶液不变蓝,A中发生的总反应方程式为___________ 。
②若溶液变蓝,证明红色固体中___________ (填“有”或“没有”)Cu2O,经称量反应前A中CuO质量为8g,反应后A中红色固体质量为6.8g,则红色固体中金属铜的质量分数为___________ (精确至1%)。
Ⅰ.实验室制取NH3通常有两种方法:①选择药品氢氧化钙与氯化铵固体;②选择药品NaOH固体与浓氨水。
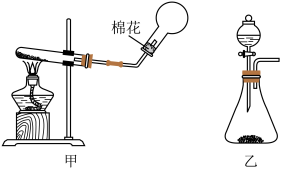
(2)下列能用作NH3尾气吸收装置的是

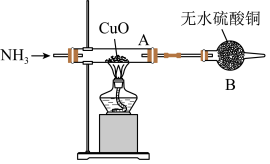
已知:Cu和Cu2O均为红色固体,Cu2O+2H+=Cu2++Cu+H2O。
①若溶液不变蓝,A中发生的总反应方程式为
②若溶液变蓝,证明红色固体中
您最近半年使用:0次
4 . Ⅰ、某校化学研究性学习小组设计实验验证NH3能还原CuO。请回答下列问题:___________ 。
(2)请将提供的装置按合理顺序连接:g→___________ →___________→a→b→___________→___________→___________。
(3)装置B的作用是___________ 。
(4)证明NH3能还原CuO的实验现象是___________ 。
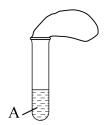
Ⅱ、试管中装有某未知A溶液,装置密闭,操作过程中未见气球中有颜色变化(如下图)
(5)无色A溶液加热后变红,停止加热后溶液又变成无色,则A溶液是___________
(6)红色A溶液加热后变成无色,停止加热后溶液又变红色,则A溶液是___________
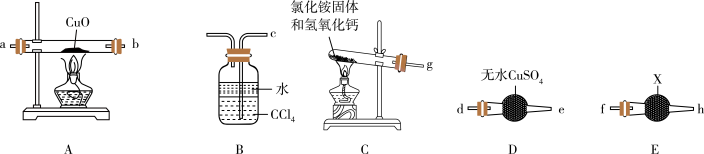
(2)请将提供的装置按合理顺序连接:g→
(3)装置B的作用是
(4)证明NH3能还原CuO的实验现象是
Ⅱ、试管中装有某未知A溶液,装置密闭,操作过程中未见气球中有颜色变化(如下图)
(5)无色A溶液加热后变红,停止加热后溶液又变成无色,则A溶液是
(6)红色A溶液加热后变成无色,停止加热后溶液又变红色,则A溶液是
您最近半年使用:0次
名校
5 . 氨气是重要的含氮元素物质。
I. 工业上氨气是重要的化工产品及制备硝酸的原料。
(1)工业合成氨的化学方程式___________ 。
(2)氨的催化氧化是工业制硝酸的基础,写出化学方程式___________ 。
II.实验室常利用如图所示装置及药品制取干燥的氨气。___________ 。
(4)C处是收集氨气的装置,请将集气瓶中导管补充完整_______ 。
(5)证明氨气已收集满的操作和现象是___________ 。
I. 工业上氨气是重要的化工产品及制备硝酸的原料。
(1)工业合成氨的化学方程式
(2)氨的催化氧化是工业制硝酸的基础,写出化学方程式
II.实验室常利用如图所示装置及药品制取干燥的氨气。
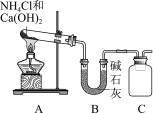
(4)C处是收集氨气的装置,请将集气瓶中导管补充完整
(5)证明氨气已收集满的操作和现象是
您最近半年使用:0次
名校
6 . 氮、硫元素的“价—类”二维图如图所示。下列有关叙述错误的是
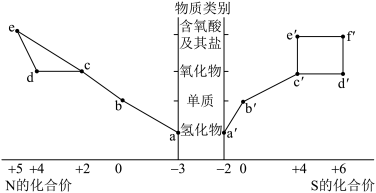
| A.b→a属于氮的固定 |
B.工业上制备 的途径为b'→c'→d'→f 的途径为b'→c'→d'→f |
| C.d或d'均可与水发生反应,生成强酸 |
| D.a'和f的浓溶液反应,产物一定有b'和c' |
您最近半年使用:0次
名校
解题方法
7 . 硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。
(1)用稀硫酸、铜和氧化铁制取硫酸铜,生产的主要过程如下图所示:___________ ;向混合溶液中通入热空气的反应的离子方程式是___________ ;可循环利用的物质是___________ (填化学式)。
(2)氨法脱硫技术可吸收硫酸工业尾气中的二氧化硫,同时制得硫酸铵。主要的工艺流程如下图所示:___________ 。(氨水用“NH3·H2O”表示)
②有数据表明,吸收塔中溶液的pH在5.5﹣6.0之间,生产效率较高。当控制好尾气的流量一定时,调节溶液的pH的方法是___________ 。
(3)氨氮废水的去除是当前科学研究的热点问题。氨氮废水中的氮元素多以 和
和 的形式存在。某工厂处理氨氮废水的流程如图:
的形式存在。某工厂处理氨氮废水的流程如图:
含 的废水
的废水 低浓度氨氮废水
低浓度氨氮废水 含余氯废水
含余氯废水 达标
达标
①过程②加入NaClO溶液可将氨氮物质(以NH3表示)转化为无毒物质,请用离子方程式表示该转化过程___________ 。
②含余氯废水的主要成分是NaClO以及HClO,X可选用以下哪种溶液以达到将余氯转化为无毒物质的目的___________ (填字母)。
a.KOH b.Na2SO3 c.KMnO4 d.Na2S
(1)用稀硫酸、铜和氧化铁制取硫酸铜,生产的主要过程如下图所示:
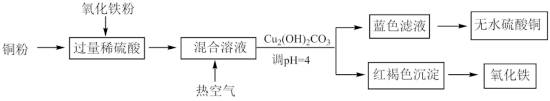
(2)氨法脱硫技术可吸收硫酸工业尾气中的二氧化硫,同时制得硫酸铵。主要的工艺流程如下图所示:

②有数据表明,吸收塔中溶液的pH在5.5﹣6.0之间,生产效率较高。当控制好尾气的流量一定时,调节溶液的pH的方法是
(3)氨氮废水的去除是当前科学研究的热点问题。氨氮废水中的氮元素多以
 和
和 的形式存在。某工厂处理氨氮废水的流程如图:
的形式存在。某工厂处理氨氮废水的流程如图:含
 的废水
的废水 低浓度氨氮废水
低浓度氨氮废水 含余氯废水
含余氯废水 达标
达标①过程②加入NaClO溶液可将氨氮物质(以NH3表示)转化为无毒物质,请用离子方程式表示该转化过程
②含余氯废水的主要成分是NaClO以及HClO,X可选用以下哪种溶液以达到将余氯转化为无毒物质的目的
a.KOH b.Na2SO3 c.KMnO4 d.Na2S
您最近半年使用:0次
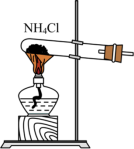
8 . NH3易液化,能与多种物质发生反应。将金属钠投入液氨中有H2产生,NH3可与酸反应制得铵盐,可通过催化氧化生产HNO3,下列说法正确的是
| A.因为液NH3具有碱性,所以可用作制冷剂 |
| B.工业上通过NH3催化氧化等反应过程生产HNO3是人工固氮的过程 |
| C.金属钠与液氨反应体现了NH3的氧化性 |
| D.实验室可以用右图装置与药品制备NH3 |
您最近半年使用:0次
名校
解题方法
9 . 现有氮及其化合物的转化关系如下图,则下列说法不正确的是
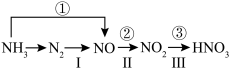
| A.上述所有反应都是氧化还原反应 |
| B.“一场雷雨,一场肥”路线Ⅰ、Ⅱ、Ⅲ是模拟雷电固氮的过程 |
| C.反应①中每生成1 mol NO,转移4 mol 电子 |
| D.S元素也能发生类似的转化,最终得到硫酸 |
您最近半年使用:0次
10 . 依据下图中氮元素及其化合物的转化关系,回答下列问题:_______ 。
(2)若要收集一瓶氨,请将下列装置补充完整,在虚框内画出连接图_______ 。_______ 。
A.浓硫酸 B.碱石灰 C.NaOH固体
(4)工业上以NH3、空气、水为原料生产硝酸分为三步:
①NH3→NO:化学方程式为_______ 。
②NO→NO2:实验现象是_______ 。
③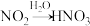 :氧化剂与还原剂的物质的量之比为
:氧化剂与还原剂的物质的量之比为_______ 。
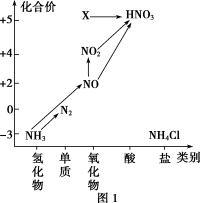
(5)图1中,只用一种物质将NO直接转化为硝酸且绿色环保,则该物质的化学式为_______ 。
(6)图1中,X的化学式为_______ ,从物质性质上看,X属于_______ 氧化物。
(2)若要收集一瓶氨,请将下列装置补充完整,在虚框内画出连接图
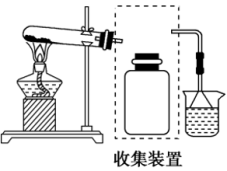
A.浓硫酸 B.碱石灰 C.NaOH固体
(4)工业上以NH3、空气、水为原料生产硝酸分为三步:
①NH3→NO:化学方程式为
②NO→NO2:实验现象是
③
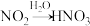 :氧化剂与还原剂的物质的量之比为
:氧化剂与还原剂的物质的量之比为(5)图1中,只用一种物质将NO直接转化为硝酸且绿色环保,则该物质的化学式为
(6)图1中,X的化学式为
您最近半年使用:0次



