1 . 氨和硝酸是重要的化工原料。工业合成氨及氨氧化制取硝酸的流程示意图如图。 和
和 反应生成
反应生成 。
。 中氮元素的化合价是
中氮元素的化合价是_______ 。
(2)氧化炉中, 转化为
转化为 。为提高该反应的化学反应速率,可采取的措施是
。为提高该反应的化学反应速率,可采取的措施是_______ (写出一条即可)。
(3)吸收塔中, 最终可转化为
最终可转化为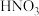 。通入空气是为了提供
。通入空气是为了提供_______ (填字母)。
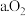
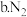
(4)尾气处理装置中,可用 将尾气中
将尾气中 还原为
还原为 。补全该反应的化学方程式:
。补全该反应的化学方程式:__________ 。
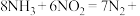 □
□

 和
和 反应生成
反应生成 。
。 中氮元素的化合价是
中氮元素的化合价是(2)氧化炉中,
 转化为
转化为 。为提高该反应的化学反应速率,可采取的措施是
。为提高该反应的化学反应速率,可采取的措施是(3)吸收塔中,
 最终可转化为
最终可转化为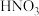 。通入空气是为了提供
。通入空气是为了提供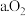
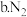
(4)尾气处理装置中,可用
 将尾气中
将尾气中 还原为
还原为 。补全该反应的化学方程式:
。补全该反应的化学方程式: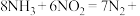 □
□
您最近一年使用:0次
解题方法
2 . 下列有关氮及其化合物的说法错误的是
| A.氮气是工业合成氨的原料 | B.氨遇氯化氢产生白烟 |
| C.铵盐受热易分解 | D.稀硝酸与铁反应产生氢气 |
您最近一年使用:0次
3 . 合成氨以及氨催化氧化制硝酸的流程如图所示。
(1)“氧化”时,产生的主要气体为___________ (填“ ”或“NO”)。
”或“NO”)。
(2)物质A不可能为___________ (填“ ”或“
”或“ ”)。
”)。
(3)浓硝酸见光易分解,通常应保存在___________ (填“棕色”或“无色”)试剂瓶中。
(4)在一定条件下发生反应: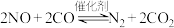 可以缓解大气中CO、NO污染问题。在1L密闭容器中加入2molNO、2molCO,在2min末测得
可以缓解大气中CO、NO污染问题。在1L密闭容器中加入2molNO、2molCO,在2min末测得 的物质的量为1mol。则:
的物质的量为1mol。则:
①2min末时NO的转化率为___________ ;
②催化剂___________ (填“可以”或“不可以”)提高反应物的转化率。

(1)“氧化”时,产生的主要气体为
 ”或“NO”)。
”或“NO”)。(2)物质A不可能为
 ”或“
”或“ ”)。
”)。(3)浓硝酸见光易分解,通常应保存在
(4)在一定条件下发生反应:
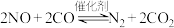 可以缓解大气中CO、NO污染问题。在1L密闭容器中加入2molNO、2molCO,在2min末测得
可以缓解大气中CO、NO污染问题。在1L密闭容器中加入2molNO、2molCO,在2min末测得 的物质的量为1mol。则:
的物质的量为1mol。则:①2min末时NO的转化率为
②催化剂
您最近一年使用:0次
4 . 氨及其化合物在工业生产中占有重要地位。回答下列问题:
(1)常温下, 是
是___________ (填“无色”或“红棕色”)气体。
(2)常温下,若将一片洁净的铝片置于浓 中,铝片不会溶解,该过程中
中,铝片不会溶解,该过程中___________ (填“发生化学反应”或“不发生化学反应”)。
(3)将氨气催化氧化的化学方程式补充完整:__________ ;
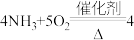 ___________
___________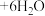 。
。
(1)常温下,
 是
是(2)常温下,若将一片洁净的铝片置于浓
 中,铝片不会溶解,该过程中
中,铝片不会溶解,该过程中(3)将氨气催化氧化的化学方程式补充完整:
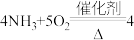 ___________
___________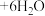 。
。
您最近一年使用:0次
5 . 氮元素的单质和常见化合物在工、农业生产中用途广泛。
(1)氮气的化学性质很稳定,可用作灯泡填充气。解释其原因是___________ 。
(2)在催化剂加热的条件下,氨气可以被二氧化氮氧化,生成氮气和水。书写该反应的化学方程式___________ 。
(3)通常用___________ (填名称)干燥氨气。
(4)铵盐大多在农业上用作化肥,固体NH4Cl与固体Ca(OH)2加热反应可生成氨气,其化学方程式为___________ 。
(5)硝酸是一种重要的含氮酸,书写铜和稀硝酸反应的离子方程式___________ 。
(1)氮气的化学性质很稳定,可用作灯泡填充气。解释其原因是
(2)在催化剂加热的条件下,氨气可以被二氧化氮氧化,生成氮气和水。书写该反应的化学方程式
(3)通常用
(4)铵盐大多在农业上用作化肥,固体NH4Cl与固体Ca(OH)2加热反应可生成氨气,其化学方程式为
(5)硝酸是一种重要的含氮酸,书写铜和稀硝酸反应的离子方程式
您最近一年使用:0次
6 . “价—类”二维图是认识和预测元素化合物及其转化关系的重要认知模型。下列有关说法不正确的是


| A.X的浓溶液需保存在棕色试剂瓶中 | B.NO既有氧化性又有还原性 |
| C.NH3能直接转化为NO | D.反应①属于氧化还原反应 |
您最近一年使用:0次
7 . 人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料,某化学兴趣小组利用图I装置制备氨并探究相关性质。
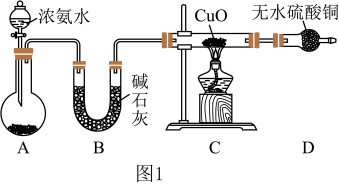
(1)装置A中,盛有浓氨水的仪器名称为________ ,烧瓶内药品可选用下列哪种试剂________ 。
A.浓硫酸 B.生石灰 C.五氧化二磷 D.二氧化硅
(2)连接好装置并检验装置的气密性后,装入药品,然后应先___________ (填“a”或“b")
a.打开旋塞逐滴向圆底烧瓶中加入氨水 b.加热装置C
(3)实验中观察到C中 粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体,则该反应相关化学方程式为
粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体,则该反应相关化学方程式为___________ ,该反应证明氨具有___________ 性。
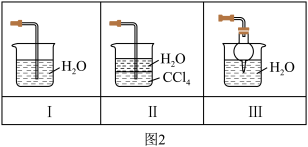
(4)该实验缺少尾气吸收装置,图2中能用来吸收尾气的装置是___________ (填装置序号)。
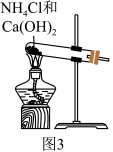
(5)实验室用图3所示装置制备氨气的化学反应方程式为___________ 。
(6)用圆底烧瓶收集干燥的氨,用图4装置进行喷泉实验,挤压胶头滴管时,可以形成红色喷泉,原因是___________ (用方程式表示)。


(1)装置A中,盛有浓氨水的仪器名称为
A.浓硫酸 B.生石灰 C.五氧化二磷 D.二氧化硅
(2)连接好装置并检验装置的气密性后,装入药品,然后应先
a.打开旋塞逐滴向圆底烧瓶中加入氨水 b.加热装置C
(3)实验中观察到C中
 粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体,则该反应相关化学方程式为
粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体,则该反应相关化学方程式为(4)该实验缺少尾气吸收装置,图2中能用来吸收尾气的装置是

(5)实验室用图3所示装置制备氨气的化学反应方程式为

(6)用圆底烧瓶收集干燥的氨,用图4装置进行喷泉实验,挤压胶头滴管时,可以形成红色喷泉,原因是

您最近一年使用:0次
解题方法
8 . 合成氨是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献,下图为合成氨以及氨氧化制硝酸的流程示意图。请回答下列问题:
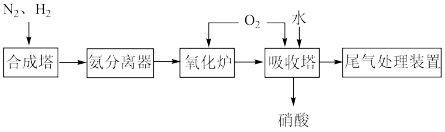
将游离态的氮转化为氮的化合物的过程叫做氮的固定。流程中发生氮的固定的设备是

将游离态的氮转化为氮的化合物的过程叫做氮的固定。流程中发生氮的固定的设备是
| A.合成塔 | B.氧化炉 | C.吸收塔 | D.尾气处理装置 |
您最近一年使用:0次
9 . 下列含氮物质常用作保护气(如填充灯泡,焊接保护等)的是
A. | B.NO | C. | D. |
您最近一年使用:0次
10 . 资源、能源、材料、环保等是当今社会重要的研究主题。请根据题意回答:
(1)中国是全球光伏发电安装量增长最快的国家。制造太阳能电池板的主要材料是______ (填“Si”或“SiO2”);
(2)将98%的浓硫酸在空气中敞口放置一段时间后,发现溶质的质量分数减小,则浓硫酸表现出______ (填“吸水性”或“脱水性”);
(3)NO是大气污染物之一。目前有一种治理方法是在400℃左右、有催化剂存在的条件下,使NH3与NO反应生成无污染的N2和H2O。该反应的化学方程式为____________ 。
(1)中国是全球光伏发电安装量增长最快的国家。制造太阳能电池板的主要材料是
(2)将98%的浓硫酸在空气中敞口放置一段时间后,发现溶质的质量分数减小,则浓硫酸表现出
(3)NO是大气污染物之一。目前有一种治理方法是在400℃左右、有催化剂存在的条件下,使NH3与NO反应生成无污染的N2和H2O。该反应的化学方程式为
您最近一年使用:0次



