名校
1 . 某校化学探究小组利用以下装置制取并探究氨气的性质。[已知生石灰与水反应生成Ca(OH)2并放出热量,实验室利用此原理往生石灰中滴加浓氨水,可以快速制取氨气。部分夹持仪器已略去]

[实验探究]
(1)装置(Ⅰ)中生石灰的化学式为_______ ,仪器a的名称是_______ 。
(2)装置(Ⅱ)中的干燥剂可选用_______ (填“碱石灰”或“浓硫酸”)。
(3)在装置(Ⅲ)连接如图所示的装置,用于收集氨气(已知氨气的密度小于空气),氨气应从导管口_______ (填“b”或“c”)通入集气瓶中。

(4)当实验进行一段时间后,挤压装置(Ⅳ)中的胶头滴管,滴入1~2滴浓盐酸,可观察到瓶内产生大量的_______ (填“白烟”或“白雾”);写出NH3与HCl反应的化学方程式:_______ 。
(5)装置(Ⅴ)中仪器d的作用是_______ 。取装置(Ⅴ)中的少量溶液于试管中,滴入1~2滴酚酞试液,溶液显_______ (填“无色”或“红色”),其原因是_______ 。
[知识应用]
(6)液氨用作制冷剂是由于液氨汽化时_______ (填“吸收”或“放出”)大量的热,使周围环境的温度降低。
(7)氨气是工业制硝酸的原料,其第一步反应为4NH3+ 5O2 4NO + 6H2O,在该反应中氨气表现出
4NO + 6H2O,在该反应中氨气表现出_______ (填“氧化性”或“还原性”),若NO 接触空气,观察到的现象是_______ 。

[实验探究]
(1)装置(Ⅰ)中生石灰的化学式为
(2)装置(Ⅱ)中的干燥剂可选用
(3)在装置(Ⅲ)连接如图所示的装置,用于收集氨气(已知氨气的密度小于空气),氨气应从导管口

(4)当实验进行一段时间后,挤压装置(Ⅳ)中的胶头滴管,滴入1~2滴浓盐酸,可观察到瓶内产生大量的
(5)装置(Ⅴ)中仪器d的作用是
[知识应用]
(6)液氨用作制冷剂是由于液氨汽化时
(7)氨气是工业制硝酸的原料,其第一步反应为4NH3+ 5O2
 4NO + 6H2O,在该反应中氨气表现出
4NO + 6H2O,在该反应中氨气表现出
您最近一年使用:0次
2 . 某化学兴趣小组利用下图装置制取、收集并探究氨气的性质。
已知: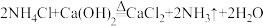


[实验探究]
(1)装置(Ⅰ)中仪器a的名称是___________ 。
(2)装置(Ⅰ)中用向下排空气法收集氨气的原因是___________ 。
(3)当实验进行一段时间后:
①用蘸有浓盐酸的玻璃棒靠近塞有棉花的试管口,观察到有白烟产生,写出该反应的化学方程式:___________ ;
②改用湿润的红色石蕊试纸靠近试管口,试纸变___________ 色,原因是___________ 。
(4)若要生成标准状况下 ,理论上参加反应的
,理论上参加反应的 的质量是
的质量是___________ g。( 的摩尔质量为
的摩尔质量为 )
)
[实验拓展]
(5)实验室也可利用装置(Ⅱ)快速制取并干燥氨气(其余装置已略去):
①锥形瓶中的固体是___________ (填“氯化钠”或“生石灰”);
②干燥管中应装的试剂是___________ (填“碱石灰”或“小苏打”)。
[知识应用]
(6)一氧化氮是大气污染物之一、目前有一种治理方法:在一定条件下,用氨气把一氧化氮还原成无色无毒气体___________ 直接排入空气中,有关反应的化学方程式为___________ 。
已知:
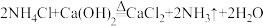


[实验探究]
(1)装置(Ⅰ)中仪器a的名称是
(2)装置(Ⅰ)中用向下排空气法收集氨气的原因是
(3)当实验进行一段时间后:
①用蘸有浓盐酸的玻璃棒靠近塞有棉花的试管口,观察到有白烟产生,写出该反应的化学方程式:
②改用湿润的红色石蕊试纸靠近试管口,试纸变
(4)若要生成标准状况下
 ,理论上参加反应的
,理论上参加反应的 的质量是
的质量是 的摩尔质量为
的摩尔质量为 )
)[实验拓展]
(5)实验室也可利用装置(Ⅱ)快速制取并干燥氨气(其余装置已略去):
①锥形瓶中的固体是
②干燥管中应装的试剂是
[知识应用]
(6)一氧化氮是大气污染物之一、目前有一种治理方法:在一定条件下,用氨气把一氧化氮还原成无色无毒气体
您最近一年使用:0次
名校
解题方法
3 . 某化学兴趣小组为制取NH3并探究其性质,按下图装置进行实验。【制取氨气的反应原理:2NH4Cl+Ca(OH)2 CaCl2+2NH3+2H2O,部分夹持仪器已略去】
CaCl2+2NH3+2H2O,部分夹持仪器已略去】
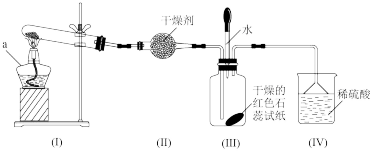
【实验探究】(1)装置(I)中仪器a的名称是_____ 。
(2)装置(Ⅱ)中可用_________ (填“碱石灰”或“食盐”)作干燥剂。
(3)实验进行一段时间后,装置(Ⅲ)中干燥的红色石蕊试纸不变色,然后滴加水,观察到试纸颜色变为___ (填“白色”或“蓝色”)原因是氨水呈____ (填“碱性”或“酸性”)。
(4)装置(Ⅲ)中胶头滴管若改装浓盐酸,实验进行一段时间后,滴加浓盐酸,观察到瓶内充满_______ (填“白烟”或“白雾”),写出NH3与HCl反应生成NH4Cl的化学方程式:_________ 。
(5)装置(IV)中稀硫酸的作用是___________ 。
(6)用0.1 mol NH4Cl与足量Ca(OH)2反应,理论上可生成NH3的物质的量是____ mol。
【实验拓展】(7)已知:2NH3+3CuO 3Cu+N2+3H2O,若把装置(Ⅲ)换为如图装置,当实验进行一段时间后,观察到黑色固体变为
3Cu+N2+3H2O,若把装置(Ⅲ)换为如图装置,当实验进行一段时间后,观察到黑色固体变为____ (填“白色”或“红色”),在这过程中NH3表现出__ (填“还原性”或“氧化性”)。
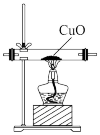
【知识应用】(8)氨气是一种重要的化工原料。写出它的一种用途:__________ 。
 CaCl2+2NH3+2H2O,部分夹持仪器已略去】
CaCl2+2NH3+2H2O,部分夹持仪器已略去】
【实验探究】(1)装置(I)中仪器a的名称是
(2)装置(Ⅱ)中可用
(3)实验进行一段时间后,装置(Ⅲ)中干燥的红色石蕊试纸不变色,然后滴加水,观察到试纸颜色变为
(4)装置(Ⅲ)中胶头滴管若改装浓盐酸,实验进行一段时间后,滴加浓盐酸,观察到瓶内充满
(5)装置(IV)中稀硫酸的作用是
(6)用0.1 mol NH4Cl与足量Ca(OH)2反应,理论上可生成NH3的物质的量是
【实验拓展】(7)已知:2NH3+3CuO
 3Cu+N2+3H2O,若把装置(Ⅲ)换为如图装置,当实验进行一段时间后,观察到黑色固体变为
3Cu+N2+3H2O,若把装置(Ⅲ)换为如图装置,当实验进行一段时间后,观察到黑色固体变为
【知识应用】(8)氨气是一种重要的化工原料。写出它的一种用途:
您最近一年使用:0次
2020-07-17更新
|
425次组卷
|
4卷引用:2020年6月福建省普通高中学业水平合格性考试化学试题
2020年6月福建省普通高中学业水平合格性考试化学试题福建省泉州市第七中学 2020--2021 学年高二上学期期末化学学业水平合格性测试二福建省莆田第七中学2021-2022学年高一下学期期中考试化学试题(已下线)专题13 元素及其化合物知识的综合应用-2020年高考真题和模拟题化学分项汇编
4 . 某化学研究性学习小组为了制取并探究氨气的性质和用途,按下列装置进行实验。(制取氨气的反应原理:2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O,部分夹持仪器已略去)
CaCl2+2NH3↑+2H2O,部分夹持仪器已略去)

【实验探究】
(1)装置(I)除制取氨气外,还可制取的气体有___________ (填一种)。
(2)装置(Ⅱ)中的干燥剂是___________ (填“碱石灰”或“氯化钙”)。
(3)实验进行一段时间后,挤压装置(Ⅲ)中的胶头滴管,滴入1~2滴浓盐酸,出现白烟,写出产生此现象的化学方程式:___________ 。
(4)装置(Ⅳ)中倒置漏斗的作用是___________ 。
(5)用10.7g NH4Cl固体与足量Ca(OH)2固体反应,理论上最多可生成NH3气体体积(标准状况下)为___________ L。(已知NH4Cl的摩尔质量为53.5g/mol)
【实验拓展】
(6)用下图所示装置(V),分别进行下列实验,描述甲烧杯中的现象。

【知识应用】
(7)氨是硝酸工业和氮肥工业的重要原料。
①氨催化氧化是工业生产硝酸的一步重要反应,把该反应的化学方程式补充完整___________ 。
4NH3+5O2 4___________+6H2O
4___________+6H2O
②碳酸氢铵是一种铵态氮肥。实验室检验碳酸氢铵中含有NH ,请从下列:a.NaOH溶液 b.稀硫酸c.蒸馏水 d.蓝色石蕊试纸 e.红色石蕊试纸中,选出需用到的试剂和试纸是
,请从下列:a.NaOH溶液 b.稀硫酸c.蒸馏水 d.蓝色石蕊试纸 e.红色石蕊试纸中,选出需用到的试剂和试纸是_____ 。
A.ace B.bcd
 CaCl2+2NH3↑+2H2O,部分夹持仪器已略去)
CaCl2+2NH3↑+2H2O,部分夹持仪器已略去)
【实验探究】
(1)装置(I)除制取氨气外,还可制取的气体有
(2)装置(Ⅱ)中的干燥剂是
(3)实验进行一段时间后,挤压装置(Ⅲ)中的胶头滴管,滴入1~2滴浓盐酸,出现白烟,写出产生此现象的化学方程式:
(4)装置(Ⅳ)中倒置漏斗的作用是
(5)用10.7g NH4Cl固体与足量Ca(OH)2固体反应,理论上最多可生成NH3气体体积(标准状况下)为
【实验拓展】
(6)用下图所示装置(V),分别进行下列实验,描述甲烧杯中的现象。

| 实验编号 | 甲烧杯中物质 | 乙烧杯中物质 | 甲烧杯中现象 |
| ① | 酚酞试液 | 浓氨水 | |
| ② | AlCl3溶液 | 浓氨水 |
(7)氨是硝酸工业和氮肥工业的重要原料。
①氨催化氧化是工业生产硝酸的一步重要反应,把该反应的化学方程式补充完整
4NH3+5O2
 4___________+6H2O
4___________+6H2O②碳酸氢铵是一种铵态氮肥。实验室检验碳酸氢铵中含有NH
 ,请从下列:a.NaOH溶液 b.稀硫酸c.蒸馏水 d.蓝色石蕊试纸 e.红色石蕊试纸中,选出需用到的试剂和试纸是
,请从下列:a.NaOH溶液 b.稀硫酸c.蒸馏水 d.蓝色石蕊试纸 e.红色石蕊试纸中,选出需用到的试剂和试纸是A.ace B.bcd
您最近一年使用:0次
5 . 某校化学探究小组利用以下装置制取并探究氨气的性质。[已知生石灰与水反应生成Ca(OH)2并放出热量,实验室利用此原理往生石灰中滴加浓氨水,可以快速制取氨气。部分夹持仪器已略去]

【实验探究】
(1)装置(Ⅰ)中生石灰的化学式为________ ,仪器a的名称是_____ 。
(2)装置(Ⅱ)中的干燥剂可选用____ (填“碱石灰”或“浓硫酸”)。
(3)在装置(Ⅲ)连接如图所示的装置,用于收集氨气(已知氨气的密度小于空气),氨气应从导管口_____ (填“b”或“c”)通入集气瓶中。

(4)当实验进行一段时间后,挤压装置(Ⅳ)中的胶头滴管,滴入1~2滴浓盐酸,可观察到瓶内产生大量的______ (填“白烟”或“白雾”),写出NH3与HCl反应的化学方程式:___________ 。
(5)装置(Ⅴ)中仪器d的作用是_______ 。取装置(Ⅴ)中的少量氨水于试管中,滴入1~2滴酚酞试液,溶液显____ (填“无色”或“红色”),其原因是_______ 。
【知识应用】
(6)液氨可作制冷剂是由于液氨汽化时_____ (填“吸收”或“放出”)大量的热,使周围环境的温度降低。
(7)氨气是工业制硝酸的原料,其第一步反应为4NH3+5O2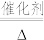 4NO+6H2O,在该反应中氮元素的化合价
4NO+6H2O,在该反应中氮元素的化合价____ (填“升高”或“降低”),氨气表现出_____ (填“氧化性”或“还原性”)。

【实验探究】
(1)装置(Ⅰ)中生石灰的化学式为
(2)装置(Ⅱ)中的干燥剂可选用
(3)在装置(Ⅲ)连接如图所示的装置,用于收集氨气(已知氨气的密度小于空气),氨气应从导管口

(4)当实验进行一段时间后,挤压装置(Ⅳ)中的胶头滴管,滴入1~2滴浓盐酸,可观察到瓶内产生大量的
(5)装置(Ⅴ)中仪器d的作用是
【知识应用】
(6)液氨可作制冷剂是由于液氨汽化时
(7)氨气是工业制硝酸的原料,其第一步反应为4NH3+5O2
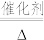 4NO+6H2O,在该反应中氮元素的化合价
4NO+6H2O,在该反应中氮元素的化合价
您最近一年使用:0次
2019-10-04更新
|
545次组卷
|
3卷引用:2019年6月福建省普通高中学业水平合格性考试化学试题



